下列框图中涉及的物质是中学化学常见的。其相互转化关系如图所示。已知:单质A在单质G中能燃烧,其产物溶于水得L;固体单C可以在B中燃烧;A、B、G通常为气态单质。请回答有关问题:
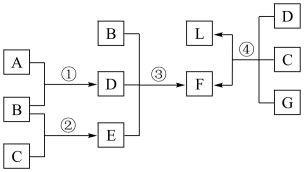
(1)写出B、L的名称:B_________ 、L_________ ;写出F在工业上的任何两点用途_______________________________________ 。
(2)写出③的化学方程式_____________________________ 。
(3)说出形成单质C的元素在元素周期表的位置,第____________ 周期,第_____ 族。
(4)将E通入到某种棕黄色的溶液中也有L、F生成。其反应的离子方程式为_______________________________________ 。
(5)写出④反应的化学方程式____________________ 。

(1)写出B、L的名称:B
(2)写出③的化学方程式
(3)说出形成单质C的元素在元素周期表的位置,第
(4)将E通入到某种棕黄色的溶液中也有L、F生成。其反应的离子方程式为
(5)写出④反应的化学方程式
2010·辽宁大连·二模 查看更多[1]
(已下线)2010年辽宁省大连市高三第二次模拟考试(理综)化学部分
更新时间:2016-12-09 00:30:13
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】在下列中学化学中常见物质的转化关系图中,已知常温下A为淡黄色固体、B为金属单质,D、E、M是常见气体单质,其中M为黄绿色,N是胃酸的主要成分,工业上用E和M来制取N,试推断:

(1)写出下列化学式 A_________________ ; I_________________ 。
(2)G转化为I的现象为___________________________________________________ 。
(3)F+M→H离子方程式为_________________________________________________ 。
(4)A+X→C+D的化学方程式为______________________________________________ 。

(1)写出下列化学式 A
(2)G转化为I的现象为
(3)F+M→H离子方程式为
(4)A+X→C+D的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D均为中学常见物质且均含有同一种元素,它们之间的部分转化关系如图所示(反应条件及其他物质已经略去):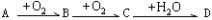 。
。
(1)若A为淡黄色固体单质,且D为强酸。则
①B物质通常用________________ (填试剂名称)来检验。
②从组成物质的元素化合价变化角度预测,B具有的与图示不相同的性质是_______________ ,并用相应的化学方程式表示你预测的性质_________________________________________________ 。
③一定条件下D转化为B有多种途径,写出其中一种D→B转化的化学方程式________________________________________ 。
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,D的稀溶液能使湿润的蓝色石蕊试纸变红。
①写出实验室制取A的化学方程式_____________________________________________ 。
②标准状况下,等物质的量的B、C形成的混合气体22.4 L,与相同条件下________ L氧气混合后溶于水,气体能被水完全吸收。
③写出C→D转化的化学方程式________________________________________________ 。
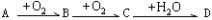 。
。(1)若A为淡黄色固体单质,且D为强酸。则
①B物质通常用
②从组成物质的元素化合价变化角度预测,B具有的与图示不相同的性质是
③一定条件下D转化为B有多种途径,写出其中一种D→B转化的化学方程式
(2)若A为能使湿润的红色石蕊试纸变蓝的气体,D的稀溶液能使湿润的蓝色石蕊试纸变红。
①写出实验室制取A的化学方程式
②标准状况下,等物质的量的B、C形成的混合气体22.4 L,与相同条件下
③写出C→D转化的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】盐X由三种常见元素组成,某科学兴趣小组称取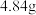 盐X进行实验,数据和现象如下:
盐X进行实验,数据和现象如下:

已知:①气体B为两种气体的混合物,能被水完全吸收。
②取D溶液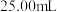 ,用
,用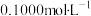 的
的 溶液滴定,消耗
溶液滴定,消耗 溶液体积
溶液体积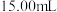 。
。
请回答:
(1)试剂Y为_______ ,气体B中的成分有_______ (填分子式)。
(2)盐X的化学式为_______ 。
(3)X的稀溶液中通入足量 气体,反应的离子方程式为
气体,反应的离子方程式为_______ 。
(4)某学生将带火星的木条放入气体B中,木条复燃,据此能否判断气体B中相对分子质量较大的成分具有助燃性_______ (填“能”或“不能”),理由是_______ 。
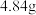 盐X进行实验,数据和现象如下:
盐X进行实验,数据和现象如下:
已知:①气体B为两种气体的混合物,能被水完全吸收。
②取D溶液
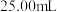 ,用
,用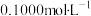 的
的 溶液滴定,消耗
溶液滴定,消耗 溶液体积
溶液体积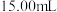 。
。请回答:
(1)试剂Y为
(2)盐X的化学式为
(3)X的稀溶液中通入足量
 气体,反应的离子方程式为
气体,反应的离子方程式为(4)某学生将带火星的木条放入气体B中,木条复燃,据此能否判断气体B中相对分子质量较大的成分具有助燃性
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:
①K2FeO4为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
②K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用。

(1)K2FeO4中铁元素的化合价为___________ 。
(2)A为氯气发生装置。发生反应的方程式为:KMnO4+HCl=MnCl2+Cl2↑+KCl+H2O,配平上述方程式______ ,并用单线桥分析该氧化还原反应的电子转移情况。
(3)装置B是为了除去Cl2中混有的HCl杂质,将除杂装置B补充完整并标明所用试剂_____ 。
(4)D中盛放的是___________ 溶液。
(5)C中得到紫色固体K2FeO4和溶液,请判断氧化性Cl2___________ K2FeO4(填“>”“=”或“<”)。C中通Cl2制得K2FeO4的化学方程式_______ ,同时还发生了另一个反应的离子方程式是_____ 。
(6)下列关于K2FeO4的说法中,正确的是___________ 。
A.是强氧化性的盐
B.固体保存需要防潮
C.其净水优点有:作用快、安全性好、无异味
(7)将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+( )H2O=( )Fe(OH)3(胶体)+( )_______+( )KOH,_________ 。
资料:
①K2FeO4为紫色固体,干燥品在室温下稳定,在碱性溶液中较稳定。随着碱性的减弱,稳定性下降,与水反应放出氧气。
②K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。
③K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用。

(1)K2FeO4中铁元素的化合价为
(2)A为氯气发生装置。发生反应的方程式为:KMnO4+HCl=MnCl2+Cl2↑+KCl+H2O,配平上述方程式
(3)装置B是为了除去Cl2中混有的HCl杂质,将除杂装置B补充完整并标明所用试剂
(4)D中盛放的是
(5)C中得到紫色固体K2FeO4和溶液,请判断氧化性Cl2
(6)下列关于K2FeO4的说法中,正确的是
A.是强氧化性的盐
B.固体保存需要防潮
C.其净水优点有:作用快、安全性好、无异味
(7)将K2FeO4与水反应的化学方程式补充完整:4K2FeO4+( )H2O=( )Fe(OH)3(胶体)+( )_______+( )KOH,
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】氯气是一种重要的化工原料,在生产和生活中的应用十分广泛。某化学兴趣小组在实验室中对Cl2与FeCl2和KSCN混合溶液的反应进行了探究。回答下列问题:
(1)氯气的制备

①氯气的发生装置可以选择上图中的_________ ,反应的化学方程式为_________________ 。
②欲收集一瓶干燥纯净的氯气,选择上图中的装置,其连接顺序为______________ (按气流方向,用小写字母表示)。
(2)Cl2与FeCl2和KSCN混合溶液的反应
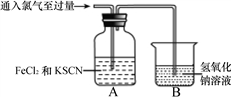
随着Cl2不断通入,A装置中溶液先变红,后由红色变为黄色。
装置B中发生反应的离子方程式为___________________________________________ 。
(3)实验探究
为了探究A装置中溶液由红色变为黄色的原因,该小组进行了如下实验:
实验一:取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成。
实验二:取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
该兴趣小组根据实验现象,猜想是SCN−可能被Cl2氧化了,他们又进行了如下研究。
查阅资料显示:SCN−的电子式为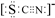 。
。
①该兴趣小组认为SCN−中碳元素没有被氧化,理由是____________________________ 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN−中被氧化的元素是________ (填元素名称)。
③通过实验证明了SCN−中氮元素转化为NO3−,他们的实验方案是__________________________________________________________________________________________________ 。
根据以上实验探究结论写出SCN−与Cl2反应的离子方程式为__________________________ 。
(1)氯气的制备

①氯气的发生装置可以选择上图中的
②欲收集一瓶干燥纯净的氯气,选择上图中的装置,其连接顺序为
(2)Cl2与FeCl2和KSCN混合溶液的反应

随着Cl2不断通入,A装置中溶液先变红,后由红色变为黄色。
装置B中发生反应的离子方程式为
(3)实验探究
为了探究A装置中溶液由红色变为黄色的原因,该小组进行了如下实验:
实验一:取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成。
实验二:取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
该兴趣小组根据实验现象,猜想是SCN−可能被Cl2氧化了,他们又进行了如下研究。
查阅资料显示:SCN−的电子式为
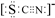 。
。①该兴趣小组认为SCN−中碳元素没有被氧化,理由是
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN−中被氧化的元素是
③通过实验证明了SCN−中氮元素转化为NO3−,他们的实验方案是
根据以上实验探究结论写出SCN−与Cl2反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】实验室用浓盐酸与二氧化锰加热制氯气,并研究氯气的性质。完成下列填空:
(1)仪器A的名称是_____ 。用排饱和NaCl溶液的方法收集氯气时,往往会有白色晶体析出,写出晶体的化学式______ 。
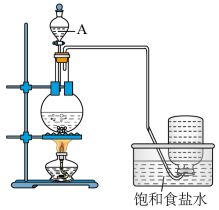
(2)将所产生的气体缓慢通入如图装置:
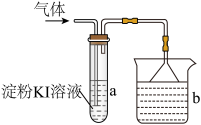
①试管a中观察到的现象是_____ 。
②当气体过量时,试管a中有HIO3生成。若n(HIO3)=2.0×10-3mol,则上述实验中产生的氯气不小于___ mL(标准状况下)。
(3)烧杯b中盛NaOH溶液,其作用是______ ,写出此反应的离子方程式_____ ,烧杯b处可观察到的现象是_____ 。
(4)试管a中的混合液体换为NaBr溶液时,再缓慢通气体,溶液变为____ 色,气体过量后溶液颜色保持不变。由此推断HBrO3、Cl2、Br2氧化性由强到弱的顺序是_____ 。
(1)仪器A的名称是

(2)将所产生的气体缓慢通入如图装置:

①试管a中观察到的现象是
②当气体过量时,试管a中有HIO3生成。若n(HIO3)=2.0×10-3mol,则上述实验中产生的氯气不小于
(3)烧杯b中盛NaOH溶液,其作用是
(4)试管a中的混合液体换为NaBr溶液时,再缓慢通气体,溶液变为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】绿水青山就是金山银山。绿色发展、生态保护已成为中国展示给世界的一张新“名片”。回答下列问题:
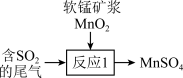
(1)硫酸工业排出的尾气(主要含 )可用软锰矿浆吸收,写出如图所示“反应1”的化学方程式
)可用软锰矿浆吸收,写出如图所示“反应1”的化学方程式_______ 。 造成的一种常见环境污染为
造成的一种常见环境污染为_______ 。
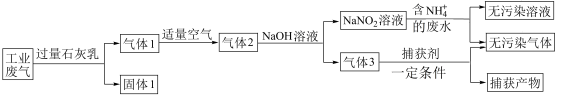
(2)某种综合处理含 ,废水和工业废气(主要含
,废水和工业废气(主要含 、
、 、
、 、
、 、
、 )的流程如图:
)的流程如图:
已知: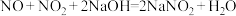 ,
,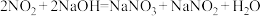 。
。
①固体1的主要成分有 、
、_______ (填化学式)。
②若实验室需要配制
 溶液1L进行模拟测试,需称取
溶液1L进行模拟测试,需称取 固体的质量为
固体的质量为_______ g。
③用 溶液处理含
溶液处理含 废水反应的离子方程式为
废水反应的离子方程式为_______ 。
④验证废水中 已基本除净的方法是
已基本除净的方法是_______ (写出操作、现象及结论)。
⑤捕获产物主要是_______ (填化学式)。
⑥气体1转化为气体2时空气不能过量的原因是_______ 。
(1)硫酸工业排出的尾气(主要含
 )可用软锰矿浆吸收,写出如图所示“反应1”的化学方程式
)可用软锰矿浆吸收,写出如图所示“反应1”的化学方程式 造成的一种常见环境污染为
造成的一种常见环境污染为
(2)某种综合处理含
 ,废水和工业废气(主要含
,废水和工业废气(主要含 、
、 、
、 、
、 、
、 )的流程如图:
)的流程如图:
已知:
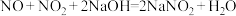 ,
,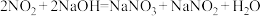 。
。①固体1的主要成分有
 、
、②若实验室需要配制

 溶液1L进行模拟测试,需称取
溶液1L进行模拟测试,需称取 固体的质量为
固体的质量为③用
 溶液处理含
溶液处理含 废水反应的离子方程式为
废水反应的离子方程式为④验证废水中
 已基本除净的方法是
已基本除净的方法是⑤捕获产物主要是
⑥气体1转化为气体2时空气不能过量的原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某化学兴趣小组为验证SO2的还原性,特邀你参与以下探究活动。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的分析,你认为可能观察到的现象是:_____________ ,你预测的理论依据是(用离子方程式表示):________________________ 。
II.实验探究
(1)配制1mol/LFeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:_______________ 。
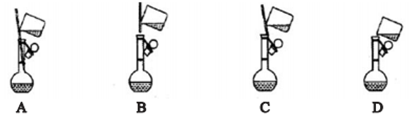
②测溶液的pH得知溶液呈酸性,其原因是:____________________ (用离子方程式表示)。
(2)SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:_______________ 。
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。
请你推测小组在实验方案设计中“加浓HCl酸化”的目的是:_______________ 。
III.感悟与分享
通过探究,小组同学深受启发、感悟良多。比如,有同学认为“实验才是化学的最高法庭”。请写出一种你的感悟与同学分享:______________________ 。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的分析,你认为可能观察到的现象是:
II.实验探究
(1)配制1mol/LFeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:

②测溶液的pH得知溶液呈酸性,其原因是:
(2)SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。
请你推测小组在实验方案设计中“加浓HCl酸化”的目的是:
III.感悟与分享
通过探究,小组同学深受启发、感悟良多。比如,有同学认为“实验才是化学的最高法庭”。请写出一种你的感悟与同学分享:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】 是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如下:
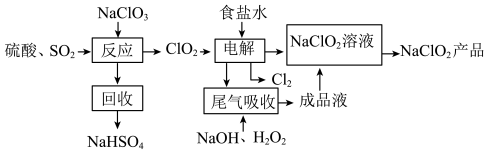
请回答:
(1) 中氯元素化合价为
中氯元素化合价为_______ ,它在流程的“反应”中作_______ (“氧化剂”、“还原剂”、“氧化剂和还原剂”)。
(2)“电解”所用食盐水要除去其中含有的 和
和 ,需要先后加入一定量
,需要先后加入一定量 溶液和
溶液和_______ (化学式)溶液,充分反应后并过滤,所得溶液再加入_______ (化学式)溶液至中性。
(3)“尾气吸收”是吸收“电解”过程排出过量的 ,“电解”步骤发生的化学反应为:
,“电解”步骤发生的化学反应为:_______ 。
(4)“电解”产生的氯气中可用石灰乳吸收制成漂白粉,写出生成漂白粉的化学方程式_______ 。
 是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如下:
是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺流程如下:
请回答:
(1)
 中氯元素化合价为
中氯元素化合价为(2)“电解”所用食盐水要除去其中含有的
 和
和 ,需要先后加入一定量
,需要先后加入一定量 溶液和
溶液和(3)“尾气吸收”是吸收“电解”过程排出过量的
 ,“电解”步骤发生的化学反应为:
,“电解”步骤发生的化学反应为:(4)“电解”产生的氯气中可用石灰乳吸收制成漂白粉,写出生成漂白粉的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】回答以下关于元素及其化合物的问题。
(1)Na原子核外有________ 种不同能量的电子,其离子最外层电子的轨道表示式________ 。
(2)相同压强下,部分元素氟化物的熔点见下表:
①试解释上表中氟化物熔点差异的原因:___________ 。
② 分子的空间构型为
分子的空间构型为___________ , 中Si—F键间的键角是
中Si—F键间的键角是___________ 。
(3)元素周期表有多种形式。下图分别是三种不同形式元素周期表的局部区域。

①图A中,数值越大,则该元素的___________ (填“金属性”或“非金属性”)越强。写出能说明O、F两元素该性质强弱的化学方程式___________ 。
②根据图B预测,整个周期表中位置最低的元素应位于___________ (放射性元素除外)。图B所示第二周期主族元素中,某元素该性质反常偏高,则该元素原子核外电子排布式为___________ 。
③图C表示的意义是___________ 。
(4)元素周期表中,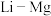 、
、 、
、 处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
(1)Na原子核外有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 |  |  |  |
| 熔点/℃ | 1266 | 1534 | 183 |
②
 分子的空间构型为
分子的空间构型为 中Si—F键间的键角是
中Si—F键间的键角是(3)元素周期表有多种形式。下图分别是三种不同形式元素周期表的局部区域。

①图A中,数值越大,则该元素的
②根据图B预测,整个周期表中位置最低的元素应位于
③图C表示的意义是
(4)元素周期表中,
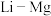 、
、 、
、 处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。
处于对角线关系,其单质与化合物的性质相似。下列说法正确的是___________(选填序号)。A. 易溶于水 易溶于水 | B. |
C. 熔点高 熔点高 | D.晶体硼为分子晶体 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】(I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:_______ ,属于_______ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
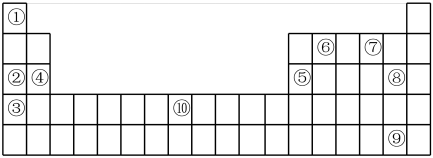
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是_______ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为_______ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为_______ ;
(5)元素⑩的名称为_______ ,其单质与⑧的单质反应的化学方程式为_______ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是_______
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩的名称为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】镓(Ga)是非常重要的稀土金属,其化合物广泛应用于诸多领域。
(1)镓元素在元素周期表中的位置是___________ 。
(2)GaN作为第三代半导体材料,广泛应用于大功率充电器和5G通讯技术。工业上利用炼锌矿渣[主要含可溶性铁酸镓 、铁酸锌
、铁酸锌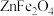 ]制备并提取GaN,工艺流程如下:
]制备并提取GaN,工艺流程如下:
①“酸浸”过程中 发生的反应的离子方程式为
发生的反应的离子方程式为___________ 。
②利用上述工艺,酸浸后的酸浸液应加入___________ 固体充分反应后再进行萃取。
③“反萃取”后,溶液中镓元素的存在形式为___________ (填离子符号)。
④回收金属元素时,锌主要从___________ 中回收。
A.浸出渣 B.酸浸液 C.水相 D.有机相
(3)MOCVD法是通过 与
与 反应得到GaN和另一种产物,该反应的化学方程式为
反应得到GaN和另一种产物,该反应的化学方程式为___________ 。
(4)该流程中,可以循环使用的物质是___________ 。
(1)镓元素在元素周期表中的位置是
(2)GaN作为第三代半导体材料,广泛应用于大功率充电器和5G通讯技术。工业上利用炼锌矿渣[主要含可溶性铁酸镓
 、铁酸锌
、铁酸锌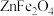 ]制备并提取GaN,工艺流程如下:
]制备并提取GaN,工艺流程如下: 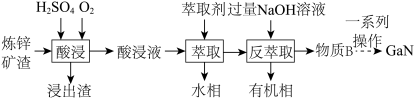
| 金属离子 |  |  |  |  |
| 萃取率/% | 0 | 0 | 99 | 97~98.5 |
 发生的反应的离子方程式为
发生的反应的离子方程式为②利用上述工艺,酸浸后的酸浸液应加入
③“反萃取”后,溶液中镓元素的存在形式为
④回收金属元素时,锌主要从
A.浸出渣 B.酸浸液 C.水相 D.有机相
(3)MOCVD法是通过
 与
与 反应得到GaN和另一种产物,该反应的化学方程式为
反应得到GaN和另一种产物,该反应的化学方程式为(4)该流程中,可以循环使用的物质是
您最近一年使用:0次



