A、B、C、D、E、X是中学常见的无机物,存在如图所示转化关系(部分生成物和反应条件略去);已知A由短周期非金属元素组成,B具有漂白性且光照易分解。

(1)若A为单质,且C为一种强酸,请回答以下问题:①组成单质A的元素在元素周期表中的位置为___________________ ;用电子式表示C 的形成过程____________________ 。
②A与H2O反应的离子反应方程式为______________________ 。
③X可能为_______________ (填代号)
a.NaOH b.AlCl3c.Na2CO3d.NaAlO 2
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生,则:①B的电子式为_________________ 。
②A与H2O反应的化学反应方程式为_______________________ 。

(1)若A为单质,且C为一种强酸,请回答以下问题:①组成单质A的元素在元素周期表中的位置为
②A与H2O反应的离子反应方程式为
③X可能为
a.NaOH b.AlCl3c.Na2CO3d.NaAlO 2
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生,则:①B的电子式为
②A与H2O反应的化学反应方程式为
更新时间:2016-12-09 14:58:53
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】某无机化合物A由X、Y两种元素组成。在空气中充分灼烧得到含X元素的8g红棕色固体B,并产生能使品红褪色的气体C,将该气体全部通入足量的双氧水中得D溶液,再向D溶液中加入足量的BaCl2溶液,过滤、洗涤、干燥得46.6g固体。
(1)写出X在元素周期表中的位置___________ ,写出Y2-的结构示意图___________ ,写出B的化学式___________
(2)写出气体C通入H2O2中反应的离子方程式_________
(3)将A溶于D的稀溶液中得到E,并产生一种单质固体和一种气体,写出该反应的化学方程式_________
(4)将化合物E固体隔绝空气充分灼烧,使其分解,生成等物质的量的B、C和另一种化合物,则另一种化合物的分子式是______ ;
(1)写出X在元素周期表中的位置
(2)写出气体C通入H2O2中反应的离子方程式
(3)将A溶于D的稀溶液中得到E,并产生一种单质固体和一种气体,写出该反应的化学方程式
(4)将化合物E固体隔绝空气充分灼烧,使其分解,生成等物质的量的B、C和另一种化合物,则另一种化合物的分子式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】化合物X由四种元素组成,按如下流程进行实验。混合气体A由气体E和元素种类相同的另两种气体组成,且气体C的平均相对分子质量为8.5。混合物B中有两种固体。
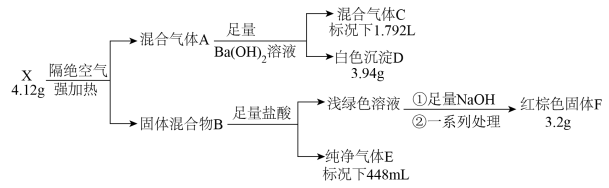
请回答:
(1)组成X的四种元素为_______ ;X的化学式为_______ 。
(2)写出由X到A的化学方程式_______ 。
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因_______ 。
(4)设计实验检验混合气体A中相对分子量较小的两种气体_______ 。

请回答:
(1)组成X的四种元素为
(2)写出由X到A的化学方程式
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因
(4)设计实验检验混合气体A中相对分子量较小的两种气体
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】化合物X由4种元素组成。某兴趣小组按如下流程进行实验:

已知:无色溶液A、B均为单一溶质,气体D为纯净物。
请回答:
(1)组成X的元素有___________ ,X的化学式为___________ 。
(2)X溶于 的反应化学方程式为
的反应化学方程式为___________ 。
(3)光学实验证明,溶有气体单质D(表示为 )的水中存在水合分子
)的水中存在水合分子 、
、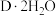 。对于两种分子的结构,下列表示正确的是___________。
。对于两种分子的结构,下列表示正确的是___________。
(4)①某同学利用铜与流程中所涉及的物质制备蓝色溶液。资料显示,溶液显蓝色的原因是稀溶液中存在水合铜离子 。写出该反应的离子方程式
。写出该反应的离子方程式___________ 。
②请在该同学实验的基础上,设计实验证明溶液显蓝色的原因___________ 。

已知:无色溶液A、B均为单一溶质,气体D为纯净物。
请回答:
(1)组成X的元素有
(2)X溶于
 的反应化学方程式为
的反应化学方程式为(3)光学实验证明,溶有气体单质D(表示为
 )的水中存在水合分子
)的水中存在水合分子 、
、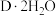 。对于两种分子的结构,下列表示正确的是___________。
。对于两种分子的结构,下列表示正确的是___________。A. | B. | C. | D. |
 。写出该反应的离子方程式
。写出该反应的离子方程式②请在该同学实验的基础上,设计实验证明溶液显蓝色的原因
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
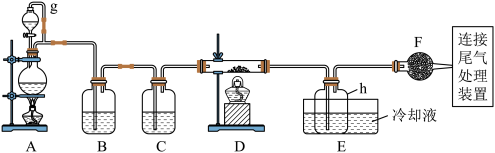
相关信息:①四氯化硅遇水极易水解;② 沸点为57.7℃,熔点为-70.0℃。请回答:
沸点为57.7℃,熔点为-70.0℃。请回答:
(1)写出装置A中发生反应的离子方程式______ 。
(2)装置C中的试剂是______ ;装置F的作用是______ ;装置E中的h瓶需要冷却的理由是______ 。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中含有铁元素,为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①反应的离子方程式:______ 。
②滴定前是否要滴加指示剂?______ (填“是”或“否”),请说明理由______ 。
③滴定前检验Fe3+是否被完全还原的实验操作是______ 。

相关信息:①四氯化硅遇水极易水解;②
 沸点为57.7℃,熔点为-70.0℃。请回答:
沸点为57.7℃,熔点为-70.0℃。请回答:(1)写出装置A中发生反应的离子方程式
(2)装置C中的试剂是
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中含有铁元素,为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①反应的离子方程式:
②滴定前是否要滴加指示剂?
③滴定前检验Fe3+是否被完全还原的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】氯化铁在金属蚀刻、污水处理等方面有广泛应用。某兴趣小组以废铁屑为原料,用如图所示装置制备FeCl3·6H2O。
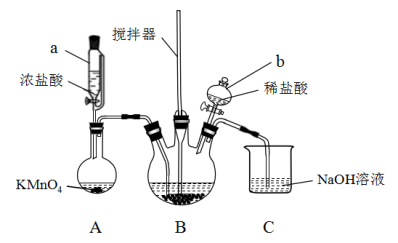
已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。
实验步骤:
I.废铁屑的净化:取一只小烧杯,放入约5 g废铁屑,向其中注入15 mL 1 mol·L−1
Na2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
II.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
III.FeCl3溶液的制备:由装置A制备氯气,向FeCl2的混合液中缓慢通入足量的氯气。
IV.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
V.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
请回答:
(1)步骤I,从碳酸钠溶液中分离出铁屑的方法是___________ 。
(2)下列有关装置仪器的说法不正确 的是___________ 。
A.装置A、B之间应加装一个盛有饱和食盐水的洗气瓶
B.装置B中,搅拌器的作用是使反应混合物充分接触
C.装置C中,NaOH溶液的作用是吸收逸出的氯气,防止空气污染
D.仪器a和仪器b的功能相同,操作方法也相同
(3)下列说法正确的是___________ 。
A.步骤II,稀盐酸适当过量的目的是提高铁屑的利用率并抑制水解
B.步骤III,可用K4Fe(CN)6溶液检验“含有FeCl3的混合液”中是否存在Fe2+
C.步骤IV ,蒸发浓缩要适度,浓缩度太小产率偏低,浓缩度太大纯度偏低
D.步骤IV,在冷却结晶后的固液混合物中加入甘油可提高产率
(4)已知碘量法的滴定反应:I2 + 2Na2S2O3 = 2NaI + Na2S4O6
①测定FeCl3·6H2O产品纯度的步骤选项如下,请排序(操作不能重复使用):用电子天平称取5.000 g粗产品→配成250mL溶液→_____ →_____ →_____ →_____ →计算FeCl3·6H2O纯度。
a.加入稍过量的KI溶液,充分反应
b.用碱式滴定管取出25.00 mL待测液于锥形瓶中
c.用淀粉溶液作指示剂,用c mol·L−1 Na2S2O3标准溶液滴定
d.平行滴定三次,消耗标准溶液的体积平均值为V mL
e.用移液管取出25.00 mL待测液于锥形瓶中
②如果碱式滴定管的乳胶管中有气泡,会导致滴定溶液体积不准确,因此,必须排出乳胶管中的气泡。具体操作是:把乳胶管向上弯曲,___________ ,使溶液从尖嘴快速喷出,气泡即可随之排掉。(请在横线上补全操作)
③实验中测得FeCl3·6H2O的产品纯度偏低,若操作过程无误,请从物质性质和反应原理角度分析,可能的原因是___________ (写出一种即可)。

已知:FeCl3易溶于水、甲醇、乙醇,不溶于甘油。
实验步骤:
I.废铁屑的净化:取一只小烧杯,放入约5 g废铁屑,向其中注入15 mL 1 mol·L−1
Na2CO3溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
II.FeCl2溶液的制备:将处理后的废铁屑加入装置B的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含FeCl2的混合液。
III.FeCl3溶液的制备:由装置A制备氯气,向FeCl2的混合液中缓慢通入足量的氯气。
IV.FeCl3·6H2O产品的分离提纯:将三颈烧瓶中的FeCl3混合液转移出来,经蒸发浓缩、冷却结晶、过滤、洗涤、重结晶、干燥,得到FeCl3·6H2O产品。
V.FeCl3·6H2O产品的纯度测定:用碘量法滴定并计算。
请回答:
(1)步骤I,从碳酸钠溶液中分离出铁屑的方法是
(2)下列有关装置仪器的说法
A.装置A、B之间应加装一个盛有饱和食盐水的洗气瓶
B.装置B中,搅拌器的作用是使反应混合物充分接触
C.装置C中,NaOH溶液的作用是吸收逸出的氯气,防止空气污染
D.仪器a和仪器b的功能相同,操作方法也相同
(3)下列说法正确的是
A.步骤II,稀盐酸适当过量的目的是提高铁屑的利用率并抑制水解
B.步骤III,可用K4Fe(CN)6溶液检验“含有FeCl3的混合液”中是否存在Fe2+
C.步骤IV ,蒸发浓缩要适度,浓缩度太小产率偏低,浓缩度太大纯度偏低
D.步骤IV,在冷却结晶后的固液混合物中加入甘油可提高产率
(4)已知碘量法的滴定反应:I2 + 2Na2S2O3 = 2NaI + Na2S4O6
①测定FeCl3·6H2O产品纯度的步骤选项如下,请排序(操作不能重复使用):用电子天平称取5.000 g粗产品→配成250mL溶液→
a.加入稍过量的KI溶液,充分反应
b.用碱式滴定管取出25.00 mL待测液于锥形瓶中
c.用淀粉溶液作指示剂,用c mol·L−1 Na2S2O3标准溶液滴定
d.平行滴定三次,消耗标准溶液的体积平均值为V mL
e.用移液管取出25.00 mL待测液于锥形瓶中
②如果碱式滴定管的乳胶管中有气泡,会导致滴定溶液体积不准确,因此,必须排出乳胶管中的气泡。具体操作是:把乳胶管向上弯曲,
③实验中测得FeCl3·6H2O的产品纯度偏低,若操作过程无误,请从物质性质和反应原理角度分析,可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】一种用 溶液和KI溶液探究氯气性质的实验装置如下图所示:
溶液和KI溶液探究氯气性质的实验装置如下图所示:
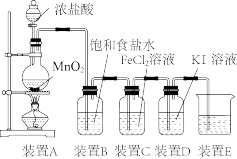
已知:氧化性: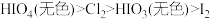 。
。
(1)装置C反应后溶液变为黄绿色。设计检验溶液中是否存在 的实验方案:
的实验方案:_______ 。
(2)实验中观察到装置D中溶液开始时变为棕黄色,后棕黄色消失变为无色,最终变为黄绿色。写出装置D中溶液由棕黄色变为无色时所发生反应的化学方程式:_______ 。
(3)KI溶液还可用于制取CuI固体。一种制取CuI固体的方法是:取一定量的 溶液,向其中加入过量KI溶液,用
溶液,向其中加入过量KI溶液,用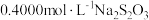 标准溶液滴定生成的
标准溶液滴定生成的 至终点,恰好完全反应时消耗
至终点,恰好完全反应时消耗 的溶液20.00mL。制备过程中发生下列反应:
的溶液20.00mL。制备过程中发生下列反应: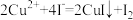 、
、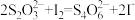
①向 溶液中加入KI溶液时,判断KI溶液已过量的方法是
溶液中加入KI溶液时,判断KI溶液已过量的方法是_______ 。
②计算所得CuI固体的质量,并写出计算过程_______ 。
 溶液和KI溶液探究氯气性质的实验装置如下图所示:
溶液和KI溶液探究氯气性质的实验装置如下图所示:
已知:氧化性:
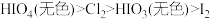 。
。(1)装置C反应后溶液变为黄绿色。设计检验溶液中是否存在
 的实验方案:
的实验方案:(2)实验中观察到装置D中溶液开始时变为棕黄色,后棕黄色消失变为无色,最终变为黄绿色。写出装置D中溶液由棕黄色变为无色时所发生反应的化学方程式:
(3)KI溶液还可用于制取CuI固体。一种制取CuI固体的方法是:取一定量的
 溶液,向其中加入过量KI溶液,用
溶液,向其中加入过量KI溶液,用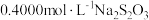 标准溶液滴定生成的
标准溶液滴定生成的 至终点,恰好完全反应时消耗
至终点,恰好完全反应时消耗 的溶液20.00mL。制备过程中发生下列反应:
的溶液20.00mL。制备过程中发生下列反应: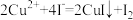 、
、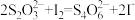
①向
 溶液中加入KI溶液时,判断KI溶液已过量的方法是
溶液中加入KI溶液时,判断KI溶液已过量的方法是②计算所得CuI固体的质量,并写出计算过程
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】五种短周期元素A、B、C、D、E,原子序数依次增大,其中A、B同周期,且A、B原子核外均有两个未成对电子;A、D同主族,B、E同主族,且C的最外层电子比E的最外层电子少5个。根据以上信息,完成下列各题。
(1)写出下列化学用语:A:_____ B:_____ C:_____ D:_______ E:_______
(2)A的最高价氧化物的熔点_________ D的最高价氧化物的熔点(填“>”或“<”),原因是_______________________ ;B氢化物的沸点______ E氢化物的沸点(填“>”或“<”),原因是______________ 。
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有___________________ ;
②含有非极性键的离子化合物__________________ (用电子式表示)
③含有极性键的非极性分子_______________ (用电子式表示)
(1)写出下列化学用语:A:
(2)A的最高价氧化物的熔点
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有
②含有非极性键的离子化合物
③含有极性键的非极性分子
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】已知A、B、C、D都是短周期元素,它们的原子半径大小顺序为B>C>D>A。B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子有2个未成对电子。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体。E是第4周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满。试回答下列(1)~(4)问题(用元素符号或化学式表示)
(1)基态E2+的核外价电子排布式为___________ 。
(2)基态D原子的最高能级的轨道表示式为___________ 。
(3)M分子中B原子轨道的杂化类型为___________ 。
(4)基态C原子核外电子云有___________ 种不同的伸展方向,共有___________ 种不同能级组的电子。
(5)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1,若该反应中形成的π键有9mol,则有___________ molN-H键断裂。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在___________ (填标号)
a.离子键b.共价键c.配位键d.范德华力
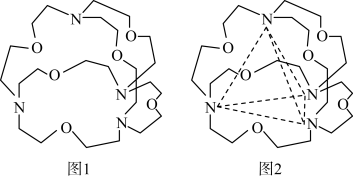
③图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________ (填标号)。
a.CF4 b.CH4 c.NH d.H2O
d.H2O
(1)基态E2+的核外价电子排布式为
(2)基态D原子的最高能级的轨道表示式为
(3)M分子中B原子轨道的杂化类型为
(4)基态C原子核外电子云有
(5)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1,若该反应中形成的π键有9mol,则有
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a.离子键b.共价键c.配位键d.范德华力
③图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是
a.CF4 b.CH4 c.NH
 d.H2O
d.H2O
您最近一年使用:0次



