(1)在2L的密闭容器中,加入2molSO2、1.2molO2,充分反应后,容器内压强为反应前的3/4,则SO2、O2 的转化率分别为多少?___________ 、 __________ 。
(2)将11. 2L标准状况下的甲烷和乙烯的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了5.6g,求原混合气体中甲烷与乙烯的质量之比。__________ 。
(2)将11. 2L标准状况下的甲烷和乙烯的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了5.6g,求原混合气体中甲烷与乙烯的质量之比。
9-10高一下·河北·阶段练习 查看更多[1]
(已下线)09—10学年衡中高一下学期第二次调研化学试卷
更新时间:2010-06-26 16:22:56
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】硫的化合物和氮的化合物在化工生产中有重要作用,试回答以下问题:
(1)在干燥烧瓶中用向下排空气法收集氨气(已知:空气不可能排净,空气的平均相对分子质量为29,瓶内气体对氢气的相对密度为9.5,氨气极易溶于水),将此瓶气体倒置于水槽中, 烧瓶内液面上升的体积占烧瓶总体积的____ 。
(2)标准状况下,容积5600 mL的烧瓶充满NH3,设NA为阿伏加德罗常数的值。
(a)集满空气时,该烧瓶总质量为a g,则集满NH3时该烧瓶总质量为____ 。
(b)烧瓶中气体原子的总数是____ 。
(3)硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4·SO3)……等。其中硫酸最为重要,在工业上有广泛的应用。已知焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将89 g焦硫酸溶于水配成800 mL硫酸,则该硫酸的物质的量浓度为____ 。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8O2=Fe3O4+6SO2,4FeS2+ 11O2=2Fe2O3+ 8SO2,若2.4 mol FeS2完全反应耗用氧气145.6 L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比_____ 。
(1)在干燥烧瓶中用向下排空气法收集氨气(已知:空气不可能排净,空气的平均相对分子质量为29,瓶内气体对氢气的相对密度为9.5,氨气极易溶于水),将此瓶气体倒置于水槽中, 烧瓶内液面上升的体积占烧瓶总体积的
(2)标准状况下,容积5600 mL的烧瓶充满NH3,设NA为阿伏加德罗常数的值。
(a)集满空气时,该烧瓶总质量为a g,则集满NH3时该烧瓶总质量为
(b)烧瓶中气体原子的总数是
(3)硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4·SO3)……等。其中硫酸最为重要,在工业上有广泛的应用。已知焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将89 g焦硫酸溶于水配成800 mL硫酸,则该硫酸的物质的量浓度为
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8O2=Fe3O4+6SO2,4FeS2+ 11O2=2Fe2O3+ 8SO2,若2.4 mol FeS2完全反应耗用氧气145.6 L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】用200 mL 1 mol/L 氯化铝溶液与一定量 3 mol/L的氢氧化钠溶液混合,可得到氢氧化铝7.8g,请计算需要此氢氧化钠溶液的体积为多少毫升?(写计算步骤)________
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)在同温同压下,两个体积相同的玻璃密闭容器中分别盛满氮气和氧气,则容器中氮气和氧气的质量之比为___________________________ 。
(2)在标准状况下,11.2L某氮氧化物NOx气体的质量是23g,则x的值为___________________ 。
(3)200 mL Fe2(SO4)3溶液中含56g Fe3+,溶液中SO42—的物质的量浓度是___________________ 。
(4)一定质量的某金属元素R的硝酸盐受热完全分解,反应按下式进行:2R(NO3)2=2RO+4NO2↑+O2↑若得到1mol RO固体,则得到的气体在标准状况下的总体积是__________ 。
(2)在标准状况下,11.2L某氮氧化物NOx气体的质量是23g,则x的值为
(3)200 mL Fe2(SO4)3溶液中含56g Fe3+,溶液中SO42—的物质的量浓度是
(4)一定质量的某金属元素R的硝酸盐受热完全分解,反应按下式进行:2R(NO3)2=2RO+4NO2↑+O2↑若得到1mol RO固体,则得到的气体在标准状况下的总体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)在某一容积为2L的密闭容器中,某一反应中A、B、C、D四种气体的物质的量n(mol)随时间t(min)的变化曲线如图所示:
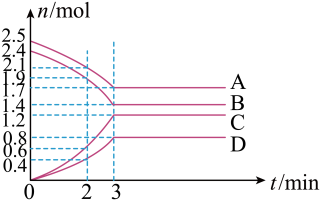
回答下列问题:
①该反应的化学方程式为___ 。
②前2min用A的浓度变化表示的化学反应速率为__ 。在2min时,图像发生改变的原因可能是__ (填字母)。
a.增大压强 b.降低温度 c.加入催化剂 d.增加A的物质的量
(2)在100℃时,将0.01mol的N2O4气体充入0.1L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
试填空:
①该反应的化学方程式__ ,达到平衡时N2O4的转化率为__ 。
②在0~20s内,四氧化二氮的平均反应速率为__ 。

回答下列问题:
①该反应的化学方程式为
②前2min用A的浓度变化表示的化学反应速率为
a.增大压强 b.降低温度 c.加入催化剂 d.增加A的物质的量
(2)在100℃时,将0.01mol的N2O4气体充入0.1L的密闭容器中发生反应,隔一定时间对该容器内的物质进行分析,得到如下表格:
| 时间/s 浓度/mol·L-1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/mol·L-1 | 0.100 | 0.070 | 0.050 | a | b | c |
| c(NO2)/mol·L-1 | 0.000 | 0.060 | d | 0.120 | 0.120 | 0.120 |
试填空:
①该反应的化学方程式
②在0~20s内,四氧化二氮的平均反应速率为
您最近一年使用:0次
【推荐2】已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) ==COS(g)+H2O(g),在610K时,将0.1mol CO2加入与0.40molH2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
①H2S的平衡转化率a1=_______ %,反应平衡常数K=___________ 。
②在620K重复实验,平衡后水的物质的量分数为003,H2S的转化率a2____ a1,该反应的ΔH___ 0。(填“>”“<”或“=”)
①H2S的平衡转化率a1=
②在620K重复实验,平衡后水的物质的量分数为003,H2S的转化率a2
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】乙炔广泛用于焊接、焊割及有机合成等方面。
(1)已知下列热化学方程式:
4CH4 (g)+3O2(g)==2C2H2(g)+6H2O(g) △H1=a kJ•mol-1;
2H2(g)+O2(g)==2H2O(g) △H2=b kJ•mol-1;
2CH4(g)==C2H2(g)+3H2 (g) △H3
①△H3=____________________ (用含a、b的代数式表示)kJ•mol-1。
②已知下列共价键的键能数据:
则△H3=____________________ (填数值)kJ•mol-1。
(2)氯仿(CHCl3)与金属银共热可以制取乙炔,该反应的化学方程式为__________________________ 。
(3)向压强为1.0×104 kPa的恒压密闭容器中充入1 mol乙炔和1 mol HCl气体,在催化剂作用下乙炔与HCl发生反应:HC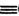 CH(g)+HCl(g)
CH(g)+HCl(g) CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
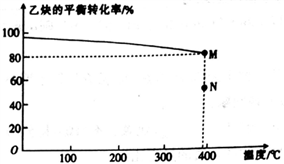
①该反应的△H__________ (填“>”或“<”)0,N点时乙炔的反应速率v(正)________ (填“>”或“<” 或“=”) v(逆)。
② M点对应温度下,该反应的平衡常数Kp=_________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(kPa)-1,
(1)已知下列热化学方程式:
4CH4 (g)+3O2(g)==2C2H2(g)+6H2O(g) △H1=a kJ•mol-1;
2H2(g)+O2(g)==2H2O(g) △H2=b kJ•mol-1;
2CH4(g)==C2H2(g)+3H2 (g) △H3
①△H3=
②已知下列共价键的键能数据:
| 共价键 | C—H | H—H | C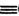 C C |
| 键能/ kJ•mol-1 | 413.4 | 436 | 812 |
(2)氯仿(CHCl3)与金属银共热可以制取乙炔,该反应的化学方程式为
(3)向压强为1.0×104 kPa的恒压密闭容器中充入1 mol乙炔和1 mol HCl气体,在催化剂作用下乙炔与HCl发生反应:HC
 CH(g)+HCl(g)
CH(g)+HCl(g) CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
CH2==CHCl(g),乙炔的平衡转化率与温度的关系如图所示。
①该反应的△H
② M点对应温度下,该反应的平衡常数Kp=
您最近一年使用:0次



