羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料。其常用的制备方法有两种:
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。
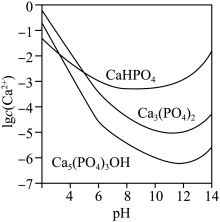
3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O=Ca5(PO4)3OH↓+________ +________
②5Ca(OH)2+3H3PO4=________________________________________________
(2)与方法A相比,方法B的优点是______________________________________ 。
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是
___________________________________________________________________________ 。
(4)图中所示3种钙盐在人体中最稳定的存在形式是______________ (填化学式)。
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因________________________________________________________ 。
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。

3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学反应方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O=Ca5(PO4)3OH↓+
②5Ca(OH)2+3H3PO4=
(2)与方法A相比,方法B的优点是
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是
(4)图中所示3种钙盐在人体中最稳定的存在形式是
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原理,分析其原因
2007·广东·高考真题 查看更多[3]
更新时间:2016-12-09 00:50:10
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】按要求完成下列填空。
(1)(溶解度与Ksp的换算)已知某温度时Ksp(CaCO3)=1×10-10,则该温度下,CaCO3的溶解度约为________ 。
(2)(平衡常数与Ksp的关系)在1.0 L Na2CO3溶液中溶解0.01 mol BaSO4,计算Na2CO3溶液的最初浓度不得低于________ mol·L-1(忽略溶液体积变化)[已知:Ksp(BaSO4)=1.1×10-10、Ksp(BaCO3)=5.1×10-9]。
(3)(Ksp与Ka的计算关系)汽车尾气中的SO2可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液的pH为9,忽略SO 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=________ (保留3位有效数字)[已知:Ka1(H2SO3)=1.54×10-2,Ka2(H2SO3)=1.02×10-7]。
(1)(溶解度与Ksp的换算)已知某温度时Ksp(CaCO3)=1×10-10,则该温度下,CaCO3的溶解度约为
(2)(平衡常数与Ksp的关系)在1.0 L Na2CO3溶液中溶解0.01 mol BaSO4,计算Na2CO3溶液的最初浓度不得低于
(3)(Ksp与Ka的计算关系)汽车尾气中的SO2可用石灰水吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液的pH为9,忽略SO
 的第二步水解,则Ksp(CaSO3)=
的第二步水解,则Ksp(CaSO3)=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】以下是某实验小组用工业硫酸铜(含硫酸亚铁等杂质)进行提纯实验,得到纯净硫酸铜晶体的流程:(已知数据:lg2=0.3;lg5=0.7)
工业CuSO4
 CuSO4溶液
CuSO4溶液 CuSO4·5H2O
CuSO4·5H2O
请回答下列问题:
(1)①步骤I的目的是除不溶性杂质。操作是_________________________ 。
②步骤Ⅱ是为了除去Fe2+,常加入氧化剂使Fe2+氧化为Fe3+,下列物质最适合的是________ 。
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________ 。
A.NaOH B.NH3·H2O C.CuO D.Cu
(2)已知常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,分别写出Cu(OH)2开始沉淀时溶液的pH=________ 并写出步骤Ⅱ调节溶液pH的合理范围______ 。
工业CuSO4

 CuSO4溶液
CuSO4溶液 CuSO4·5H2O
CuSO4·5H2O请回答下列问题:
(1)①步骤I的目的是除不溶性杂质。操作是
②步骤Ⅱ是为了除去Fe2+,常加入氧化剂使Fe2+氧化为Fe3+,下列物质最适合的是
A.KMnO4 B.H2O2 C.Cl2水 D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
A.NaOH B.NH3·H2O C.CuO D.Cu
(2)已知常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,分别写出Cu(OH)2开始沉淀时溶液的pH=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】请你利用所学的化学反应原理解决下列问题:
(1)下列溶液在空气中加热蒸干,并且灼烧之后,所得固体仍为原溶液中的溶质的是__________ 。
A.FeCl3 B.NaClO C.Fe2(SO4)3 D.K2SO3
(2)焙制糕点把NaHCO3作为发酵粉使用,往往添加少量的明矾,就是利用明矾中的Al3+与HCO3-发生双水解,写出离子方程式____________________________
(3)常温下,有0.1mol/L的盐酸,由水电离出的c(H+)=__________ ,该盐酸与0.04mol/L的Ba(OH)2等体积混合,混合后的pH值________
(4)常温下,物质的量浓度均为0.1 mol·L-1的下列溶液:
①Na2CO3溶液 ②NaOH溶液 ③CH3COONa溶液 ④NH4Cl溶液 ⑤NaNO3,溶液的pH由大到小的排列顺序是__________________
(5)实验:①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
A. 写出AgCl沉淀溶解平衡方程式______________________
B. ③中颜色变化说明Ksp(AgCl)____ Ksp(AgI)(填“>”、“<”、“=”)
(1)下列溶液在空气中加热蒸干,并且灼烧之后,所得固体仍为原溶液中的溶质的是
A.FeCl3 B.NaClO C.Fe2(SO4)3 D.K2SO3
(2)焙制糕点把NaHCO3作为发酵粉使用,往往添加少量的明矾,就是利用明矾中的Al3+与HCO3-发生双水解,写出离子方程式
(3)常温下,有0.1mol/L的盐酸,由水电离出的c(H+)=
(4)常温下,物质的量浓度均为0.1 mol·L-1的下列溶液:
①Na2CO3溶液 ②NaOH溶液 ③CH3COONa溶液 ④NH4Cl溶液 ⑤NaNO3,溶液的pH由大到小的排列顺序是
(5)实验:①0.1 mol·L-1 AgNO3溶液和0.1 mol·L-1NaCl溶液等体积混合得到浊液a,过滤得到滤液b和白色沉淀c;②向滤液b中滴加0.1 mol·L-1 KI溶液,出现浑浊;③向沉淀c中滴加0.1 mol·L-1KI溶液,沉淀变为黄色。
A. 写出AgCl沉淀溶解平衡方程式
B. ③中颜色变化说明Ksp(AgCl)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。从溶液中将Cu2+、Fe2+、Fe3+沉淀为氢氧化物所需pH分别为6.4,6.4,3.7。现有某氯化铜晶体中含有FeCl2杂质,为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图所示步骤进行提纯。
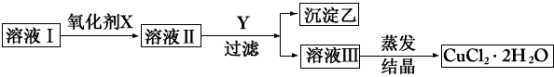
回答下列问题:
(1)最适合本实验的氧化剂是_____________ 。(填序号)
a.K2Cr2O7 b.H2O2 c.NaClO d.KMnO4
加入氧化剂对应的离子方程式为:_____________________________ 。
(2)物质Y是______________ (填名称)。
(3)本实验加碱沉淀法能不能达到目的?______________ 原因是_________________________ 。
(4)最后能否直接蒸发结晶?若不能,应如何操作?_________________ 。
(5)加氧化剂的目的是__________________________ 。
(6)除去Fe3+的有关离子方程式_______________________________ 。

回答下列问题:
(1)最适合本实验的氧化剂是
a.K2Cr2O7 b.H2O2 c.NaClO d.KMnO4
加入氧化剂对应的离子方程式为:
(2)物质Y是
(3)本实验加碱沉淀法能不能达到目的?
(4)最后能否直接蒸发结晶?若不能,应如何操作?
(5)加氧化剂的目的是
(6)除去Fe3+的有关离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】亚硝酰氯(NOC1,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水反应生成一种氯化 物和两种氮化物,可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
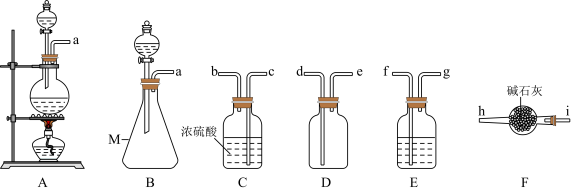
①仪器M的名称为_____ .
②制备NO发生装置可以选用____ (填写字母代号),请写出发生反应的离子方程式: ________ .
③欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a->______ (按气流方向,用小写字母表示)。
(2)乙组同学利用甲组制得的NO和Cl2制备NOC1,装置如下图所示。操作为:检验装置气密性并装入药品,打开K2,然后再打开K3通入一段时间气体Cl2,然后进行其他操作,当Z有一定量液体生成时, 停止实验。
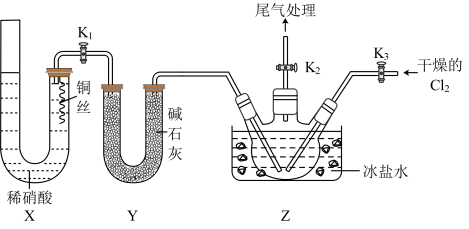
①实验室也可用X装置制备NO,相对甲组同学的气体发生装置,X装置的优点为______ .
②若无装置Y,则Z中NOC1可能发生反应的化学方程式为____ .
(3)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用 cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。滴定终点的现象是________ ;亚硝酰氯(NOC1)的质量分数为________ (用代数式表示)。
[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)= 1.56×10-10, Ksp(Ag2CrO4)=l×l012]
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:

①仪器M的名称为
②制备NO发生装置可以选用
③欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a->
(2)乙组同学利用甲组制得的NO和Cl2制备NOC1,装置如下图所示。操作为:检验装置气密性并装入药品,打开K2,然后再打开K3通入一段时间气体Cl2,然后进行其他操作,当Z有一定量液体生成时, 停止实验。

①实验室也可用X装置制备NO,相对甲组同学的气体发生装置,X装置的优点为
②若无装置Y,则Z中NOC1可能发生反应的化学方程式为
(3)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用 cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。滴定终点的现象是
[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)= 1.56×10-10, Ksp(Ag2CrO4)=l×l012]
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】重铬酸钠(Na2Cr2O7)广泛用作氧化剂、鞣革剂等。以铬矿石(主要成分为Cr2O3,还含有FeO、A12O3、SiO2等杂质)为原料制取重铬酸钠的流程如下:

请回答下列问题:
(1)Cr2O3在高温焙烧时反应的化学方程式为_____ 。
(2)生产过程中,调节(含Na2CrO4、Na2SiO3、NaAlO2的溶液)pH的目的是_______ 。
(3)某化工厂采用石墨作电极电解Na2CrO4溶液,实现了Na2CrO4转化为Na2Cr2O7的生产,其原理如下图所示。
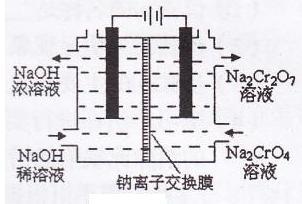
①写出阳极的电极方程式:________ ;
②此生产方法和上述流程相比的优点主要有_____ 。
(4)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要的O2的质量)。现有某水样100.00 mL,酸化后加入clmol/L的Na2Cr2O7溶液V1mL,使水中的还原性物质完全被氧化(还原产物为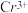 );再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为
);再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为___ mg/L。

请回答下列问题:
(1)Cr2O3在高温焙烧时反应的化学方程式为
(2)生产过程中,调节(含Na2CrO4、Na2SiO3、NaAlO2的溶液)pH的目的是
(3)某化工厂采用石墨作电极电解Na2CrO4溶液,实现了Na2CrO4转化为Na2Cr2O7的生产,其原理如下图所示。

①写出阳极的电极方程式:
②此生产方法和上述流程相比的优点主要有
(4)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要的O2的质量)。现有某水样100.00 mL,酸化后加入clmol/L的Na2Cr2O7溶液V1mL,使水中的还原性物质完全被氧化(还原产物为
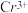 );再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为
);再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为
您最近一年使用:0次



