图1是部分短周期元素的常见化合价与原子序数的关系图:
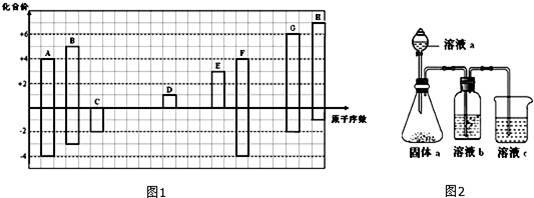
(1)元素F在周期表中的位置__________ .
(2)DH其所含化学键类型为__________ .
(3)C、D、G对应的简单离子半径大小顺序是__________ .(用离子符号回答)
(4)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:
①溶液a和溶液b分别为__________ ,__________ .
②溶液c中的离子反应方程式为__________________________________ .

(1)元素F在周期表中的位置
(2)DH其所含化学键类型为
(3)C、D、G对应的简单离子半径大小顺序是
(4)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:
①溶液a和溶液b分别为
②溶液c中的离子反应方程式为
更新时间:2016-12-09 07:11:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列十种物质:①HCl;②NaHCO3;③K2SO4溶液;④CO2;⑤蔗糖晶体;⑥Ca(OH)2;⑦氢氧化铁胶体;⑧NH3·H2O;⑨空气;⑩Al2(SO4)3
(a)上述物质中属于电解质的有_____________ ,非电解质的有_____________ (填序号)。
(b)②在水溶液中的电离方程式为____________________________________________
(c)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,如果病人同时患胃溃疡,为防胃壁穿孔,不宜服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:_____
(d)若⑦中混有少量的③,提纯的方法是:_________
A.蒸馏 B.萃取 C.渗析 D.分液
(a)上述物质中属于电解质的有
(b)②在水溶液中的电离方程式为
(c)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,如果病人同时患胃溃疡,为防胃壁穿孔,不宜服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:
(d)若⑦中混有少量的③,提纯的方法是:
A.蒸馏 B.萃取 C.渗析 D.分液
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】无机非金属材料与人类社会的发展与进步息息相关,硅元素更是无机非金属材料的主角,地壳质量的90%以上是二氧化硅和硅酸盐。回答下列问题:
(1)烧制普通玻璃的原料是纯碱、石灰石和石英砂,它们在玻璃窑中发生化学变化生成CaSiO3和Na2SiO3的化学方程式为___________ 、___________ 。
(2)工业上可利用水玻璃和盐酸反应制备硅酸凝胶后,进一步脱水处理可得到硅胶,请设计实验验证水玻璃与盐酸反应产生少量硅酸时,形成的分散系属于胶体:___________ (写出实验操作、现象和结论)。
(3)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=___________ 。
(4)高纯度单晶硅可以按下列方法制备:
SiO2 Si(粗)
Si(粗) SiHCl3
SiHCl3 高纯度单晶硅
高纯度单晶硅
①写出SiO2转化为Si(粗)的化学方程式:___________ 。
②SiHCl3被H2还原为Si(纯)的基本反应类型为___________ 。
③写出高纯度单晶硅在信息技术或新能源技术等领域的应用:___________ (任写一种)。
(5)SiO2属于___________ 氧化物,试用任一离子方程式说明___________ 。
(6)向盐酸中逐滴滴加制得的硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在5~100nm的SiO2·nH2O粒子。该分散系属于___________ (选填“溶液”“浊液”或“胶体”),可以通过___________ 来鉴别。
(7)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是___________ (填序号)。
①玻璃②石英玻璃③陶瓷④硅芯片⑤砖瓦⑥水泥⑦光导纤维
(8)0.1mol 与0.05mol
与0.05mol 在高温下充分反应,可生成标准状况下气体
在高温下充分反应,可生成标准状况下气体___________ L。
(9)我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石[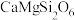 ]和橄榄石[
]和橄榄石[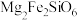 ])等,则辉石[
])等,则辉石[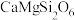 ]的氧化物形式可表示为
]的氧化物形式可表示为___________ ,斜长石[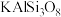 ]
]___________ (填“难”或“易”)溶于水,1mol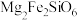 完全溶解于盐酸中消耗溶质HCl
完全溶解于盐酸中消耗溶质HCl___________ mol。
(1)烧制普通玻璃的原料是纯碱、石灰石和石英砂,它们在玻璃窑中发生化学变化生成CaSiO3和Na2SiO3的化学方程式为
(2)工业上可利用水玻璃和盐酸反应制备硅酸凝胶后,进一步脱水处理可得到硅胶,请设计实验验证水玻璃与盐酸反应产生少量硅酸时,形成的分散系属于胶体:
(3)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=
(4)高纯度单晶硅可以按下列方法制备:
SiO2
 Si(粗)
Si(粗) SiHCl3
SiHCl3 高纯度单晶硅
高纯度单晶硅①写出SiO2转化为Si(粗)的化学方程式:
②SiHCl3被H2还原为Si(纯)的基本反应类型为
③写出高纯度单晶硅在信息技术或新能源技术等领域的应用:
(5)SiO2属于
(6)向盐酸中逐滴滴加制得的硅酸钠溶液,当pH达到6~7时得到一种乳白色、半透明的分散系,其分散质为粒径在5~100nm的SiO2·nH2O粒子。该分散系属于
(7)硅酸盐材料是传统无机非金属材料,下列产品不属于硅酸盐的是
①玻璃②石英玻璃③陶瓷④硅芯片⑤砖瓦⑥水泥⑦光导纤维
(8)0.1mol
 与0.05mol
与0.05mol 在高温下充分反应,可生成标准状况下气体
在高温下充分反应,可生成标准状况下气体(9)我国成功地发射了嫦娥一号探测卫星,对月球土壤中14种元素的分布及含量进行探测。月球上的主要矿物有辉石[
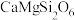 ]和橄榄石[
]和橄榄石[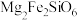 ])等,则辉石[
])等,则辉石[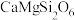 ]的氧化物形式可表示为
]的氧化物形式可表示为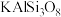 ]
]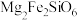 完全溶解于盐酸中消耗溶质HCl
完全溶解于盐酸中消耗溶质HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某同学在用锌与稀硫酸反应制氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率,请回答问题:
(1)上述实验中,发生反应的离子方程式是:_______________ ;________________________ 。
(2)少量硫酸铜溶液可以加快氢气的生成速率的原因是_______ 。
(3)实验室有Na2SO4、MgSO4、Ag2SO4等三种溶液,可与实验中的硫酸铜溶液起相似作用的是___________ 。
(4)为进一步研究硫酸铜的量对锌与硫酸反应生成氢气速率的影响,该同学设计了如下一系列的实验,将表中混合溶液加到6个盛有过量锌粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需要的时间:
请完成此实验设计:V2 =_________ V5=_________
(5)要加快锌与氢气的生成速率还可以采取的措施是________ (至少写两点)。
(1)上述实验中,发生反应的离子方程式是:
(2)少量硫酸铜溶液可以加快氢气的生成速率的原因是
(3)实验室有Na2SO4、MgSO4、Ag2SO4等三种溶液,可与实验中的硫酸铜溶液起相似作用的是
(4)为进一步研究硫酸铜的量对锌与硫酸反应生成氢气速率的影响,该同学设计了如下一系列的实验,将表中混合溶液加到6个盛有过量锌粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需要的时间:
| 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 40 | 40 | V1 | 40 | 40 | V2 |
| 饱和CuSO4溶液/mL | 0 | 1 | 5 | V5 | V6 | 25 |
| H2O/mL | V3 | V4 | 20 | 15 | 5 | 0 |
请完成此实验设计:V2 =
(5)要加快锌与氢气的生成速率还可以采取的措施是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,参照元素 在表中的位置,按要求回答下列问题:
在表中的位置,按要求回答下列问题:
(1)在元素 ,最活泼的金属元素是
,最活泼的金属元素是______  填元素名称
填元素名称 ;最活泼的非金属元素名称是
;最活泼的非金属元素名称是______  填元素名称
填元素名称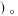
(2)用电子式表示元素 与
与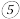 形成的原子个数比为1:2的化合物
形成的原子个数比为1:2的化合物 _______________ 。元素①和③所形成的化学键的类型是___________________ 。
(3)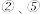 、
、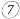 三种元素的原子半径由大到小的顺序是
三种元素的原子半径由大到小的顺序是______  用元素符号表示
用元素符号表示 。
。
(4)元素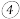 和
和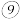 所能形成的气态氢化物的稳定性
所能形成的气态氢化物的稳定性___________  化学式表示
化学式表示 ;元素
;元素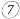 、
、 、
、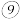 的最高价氧化物对应的水化物的酸性由强到弱的顺序
的最高价氧化物对应的水化物的酸性由强到弱的顺序 ___  化学式表示
化学式表示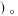
(5)写出元素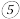 和
和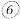 的最高价氧化物的水化物相互反应的离子方程式:
的最高价氧化物的水化物相互反应的离子方程式:______________ 。
 在表中的位置,按要求回答下列问题:
在表中的位置,按要求回答下列问题:| 周期主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ⅧA |
| 一 |  | |||||||
| 二 |  |  | 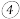 | |||||
| 三 | 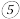 | 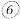 | 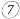 |  | 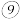 |
(1)在元素
 ,最活泼的金属元素是
,最活泼的金属元素是 填元素名称
填元素名称 ;最活泼的非金属元素名称是
;最活泼的非金属元素名称是 填元素名称
填元素名称
(2)用电子式表示元素
 与
与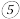 形成的原子个数比为1:2的化合物
形成的原子个数比为1:2的化合物 (3)
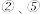 、
、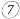 三种元素的原子半径由大到小的顺序是
三种元素的原子半径由大到小的顺序是 用元素符号表示
用元素符号表示 。
。(4)元素
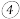 和
和 所能形成的气态氢化物的稳定性
所能形成的气态氢化物的稳定性 化学式表示
化学式表示 ;元素
;元素 、
、 、
、 的最高价氧化物对应的水化物的酸性由强到弱的顺序
的最高价氧化物对应的水化物的酸性由强到弱的顺序  化学式表示
化学式表示
(5)写出元素
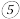 和
和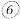 的最高价氧化物的水化物相互反应的离子方程式:
的最高价氧化物的水化物相互反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】类推法是科学学习的重要方法之一、下表提供的是VIA族元素的部分性质。请结合元素周期律完成下列问题:
(1)硒的熔点(x)范围可能是_______ 。
(2)碲的主要化合价可能有_______ 。
(3)在 、
、 、
、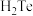 四种氢化物中,沸点最低的是
四种氢化物中,沸点最低的是_______ ,沸点最高的是_______ 。
| 元素 | 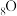 | 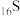 | 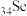 | 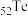 |
| 单质熔点/℃ | 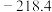 | 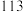 (斜方硫) (斜方硫) | x | 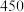 |
| 单质沸点/℃ |  |  (斜方硫) (斜方硫) | 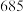 |  |
| 主要化合价 |  |  、 、 、 、 |  、 、 、 、 | |
| 原子半径 | 逐渐增大 | |||
单质与 反应的情况 反应的情况 | 点燃时易化合 | 加热化合 | 加热时难化合 | 不能直接化合 |
(2)碲的主要化合价可能有
(3)在
 、
、 、
、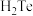 四种氢化物中,沸点最低的是
四种氢化物中,沸点最低的是
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】A、B、C、D为原子序数依次增大的四种短周期元素,A、D同主族,B、C同周期。它们中的两种元素可形成多种原子个数比为1:1的化合物,甲、乙、丙为其中的三种,它们的元素组成如下表:
通常情况下,甲为气体,密度比空气小;乙为液体;丙为固体且为离子化合物。请填写下列空白:
(1)乙的电子式为 ,丙中阴离子与阳离子的个数比为 。
(2)已知甲是同系列中最简单的化合物,且在标准状况下,5.6 L的甲完全燃烧放出的热量为325 kJ,试写出甲的燃烧热的热化学方程式 。
(3)研究表明,乙是一种二元弱酸,请写出乙在水中的电离方程式 。
(4)A、B、C、D所对应元素的原子半径大小顺序为 (用元素符号表示)。
| 化合物 | 甲 | 乙 | 丙 |
| 元素种类 | A、B | A、C | C、D |
通常情况下,甲为气体,密度比空气小;乙为液体;丙为固体且为离子化合物。请填写下列空白:
(1)乙的电子式为 ,丙中阴离子与阳离子的个数比为 。
(2)已知甲是同系列中最简单的化合物,且在标准状况下,5.6 L的甲完全燃烧放出的热量为325 kJ,试写出甲的燃烧热的热化学方程式 。
(3)研究表明,乙是一种二元弱酸,请写出乙在水中的电离方程式 。
(4)A、B、C、D所对应元素的原子半径大小顺序为 (用元素符号表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 是一种重要的化工原料。工业上可以利用硫(
是一种重要的化工原料。工业上可以利用硫( )与
)与 为原料制备
为原料制备 ,
, 受热分解成气态
受热分解成气态 ,发生反应
,发生反应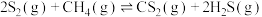 ,回答下列问题:
,回答下列问题:
(1) 的电子式为
的电子式为___________ , 分子的立体构型为
分子的立体构型为___________ 。
(2)某温度下,若 完全分解成气态
完全分解成气态 。在恒温密闭容器中,
。在恒温密闭容器中, 与
与 物质的量比为2∶1时开始反应。
物质的量比为2∶1时开始反应。
①当 的体积分数为10%时,
的体积分数为10%时, 的转化率为
的转化率为___________ 。
②当以下数值不变时,能说明该反应达到平衡的是___________ (填序号)。
a.气体密度 b.气体总压 c. 与
与 体积比 d.
体积比 d. 的体积分数
的体积分数
(3)一定条件下, 与
与 反应中
反应中 的平衡转化率、
的平衡转化率、 分解产生
分解产生 的体积分数随温度的变化曲线如图所示。据图分析,生成
的体积分数随温度的变化曲线如图所示。据图分析,生成 的反应为
的反应为___________ (填“放热”或“吸热”)反应。工业上通常采用在600~650℃的条件下进行此反应,不采用低于600℃的原因是___________ 。

(4)将 和
和 的混合气体在固态金属氧化物电解池中电解可制备
的混合气体在固态金属氧化物电解池中电解可制备 和
和 ,是一种新的能源利用方式,基本原理如下图所示。
,是一种新的能源利用方式,基本原理如下图所示。

①a电极上发生的电极反应式为: 和
和___________ 。
②a和b两电极生成的气体的物质的量之比___________ 。
 是一种重要的化工原料。工业上可以利用硫(
是一种重要的化工原料。工业上可以利用硫( )与
)与 为原料制备
为原料制备 ,
, 受热分解成气态
受热分解成气态 ,发生反应
,发生反应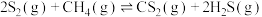 ,回答下列问题:
,回答下列问题:(1)
 的电子式为
的电子式为 分子的立体构型为
分子的立体构型为(2)某温度下,若
 完全分解成气态
完全分解成气态 。在恒温密闭容器中,
。在恒温密闭容器中, 与
与 物质的量比为2∶1时开始反应。
物质的量比为2∶1时开始反应。①当
 的体积分数为10%时,
的体积分数为10%时, 的转化率为
的转化率为②当以下数值不变时,能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.
 与
与 体积比 d.
体积比 d. 的体积分数
的体积分数(3)一定条件下,
 与
与 反应中
反应中 的平衡转化率、
的平衡转化率、 分解产生
分解产生 的体积分数随温度的变化曲线如图所示。据图分析,生成
的体积分数随温度的变化曲线如图所示。据图分析,生成 的反应为
的反应为
(4)将
 和
和 的混合气体在固态金属氧化物电解池中电解可制备
的混合气体在固态金属氧化物电解池中电解可制备 和
和 ,是一种新的能源利用方式,基本原理如下图所示。
,是一种新的能源利用方式,基本原理如下图所示。
①a电极上发生的电极反应式为:
 和
和②a和b两电极生成的气体的物质的量之比
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
(1)Fe3+价层电子的轨道表达式(电子排布图)为__ 。
(2)晶体硅属于______ 晶体。硅能形成多种化合物(如SiH4、Si2H4等),SiH4的分子的立体构型为____ ;Si2H4分子中含有的σ键和π键的数目之比为____ 。
有机物种类繁多的原因其中之一就是因为碳原子之间既可以形成单键又可以形成双键和三键,Si和Ge与C是同主族价电子数相同,但是Si和Ge就难形成双键或三键,原因是________
(3)Mg、Al、Si的第一电离能由大到小顺序:______________
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是______ 。
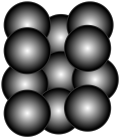
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为______ ;设Ag原子半径为rcm,阿伏加 德罗常数的值用NA表示,则Ag晶体的密度为______ g·cm-3(写出表达式)。
(1)Fe3+价层电子的轨道表达式(电子排布图)为
(2)晶体硅属于
有机物种类繁多的原因其中之一就是因为碳原子之间既可以形成单键又可以形成双键和三键,Si和Ge与C是同主族价电子数相同,但是Si和Ge就难形成双键或三键,原因是
(3)Mg、Al、Si的第一电离能由大到小顺序:
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为

您最近一年使用:0次

 和
和 结合H+能力的相对强弱
结合H+能力的相对强弱

