已知B、C为用途广泛的金属,H具有磁性氧化物,I是一种白色胶状沉淀,它们有如图所示的转化关系(部分产物未列出):

回答下列问题:
(1).E和G的化学式分别为_______ 。
(2).写出反应的化学方程式:①_______ 、③_______ 。
(3)写出反应的离子方程式②_______ 、④_______ 。

回答下列问题:
(1).E和G的化学式分别为
(2).写出反应的化学方程式:①
(3)写出反应的离子方程式②
10-11高三上·河南许昌·阶段练习 查看更多[2]
更新时间:2016-12-09 00:56:55
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】已知:常温常压下,D、E、F、I、J为气体; 1molE与含1molF的水溶液恰好反应生成B。B是一种常见的化肥。物质A—K之间有如下图所示转化关系(部分反应中生成的水已略去)。

试回答下列问题:(1)已知A中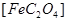 和C中Fe元素均为+2价,则
和C中Fe元素均为+2价,则 中碳元素的化合价为
中碳元素的化合价为______ 。
(2)B的化学式为________________________ 。
(3)写出反应③的化学方程式______________________________ 。
(4)写出过量单质H与K的稀溶液反应的离子方程式:__________________ 。

试回答下列问题:(1)已知A中
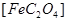 和C中Fe元素均为+2价,则
和C中Fe元素均为+2价,则 中碳元素的化合价为
中碳元素的化合价为(2)B的化学式为
(3)写出反应③的化学方程式
(4)写出过量单质H与K的稀溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有关物质的转化关系如下图所示(部分物质与条件已略去)。已知A是由两种元素组成的黑色粉末,B由两种元素组成、其摩尔质量为65g•mol-1,C是空气中含量最多的单质,D是白色粉末且焰色反应呈黄色,E是一种紫红色金属,F是一种无色气体单质,H是一种红棕色气体,I是最常见的液体,K是一种强碱。
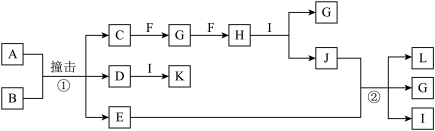
(1)B的化学式为__________________ 。
(2)K的电子式为__________________ 。
(3)写出反应①的化学方程式:_________________________________________ 。
(4)写出反应②的离子方程式:____________________________________ 。

(1)B的化学式为
(2)K的电子式为
(3)写出反应①的化学方程式:
(4)写出反应②的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。

已知:A、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是____________ ;Y中含有的化学键类型为____________ 。
(2)写出N的化学式__________ ;并任写一种N的主要用途_______________ 。
(3)写出下列反应的离子方程式:
反应①__________________ 。
反应③__________________ 。

已知:A、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是
(2)写出N的化学式
(3)写出下列反应的离子方程式:
反应①
反应③
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某工业废渣中主要含有 及少量杂质(
及少量杂质( 、
、 、
、 等),从该工业废渣中提取铜的工艺流程如图所示[已知
等),从该工业废渣中提取铜的工艺流程如图所示[已知 与足量
与足量 溶液反应生成
溶液反应生成 ,最终不会有
,最终不会有 ]:
]:
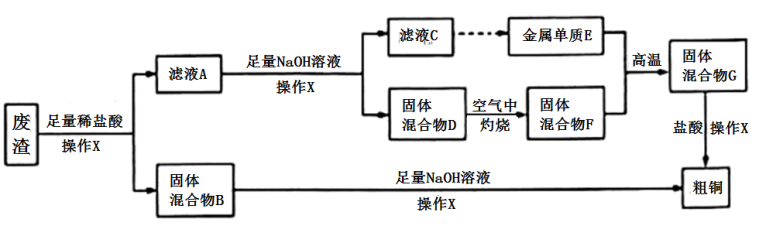
试回答下列问题。
(1)废渣中加入稀盐酸时, 发生
发生 元素自身的氧化还原反应,该反应的离子方程式为
元素自身的氧化还原反应,该反应的离子方程式为____________________________________ 。
(2)滤液 中的金属阳离子为
中的金属阳离子为 、
、 、
、___________ ,固体混合物 中含有的物质是
中含有的物质是____________ (写化学式)。
(3)操作 为常见的实验操作,其操作名称是
为常见的实验操作,其操作名称是_________________ ,在实验室,该操作中使用的玻璃仪器有________________________________________ 。
(4)金属单质 与固体混合物
与固体混合物 的反应常称为
的反应常称为________________ 反应,列举该反应的一种用途:____________________________________ 。
(5)上述方法制备的铜可用来制备铜合金,某铜合金中可能含有 、
、 中的一种,采用下列方法可测定该铜合金的组成。
中的一种,采用下列方法可测定该铜合金的组成。
实验方法:取 铜合金粉末样品放入烧杯中,将
铜合金粉末样品放入烧杯中,将 14.0%的稀硫酸(密度为
14.0%的稀硫酸(密度为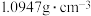 )平均分四次依次加入该烧杯中,每次均充分反应。
)平均分四次依次加入该烧杯中,每次均充分反应。
实验数据记录如下表:
①稀硫酸的物质的量浓度为_____________  。(结果保留两位小数)
。(结果保留两位小数)
②该铜合金中另一种金属是_____________ (填化学式)。
 及少量杂质(
及少量杂质( 、
、 、
、 等),从该工业废渣中提取铜的工艺流程如图所示[已知
等),从该工业废渣中提取铜的工艺流程如图所示[已知 与足量
与足量 溶液反应生成
溶液反应生成 ,最终不会有
,最终不会有 ]:
]:
试回答下列问题。
(1)废渣中加入稀盐酸时,
 发生
发生 元素自身的氧化还原反应,该反应的离子方程式为
元素自身的氧化还原反应,该反应的离子方程式为(2)滤液
 中的金属阳离子为
中的金属阳离子为 、
、 、
、 中含有的物质是
中含有的物质是(3)操作
 为常见的实验操作,其操作名称是
为常见的实验操作,其操作名称是(4)金属单质
 与固体混合物
与固体混合物 的反应常称为
的反应常称为(5)上述方法制备的铜可用来制备铜合金,某铜合金中可能含有
 、
、 中的一种,采用下列方法可测定该铜合金的组成。
中的一种,采用下列方法可测定该铜合金的组成。实验方法:取
 铜合金粉末样品放入烧杯中,将
铜合金粉末样品放入烧杯中,将 14.0%的稀硫酸(密度为
14.0%的稀硫酸(密度为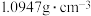 )平均分四次依次加入该烧杯中,每次均充分反应。
)平均分四次依次加入该烧杯中,每次均充分反应。实验数据记录如下表:
实验编号 |
|
|
|
|
加入稀硫酸的质量 | 14.0 | 14.0 | 14.0 | 14.0 |
剩余固体的质量 | 8.7 | 7.4 | 6.1 | 6.0 |
①稀硫酸的物质的量浓度为
 。(结果保留两位小数)
。(结果保留两位小数)②该铜合金中另一种金属是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
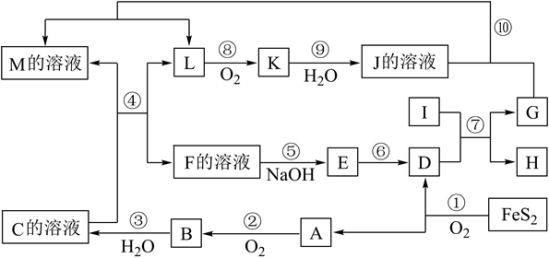
请填写下来空白:
(1)在周期表中,组成单质G的元素位于第______ 周期第________ 族。
(2)反应⑦的化学反应方程式为________________
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_______ (填写序号)
(4)反应④的离子方程式是:____________________
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:_____________________

请填写下来空白:
(1)在周期表中,组成单质G的元素位于第
(2)反应⑦的化学反应方程式为
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是
(4)反应④的离子方程式是:
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:
您最近一年使用:0次
【推荐3】铬及其化合物在生产生活中具有十分广泛的用途。工业上以铬铁矿(主要成分是Fe(CrO2)2,Cr元素为+3价。含少量MgCO3、Al2O3、SiO2等杂质)为原料制取铬酸钠(Na2CrO4)晶体,其工艺流程如图:

已知:+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO 形式存在且易被氧化。
形式存在且易被氧化。
(1)如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成__ 。
(2)若省略“过滤2”步骤,产品中可能混有__ (写化学式)。
(3)流程中两次使用了H2O2进行氧化,第二次氧化时反应的离子方程式为__ 。
(4)制取铬酸钠后的酸性废水中含有Cr2O ,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性Cr2O
,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性Cr2O 溶液形成原电池,使Cr2O
溶液形成原电池,使Cr2O 转化为Cr3+,再用石灰乳对Cr3+进行沉降。该电池的正极反应式为
转化为Cr3+,再用石灰乳对Cr3+进行沉降。该电池的正极反应式为__ ;沉降Cr3+的离子方程式为__ ,该反应的K=__ (列出计算式)。(已知Ksp[Ca(OH2)]=8×10-6,Ksp[Cr(OH)3]=6.3×10-31)
(5)产品铬酸钠可用如图所示方法冶炼铬。
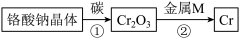
②的化学方程式为__ ,在实验室中引发该反应用到的两种药品是__ (填化学式)。

已知:+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO
 形式存在且易被氧化。
形式存在且易被氧化。(1)如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成
(2)若省略“过滤2”步骤,产品中可能混有
(3)流程中两次使用了H2O2进行氧化,第二次氧化时反应的离子方程式为
(4)制取铬酸钠后的酸性废水中含有Cr2O
 ,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性Cr2O
,必须经过处理与净化才能排放。在废水中加入焦炭和铁屑,与酸性Cr2O 溶液形成原电池,使Cr2O
溶液形成原电池,使Cr2O 转化为Cr3+,再用石灰乳对Cr3+进行沉降。该电池的正极反应式为
转化为Cr3+,再用石灰乳对Cr3+进行沉降。该电池的正极反应式为(5)产品铬酸钠可用如图所示方法冶炼铬。

②的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】有关物质的转化关系如下图所示(部分物质与条件已略去)。A是常见的金属单质, B是常见的强酸,D是常见的气体单质,E是空气中含量最多的气体,I是既能与强酸又能与强碱反应的氧化物,G是最常见的无色液体,J是一种高硬度材料(摩尔质量为41g/ mol)。

请回答下列问题:
(1)D的化学式为___________ 。
(2)F的电子式为___________ 。
(3)G的结构式为___________ 。
(4)写出反应①的离子方程式:___________ 。
(5)写出反应②的化学方程式:___________ 。

请回答下列问题:
(1)D的化学式为
(2)F的电子式为
(3)G的结构式为
(4)写出反应①的离子方程式:
(5)写出反应②的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】从某硫铁矿(主要成分为 、
、 、
、 等)中提取金属化合物的流程如下:
等)中提取金属化合物的流程如下:
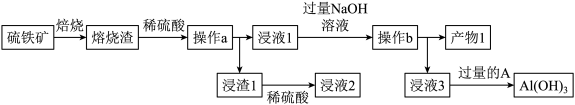
(1)为了加快焙烧速率可以采取的措施有_______ ,焙烧时 全部转化为
全部转化为 和一种具有刺激性气味的气体X,反应的化学方程式为
和一种具有刺激性气味的气体X,反应的化学方程式为_______ ,气体X在工业上可以作为制硫酸的原料。将浓硫酸滴加到蔗糖上,蔗糖变黑,体积膨胀,放出气体X,该实验体现了浓硫酸的_______ (填标号)。
A.难挥发性 B.酸性 C.强氧化性 D.脱水性
(2)操作a、b需使用到的硅酸盐制品有烧杯、_______ 、_______ ;“浸渣1”用稀硫酸浸泡洗涤可以提高金属元素的提取率,该过程所得的“浸液2”可以合并到浸液_______ (填“1”或“3”)中。
(3)“浸渣1”的主要成分为_______ (填化学式),该物质与氢氟酸(HF的水溶液)发生反应的化学方程式为_______ 。
(4)A为常见气体,则“浸液3”生成 的离子方程式为
的离子方程式为_______ 。
(5) 可以和稀硝酸反应,氧化产物为
可以和稀硝酸反应,氧化产物为 和
和 ,还原产物仅有NO,则氧化剂和还原剂的物质的量之比为
,还原产物仅有NO,则氧化剂和还原剂的物质的量之比为_______ 。
 、
、 、
、 等)中提取金属化合物的流程如下:
等)中提取金属化合物的流程如下:
(1)为了加快焙烧速率可以采取的措施有
 全部转化为
全部转化为 和一种具有刺激性气味的气体X,反应的化学方程式为
和一种具有刺激性气味的气体X,反应的化学方程式为A.难挥发性 B.酸性 C.强氧化性 D.脱水性
(2)操作a、b需使用到的硅酸盐制品有烧杯、
(3)“浸渣1”的主要成分为
(4)A为常见气体,则“浸液3”生成
 的离子方程式为
的离子方程式为(5)
 可以和稀硝酸反应,氧化产物为
可以和稀硝酸反应,氧化产物为 和
和 ,还原产物仅有NO,则氧化剂和还原剂的物质的量之比为
,还原产物仅有NO,则氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】铝元素含量居金属首位,主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。铝的单质及其化合物在生产、生活、科研等领域应用广泛。
Ⅰ、工业上用铝土矿制备铝的某种化合物的工艺流程如下:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
Fe2++□ClO-+□ ═□Fe(OH)3↓+□Cl-+□__________
②检验滤液B中是否还含有铁元素的方法为:_________________________
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为__________ (选填代号)
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、__________ (填操作名称)、过滤、洗涤。
Ⅱ、明矾(KAl(SO4)2·12H2O)在日常生活、生产中也占有一席之地。
(1)明矾曾经是净水明星,用离子方程式表示其净水原理_____________________________ 。
(2)明矾净水时,若不慎过量会有一定程度的副作用。将含有明矾的水溶液中加入Ba(OH)2溶液至铝离子恰好完全沉淀,并且过滤,就可以避免,请用离子反方程式描述其过程______________ 。
Ⅰ、工业上用铝土矿制备铝的某种化合物的工艺流程如下:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
Fe2++□ClO-+□ ═□Fe(OH)3↓+□Cl-+□
②检验滤液B中是否还含有铁元素的方法为:
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、
Ⅱ、明矾(KAl(SO4)2·12H2O)在日常生活、生产中也占有一席之地。
(1)明矾曾经是净水明星,用离子方程式表示其净水原理
(2)明矾净水时,若不慎过量会有一定程度的副作用。将含有明矾的水溶液中加入Ba(OH)2溶液至铝离子恰好完全沉淀,并且过滤,就可以避免,请用离子反方程式描述其过程
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并进行了其他有关实验(图中夹持及尾气处理装置均已略去)
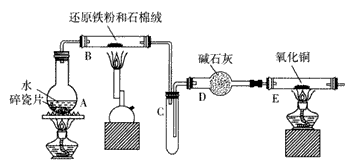
(1)装置B中发生反应的化学方程式是___________ 。
(2)装置E中的现象是___________ 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。
①欲检验溶液中含有Fe3+,选用的试剂为_____________ ,现象是_____________ 。
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释溶液中不存在Fe3+可能的原因:__________________ 。
③在此溶液中加入少量酸性高锰酸钾溶液,高锰酸钾褪色,溶液中反应的离子方程式___________ 。

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。
①欲检验溶液中含有Fe3+,选用的试剂为
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释溶液中不存在Fe3+可能的原因:
③在此溶液中加入少量酸性高锰酸钾溶液,高锰酸钾褪色,溶液中反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:
用如图所示实验装置,在硬质玻璃管B中放入还原铁粉和石棉绒的混合物,再结合一些步骤,就可以完成高温下“Fe与水蒸气的反应实验”(已知石棉绒是耐高温材料,不与水和铁反应)。

Ⅰ.探究“铁与水蒸气”能否发生反应
(1)如何检查该装置的气密性_________ 。
(2)实验中石棉绒的作用是___________________ 。
(3)反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当_________ 时(填实验现象),说明“铁与水蒸气”能够进行反应,写出铁与水蒸气反应的化学方程式______ 。
Ⅱ.探究“铁与水蒸气” 反应的产物
(4)假设还原铁粉反应完全,黑色固体为某种单一成分,为研究黑色固体成分,该研究小组甲同学提出以下假设:
假设一:黑色固体全部是Fe3O4
假设二:黑色固体全部是Fe2O3
假设三:黑色固体全部是FeO
乙同学认为即使不通过实验就可以否定甲同学的一个假设,你认为乙同学否认的假设是___________ ,理由是______________________________________ 。
(5)若假设一正确,请设计实验加以验证,完成下列表格(仪器自选)。
限选实验试剂:1 mol·L-1硫酸、2 mol·L-1NaOH溶液、新制氯水、澄清石灰水、酸性KMnO4溶液、KSCN 溶液、品红溶液
用如图所示实验装置,在硬质玻璃管B中放入还原铁粉和石棉绒的混合物,再结合一些步骤,就可以完成高温下“Fe与水蒸气的反应实验”(已知石棉绒是耐高温材料,不与水和铁反应)。

Ⅰ.探究“铁与水蒸气”能否发生反应
(1)如何检查该装置的气密性
(2)实验中石棉绒的作用是
(3)反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当
Ⅱ.探究“铁与水蒸气” 反应的产物
(4)假设还原铁粉反应完全,黑色固体为某种单一成分,为研究黑色固体成分,该研究小组甲同学提出以下假设:
假设一:黑色固体全部是Fe3O4
假设二:黑色固体全部是Fe2O3
假设三:黑色固体全部是FeO
乙同学认为即使不通过实验就可以否定甲同学的一个假设,你认为乙同学否认的假设是
(5)若假设一正确,请设计实验加以验证,完成下列表格(仪器自选)。
限选实验试剂:1 mol·L-1硫酸、2 mol·L-1NaOH溶液、新制氯水、澄清石灰水、酸性KMnO4溶液、KSCN 溶液、品红溶液
| 实验步骤 | 预期实验现象与结论 |
| 取反应后干燥的固体于试管中,加入足量的1mol·L-1硫酸溶解 | |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】置换反应的通式可表示为:

单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
(1)单质甲是生活中用途最广泛的金属,单质乙是最轻的气体,写出离子方程式:____________________ 。
(2)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,则该反应的化学方程式为____________________ 。
(3)若乙是一种红色金属单质,化合物B的溶液呈浅绿色,则该反应的离子方程式为____________________ 。
(4)工业上利用置换反应原理制备一种半导体材料,写出该反应的化学方程式____________________ 。
(5)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,则该反应的化学方程式____________________ 。
(6)若化合物B为黑色磁性晶体,,气体单质乙能在空气中燃烧,写出该反应的化学方程式____________________ 。

单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
(1)单质甲是生活中用途最广泛的金属,单质乙是最轻的气体,写出离子方程式:
(2)若化合物A常温下呈液态,化合物B的焰色反应呈黄色,则该反应的化学方程式为
(3)若乙是一种红色金属单质,化合物B的溶液呈浅绿色,则该反应的离子方程式为
(4)工业上利用置换反应原理制备一种半导体材料,写出该反应的化学方程式
(5)若单质乙是黑色非金属固体单质,化合物B是一种白色金属氧化物,则该反应的化学方程式
(6)若化合物B为黑色磁性晶体,,气体单质乙能在空气中燃烧,写出该反应的化学方程式
您最近一年使用:0次