某反应中反应物与生成物有:AsH3、H2SO4、HBrO3、K2SO4、H3AsO4、Br2和水。
(1)配平上述化学反应方程式并标出电子转移的方向和数目:
AsH3+ H2SO4+ KBrO3→K2SO4+ H3AsO4+ H2O+ Br2________________ 。
(2)反应中,被还原的元素是___________ ,还原剂是________________ 。
(3)根据上述反应可推知_________ 。
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>Br2 d.还原性:Br2>AsH3
(1)配平上述化学反应方程式并标出电子转移的方向和数目:
AsH3+ H2SO4+ KBrO3→K2SO4+ H3AsO4+ H2O+ Br2
(2)反应中,被还原的元素是
(3)根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>Br2 d.还原性:Br2>AsH3
10-11高一上·宁夏银川·期中 查看更多[1]
(已下线)2010年宁夏银川一中高一上学期期中考试化学卷
更新时间:2016-12-09 01:02:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应,式为:
C + K2Cr2O7+ H2SO4→ CO2+ Cr2(SO4)3+ K2SO4+ H2O
(1)完成并配平上述反应的化学方程式并标出电子转移方向与数目;_________
(2)此反应的氧化剂是_________ ,氧化产物是_________ ;
(3)H2SO4在上述反应中表现出来的性质是______ (填选项编号)
(4)上述反应中若产生0.1mol CO2气体,则转移电子的物质的量是______ mol。
C + K2Cr2O7+ H2SO4→ CO2+ Cr2(SO4)3+ K2SO4+ H2O
(1)完成并配平上述反应的化学方程式并标出电子转移方向与数目;
(2)此反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
(4)上述反应中若产生0.1mol CO2气体,则转移电子的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
(2)我国从2000年起逐步用 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,
,________ 是还原剂,________ 是还原产物,用单线桥法表示反应中电子得失的方向和数目:___________ 。
(3)某温度下将 通入
通入 溶液里,反应后得到
溶液里,反应后得到 、
、 、
、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为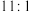 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(1)亚氯酸钠
 较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。A. 、 、 | B. 、 、 |
C. 、 、 | D. 、 、 |
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,
,(3)某温度下将
 通入
通入 溶液里,反应后得到
溶液里,反应后得到 、
、 、
、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为
的个数之比为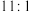 ,则
,则 与
与 反应时,被还原的氯原子和被氧化的氯原子的个数之比为
反应时,被还原的氯原子和被氧化的氯原子的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为: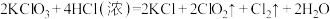 (
( 中氯元素的化合价为+4价)
中氯元素的化合价为+4价)
(1)浓盐酸在反应中表现出来的性质是_______ (填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)产生0.1 mol ,则转移电子的物质的量为
,则转移电子的物质的量为_______ mol。
(3) 具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1 g质量的物质得到的电子数)是
具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1 g质量的物质得到的电子数)是 的
的_______ 倍。
(4)亚氯酸钠( )是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
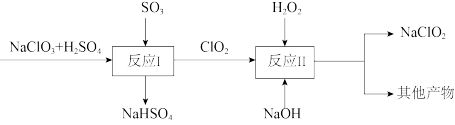
反应Ⅰ中氧化剂与还原剂的物质的量之比为_______ ;反应Ⅱ中的氧化产物是_______ 。
 和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:
和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为: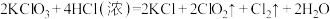 (
( 中氯元素的化合价为+4价)
中氯元素的化合价为+4价)(1)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)产生0.1 mol
 ,则转移电子的物质的量为
,则转移电子的物质的量为(3)
 具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1 g质量的物质得到的电子数)是
具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以1 g质量的物质得到的电子数)是 的
的(4)亚氯酸钠(
 )是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
反应Ⅰ中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列化学用语:
(1)画出 O2﹣结构示意图:_____ ,某种核素质量数 37,中子数 20,其原子符号:_____
(2)写出实验室制氯气的化学方程式:______________________
(3)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目__________________________________
(1)画出 O2﹣结构示意图:
(2)写出实验室制氯气的化学方程式:
(3)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:
(1)氧化剂是___________ (填写化学式);还原剂是___________ (填写化学式);氧化产物是___________ (填化学式),HCl在反应中体现的性质___________ 。氧化剂和还原剂个数比是 ___________ 。
(2)该实验室制取氯气反应的离子方程式为___________ 。
(3)用单线桥法表示电子转移的方向和数目:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O ___________
(4)请配平反应
①___________ ____H++____ +____
+____ = ____Cr3++____
= ____Cr3++____ +____H2O
+____H2O
②___________ ____Fe2++____H++____ =____Fe3++____N2O↑+____H2O
=____Fe3++____N2O↑+____H2O
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:(1)氧化剂是
(2)该实验室制取氯气反应的离子方程式为
(3)用单线桥法表示电子转移的方向和数目:KClO3+6HCl(浓)
 KCl+3Cl2↑+3H2O
KCl+3Cl2↑+3H2O (4)请配平反应
①
 +____
+____ = ____Cr3++____
= ____Cr3++____ +____H2O
+____H2O②
 =____Fe3++____N2O↑+____H2O
=____Fe3++____N2O↑+____H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】为测试铁片中铁元素的含量,某课外活动小组提出下面方案并进行了实验。将0.200g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.0200mol•L-1的KMnO4溶液滴定,达到终点时消耗了25.00mLKMnO4溶液。
(1)配平以下方程式并标出电子转移的方同与数目:___ 。
H2SO4+KMnO4+FeSO4→MnSO4+Fe2(SO4)3+K2SO4+H2O
(2)铁片中铁元素的质量分数为___ ;若通过仪器分析发现该小组的测量结果偏高,以下可能的情况有___ 。
A.酸式滴定管洗净后,直接注入高锰酸钾溶液
B.洗净的锥形瓶,再用待测液润洗
C.锥形瓶中残留有少量蒸馏水
D.滴定至终点时,在滴定管尖嘴部位有气泡
(3)高锰酸钾溶液往往用硫酸酸化而不用盐酸酸化,原因是:___ 。
(4)Fe2(SO4)3溶液中c(Fe3+):c(SO )
)___ 2:3(填写“>”、“<”或“=”),用离子方程式解释:___ 。
(5)高锰酸钾在化学品生产中,广泛用作为氧化剂,可以氧化H2O2、Fe2+、S2-、SO 等多种物质。如H2O2+KMnO4+H2SO4→MnSO4+ +K2SO4+H2O,试推测空格上应填物质的化学式为
等多种物质。如H2O2+KMnO4+H2SO4→MnSO4+ +K2SO4+H2O,试推测空格上应填物质的化学式为___ 。
(6)上述反应在恒温下进行,该过程中会明显看到先慢后快的反应,原因可能是___ 。
(1)配平以下方程式并标出电子转移的方同与数目:
H2SO4+KMnO4+FeSO4→MnSO4+Fe2(SO4)3+K2SO4+H2O
(2)铁片中铁元素的质量分数为
A.酸式滴定管洗净后,直接注入高锰酸钾溶液
B.洗净的锥形瓶,再用待测液润洗
C.锥形瓶中残留有少量蒸馏水
D.滴定至终点时,在滴定管尖嘴部位有气泡
(3)高锰酸钾溶液往往用硫酸酸化而不用盐酸酸化,原因是:
(4)Fe2(SO4)3溶液中c(Fe3+):c(SO
 )
)(5)高锰酸钾在化学品生产中,广泛用作为氧化剂,可以氧化H2O2、Fe2+、S2-、SO
 等多种物质。如H2O2+KMnO4+H2SO4→MnSO4+ +K2SO4+H2O,试推测空格上应填物质的化学式为
等多种物质。如H2O2+KMnO4+H2SO4→MnSO4+ +K2SO4+H2O,试推测空格上应填物质的化学式为(6)上述反应在恒温下进行,该过程中会明显看到先慢后快的反应,原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】亚硝酸钠(NaNO2)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究NaNO2的性质。
(1)NaNO2中N元素的化合价是___________ ,根据化合价,推测其具有氧化性和还原性。
(2)化学兴趣小组为了验证推测的结果,设计实验操作如下表所示,请完善表格中的实验现象和结论(已知I2遇淀粉变蓝)。
(3)通过上述实验可知,NaNO2、KMnO4、I2的氧化性由强到弱的顺序为___________ 。
(1)NaNO2中N元素的化合价是
(2)化学兴趣小组为了验证推测的结果,设计实验操作如下表所示,请完善表格中的实验现象和结论(已知I2遇淀粉变蓝)。
| 实验 | 实验操作及现象 | 结论 |
| ① | 取5mLNaNO2溶液于试管中,加入少量KI溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 | NaNO2具有 |
| ② | 取2mLKMnO4溶液(先酸化好)于试管中,滴加足量的NaNO2溶液,可观察到的实验现象为 | NaNO2具有还原性 |
| ③ | NaNO2固体与70%硫酸反应生成了NO和NO2两种气体 | NaNO2具有 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与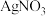 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的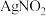 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一:_______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一:_______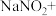 _______KI+_______=_______NO↑+_______
_______KI+_______=_______NO↑+_______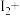 _______
_______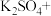 _______
_______ _______
_______
(1)请完成该化学方程式并配平_______ 。
(2)从物质分类角度来看, 是
是_______ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理 并不是最佳方法,从环保角度来讲,要将
并不是最佳方法,从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的_______ (填“氧化性”或“还原性”应该比KI更_______ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是_______(填序号)
和NaCl的是_______(填序号)
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列_______(填序号)反应中
表现出的性质与下列_______(填序号)反应中 表现出的性质相同。
表现出的性质相同。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:_______ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒,亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与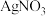 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的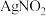 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一:_______
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一:_______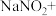 _______KI+_______=_______NO↑+_______
_______KI+_______=_______NO↑+_______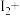 _______
_______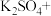 _______
_______ _______
_______
(1)请完成该化学方程式并配平
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理
 并不是最佳方法,从环保角度来讲,要将
并不是最佳方法,从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是_______(填序号)
和NaCl的是_______(填序号)| A.分别溶于水并滴加几滴酚酞溶液 |
B.分别溶于水并滴加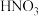 酸化的 酸化的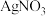 溶液 溶液 |
| C.分别加强热并收集气体检验 |
| D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列_______(填序号)反应中
表现出的性质与下列_______(填序号)反应中 表现出的性质相同。
表现出的性质相同。A.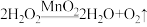 |
B. |
C.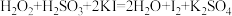 |
D.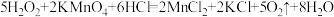 |
您最近一年使用:0次
【推荐3】碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛。完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。写出该反应的化学方程式_____ 。
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是__________________________________ 。
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2 + Hg=Cu2HgI4(玫瑰红)+ 2Cu,产物Cu2HgI4中Cu元素显____ 价。当有1 molCu2I2参与反应时,转移电子____ mol。
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是_____ (选填编号)
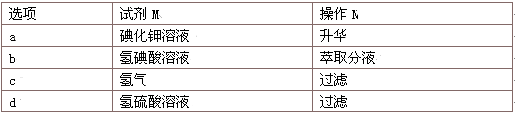
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。写出该反应的化学方程式
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2 + Hg=Cu2HgI4(玫瑰红)+ 2Cu,产物Cu2HgI4中Cu元素显
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O===Se+2 SO42-+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是__________ ,还原剂是___________ ,反应中被还原的元素是________ 。当有标准状况下22.4 L SO2气体生成时,转移电子的物质的量是________ mol。
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是______________________________________________________________________ 。
(3)用双线桥法标出反应②电子转移的方向和数目:_____________________________________ 。
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O
配平上述反应的化学方程式。________________________ 。
已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O===Se+2 SO42-+4H+。
(1)Se与浓H2SO4的反应中,氧化剂是
(2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是
(3)用双线桥法标出反应②电子转移的方向和数目:
(4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O
配平上述反应的化学方程式。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】SCR和NSR技术可有效降低柴油发动机在空气过量时 的排放。
的排放。
(1)SCR(选择性催化还原)工作原理如图所示:
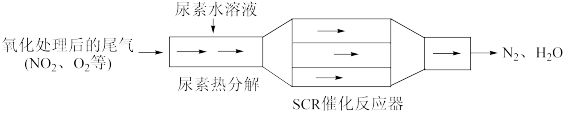
①尿素 水溶液热分解为
水溶液热分解为 和
和 。
。
②反应器中 还原
还原 的化学方程式
的化学方程式_________________________ 。
(2)NSR( 储存还原)工作原理:
储存还原)工作原理: 的储存和还原在不同时段交替进行,如图1所示。
的储存和还原在不同时段交替进行,如图1所示。
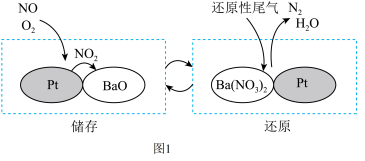
①通过BaO和 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是__________ 。
②用 模拟尾气中还原性气体研究了
模拟尾气中还原性气体研究了 的催化还原过程,该过程分两步进行,如图2表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的
的催化还原过程,该过程分两步进行,如图2表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 与
与 的物质的量之比是
的物质的量之比是__________ 。

③还原过程中,有时会产生笑气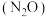 。笑气为直线形不对称分子,与
。笑气为直线形不对称分子,与 具有相似的化学键特征,则笑气的结构式为
具有相似的化学键特征,则笑气的结构式为__________ 。研究发现还原过程中笑气的产生与NO有关,在有氧条件下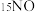 与
与 以一定比例反应时,得到的笑气几乎都是
以一定比例反应时,得到的笑气几乎都是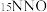 。
。
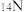 与
与 互为
互为____________________ (填“同位素”或“同素异形体”)。
请将该反应的化学方程式补充完整:__________ 。
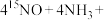 ____
____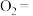 ________
________
 的排放。
的排放。(1)SCR(选择性催化还原)工作原理如图所示:

①尿素
 水溶液热分解为
水溶液热分解为 和
和 。
。②反应器中
 还原
还原 的化学方程式
的化学方程式(2)NSR(
 储存还原)工作原理:
储存还原)工作原理: 的储存和还原在不同时段交替进行,如图1所示。
的储存和还原在不同时段交替进行,如图1所示。
①通过BaO和
 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是②用
 模拟尾气中还原性气体研究了
模拟尾气中还原性气体研究了 的催化还原过程,该过程分两步进行,如图2表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的
的催化还原过程,该过程分两步进行,如图2表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的 与
与 的物质的量之比是
的物质的量之比是
③还原过程中,有时会产生笑气
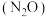 。笑气为直线形不对称分子,与
。笑气为直线形不对称分子,与 具有相似的化学键特征,则笑气的结构式为
具有相似的化学键特征,则笑气的结构式为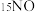 与
与 以一定比例反应时,得到的笑气几乎都是
以一定比例反应时,得到的笑气几乎都是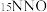 。
。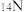 与
与 互为
互为请将该反应的化学方程式补充完整:
 ____
____ ________
________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列有关氧化还原的问题。
(1)下列微粒:①S② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ 。在化学反应中只能被氧化的是
。在化学反应中只能被氧化的是______ (填序号,下同),只能表现出氧化性的是______ 。
(2)将 溶液滴加到酸性
溶液滴加到酸性 溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是
溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是______ ,这样推测的理由是______ 。
(3)自来水中的 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出两种方案:
的浓度,某研究人员提出两种方案:
①方案a:碱性条件下用 还原
还原 ,产物为
,产物为 。生成1个
。生成1个 分子的同时会生成
分子的同时会生成______ 个 。
。
②方案b:碱性条件下用 粉还原
粉还原 ,产物是
,产物是 发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目
发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目______ 。

(4)设计实验验证亚硫酸钠具有还原性。
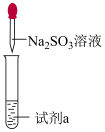
试剂a:______ 现象:______ 。
(5)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
 。试通过计算和推理完成下面的问题:
。试通过计算和推理完成下面的问题:
①A物质可以导致酸雨的形成。A应该属于______ (用字母代号填写)。
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
② 物质可以使酸性
物质可以使酸性 溶液褪色,写出反应的离子方程式
溶液褪色,写出反应的离子方程式______ 。此反应中每个 分子
分子______ (填“得到”或“失去”)______ 个电子,发生______ 反应(填“氧化反应”或“还原反应”)。
(1)下列微粒:①S②
 ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ 。在化学反应中只能被氧化的是
。在化学反应中只能被氧化的是(2)将
 溶液滴加到酸性
溶液滴加到酸性 溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是
溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是(3)自来水中的
 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出两种方案:
的浓度,某研究人员提出两种方案:①方案a:碱性条件下用
 还原
还原 ,产物为
,产物为 。生成1个
。生成1个 分子的同时会生成
分子的同时会生成 。
。②方案b:碱性条件下用
 粉还原
粉还原 ,产物是
,产物是 发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目
发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目
(4)设计实验验证亚硫酸钠具有还原性。

试剂a:
(5)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
 。试通过计算和推理完成下面的问题:
。试通过计算和推理完成下面的问题:①A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
②
 物质可以使酸性
物质可以使酸性 溶液褪色,写出反应的离子方程式
溶液褪色,写出反应的离子方程式 分子
分子
您最近一年使用:0次



