有X、Y、Z、W、M、N六种短周期元素,其中X、Y、Z、W同周期,Z与M、N与Y分别同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。
(1)元素X与 M形成X2M2型化合物中阴阳离子个数比为:____________
(2)YM2晶体属于___________ 晶体(填晶体类型);30g YM2晶体中含_________ 条共价键(阿伏加德罗常数用NA表示)
(3)在工业上常用电解饱和XW的溶液来制碱。若用阴极室产生的气体为碱性燃料电池的燃料,则燃料电池中该气体所在电极为_______ 极,电极反应式为: _______ 。
(4)已知单质A为常见黑色固体粉末,B是元素Z的最高价含氧酸,其存在如图所示的转换关系:
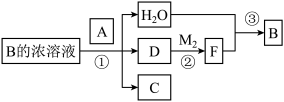
(Ⅰ) 若向C中滴加KSCN溶液立即呈血红色。则:常温下A在B的浓溶液中难以溶解的原因是_____ ;因此反应①的的条件是______ 。在工业上反应③是在__________ (填设备)中进行的;在实验室用________ (填药品名)检验D的存在;含D的尾气直接排放到大气中造成环境污染的后果是_______ ;
(Ⅱ) 按要求写方程式:
写出反应②的化学方程式_____________________________________ ,
写出C与小苏打溶液反应的离子方程式__________________________ ,
(Ⅲ) 若A是元素N的单质写出反应①的化学方程式:_________________ 。
(1)元素X与 M形成X2M2型化合物中阴阳离子个数比为:
(2)YM2晶体属于
(3)在工业上常用电解饱和XW的溶液来制碱。若用阴极室产生的气体为碱性燃料电池的燃料,则燃料电池中该气体所在电极为
(4)已知单质A为常见黑色固体粉末,B是元素Z的最高价含氧酸,其存在如图所示的转换关系:

(Ⅰ) 若向C中滴加KSCN溶液立即呈血红色。则:常温下A在B的浓溶液中难以溶解的原因是
(Ⅱ) 按要求写方程式:
写出反应②的化学方程式
写出C与小苏打溶液反应的离子方程式
(Ⅲ) 若A是元素N的单质写出反应①的化学方程式:
10-11高三上·重庆·期中 查看更多[1]
(已下线)2011届重庆市西南师大附中高三上学期期中考试(理综)化学部分
更新时间:2016-12-09 01:20:33
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为铜丝与浓硫酸反应并验证其产物性质的实验装置:
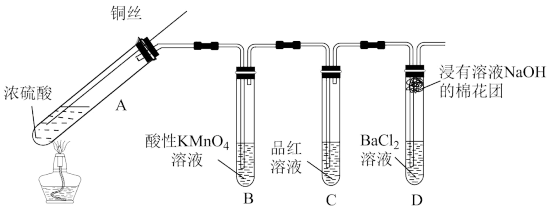
(1)试管A中反应的化学方程式是_______ 。
(2)加热一段时间后,试管B中溶液褪色,说明SO2具有_______ 性。若要立即终止铜与浓硫酸的反应,恰当的方法是_______ 。
A.撤去酒精灯 B.上移铜丝,使其脱离浓硫酸 C.拔掉橡胶塞倒出浓硫酸
(3)试管C中品红溶液褪色,体现了SO2具有_______ 的性质,试管C可以探究SO2与品红作用的可逆性,请写出实验操作及现象_______ 。
(4)装置D中NaOH溶液的作用是_______ ,反应停止后,试管D中溶液依然澄清,待装置冷却,把D取下后将其中溶液分成两份做如下实验:

(1)试管A中反应的化学方程式是
(2)加热一段时间后,试管B中溶液褪色,说明SO2具有
A.撤去酒精灯 B.上移铜丝,使其脱离浓硫酸 C.拔掉橡胶塞倒出浓硫酸
(3)试管C中品红溶液褪色,体现了SO2具有
(4)装置D中NaOH溶液的作用是
| 加入试剂 | 现象 | 结论 | |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | 沉淀为 |
| 第二份 | 加入H2O2溶液 | 有白色沉淀生成 | 沉淀为 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
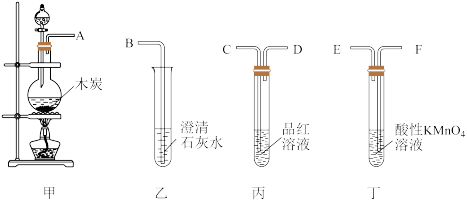
【推荐2】某小组同学设计下图装置验证木炭可被浓硫酸氧化成 。
。
回答下列问题:
(1)甲中碳与浓硫酸共热时反应的化学方程式为_______ 。
(2)如按气流由左向右流向,连接上述装置的正确顺序是A→_____→_______→_______→_______→B(填各接口字母)。_______
(3)丁中酸性高锰酸钾溶液的作用是_______ 。
(4)仪器乙、丙应有怎样的实验现象才表明已检验出CO2:乙中_______ ;丙中_______
(5)木炭能与浓硫酸反应,而不能与稀硫酸反应,是因为浓硫酸具有_______ 性。
(6)该小组同学设计如下方法鉴别浓硫酸与稀硫酸:
 。
。
回答下列问题:
(1)甲中碳与浓硫酸共热时反应的化学方程式为
(2)如按气流由左向右流向,连接上述装置的正确顺序是A→_____→_______→_______→_______→B(填各接口字母)。
(3)丁中酸性高锰酸钾溶液的作用是
(4)仪器乙、丙应有怎样的实验现象才表明已检验出CO2:乙中
(5)木炭能与浓硫酸反应,而不能与稀硫酸反应,是因为浓硫酸具有
(6)该小组同学设计如下方法鉴别浓硫酸与稀硫酸:
| 组别 | 操作 | 结论 |
| a | 分别滴在白纸上 | 纸变 |
| b | 分别滴在铁片上 | 产生气泡的是 |
| c | 分别滴在胆矾晶体中 | 晶体变 |
| d | 分别加入到水中 | 剧烈放热的是 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学根据铜与浓硫酸反应能生成 ,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
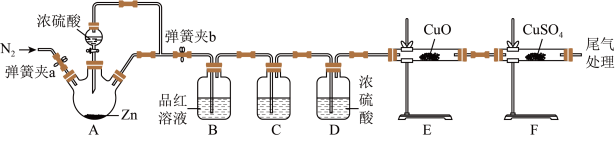
回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式___________ 。
(2)该同学预测锌与浓硫酸反应生成的混合气体的成分可能为___________ (用化学式表示)。
(3)C装置所盛常见试剂可以是___________ (填一种)。
(4)为了验证 是酸性氧化物,B中可选用的试剂是___________。
是酸性氧化物,B中可选用的试剂是___________。
(5)为测定空气中 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的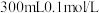 的酸性高锰酸钾溶液。若管道中空气流量为
的酸性高锰酸钾溶液。若管道中空气流量为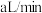 ,经过
,经过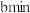 溶液恰好褪色,假定样品中的
溶液恰好褪色,假定样品中的 可以被溶液完全吸收,则该样品中的
可以被溶液完全吸收,则该样品中的 含量是
含量是___________  。
。
 ,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
,预测锌与浓硫酸反应生成的产物可能为混合气体(水蒸气除外),设计如下装置进行验证(加热和部分夹持装置略):
回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式
(2)该同学预测锌与浓硫酸反应生成的混合气体的成分可能为
(3)C装置所盛常见试剂可以是
(4)为了验证
 是酸性氧化物,B中可选用的试剂是___________。
是酸性氧化物,B中可选用的试剂是___________。| A.无色酚酞溶液 | B.紫色石蕊试液 | C.红色品红溶液 | D. 淀粉混合溶液 淀粉混合溶液 |
 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的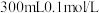 的酸性高锰酸钾溶液。若管道中空气流量为
的酸性高锰酸钾溶液。若管道中空气流量为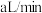 ,经过
,经过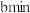 溶液恰好褪色,假定样品中的
溶液恰好褪色,假定样品中的 可以被溶液完全吸收,则该样品中的
可以被溶液完全吸收,则该样品中的 含量是
含量是 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】H2作为重要的化工原料及清洁能源,一直备受关注。请回答下列问题:
I.利用H2人工固氮,其反应原理为N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)下表为部分化学键的键能(键能:断开1 mol化学键所需的热量):
每有1 mol N2参与人工固氮,会_______ (填“吸收”或“放出”)的能量为_______ kJ。
(2)一定温度下,向体积为1 L的刚性密闭容器中充入0.1 mol N2和0.3 mol H2,发生反应:N2(g)+3H2(g) 2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:
2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:

①0~2min内,用NH3表示该反应的速率为___________ mol·L-1·min-1。
②N2的转化率为___________ 。
③能说明上述反应已达到平衡状态的是___________ (填选项字母)。
a.容器内N2、H2的浓度之比为1:3
b.3v(N2)=v(H2)
c.混合气体的密度保持不变
d.容器中气体的平均相对分子质量不随时间而变化
II.氢能源的利用。氢氧燃料碱性电池工作原理如图。
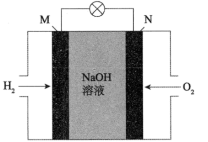
①M极为___________ (填“正极”或“负极”)。
②N极上发生反应的电极反应式为______________ 。
③电池工作时,当外电路中流过0.2 mol电子时,消耗氧气在标准状况下的体积为_____ L。
I.利用H2人工固氮,其反应原理为N2(g)+3H2(g)
 2NH3(g)。
2NH3(g)。(1)下表为部分化学键的键能(键能:断开1 mol化学键所需的热量):
| 化学键 |  | H-H | N-H |
键能/(kJ mol-1) mol-1) | 946 | 436 | 391 |
每有1 mol N2参与人工固氮,会
(2)一定温度下,向体积为1 L的刚性密闭容器中充入0.1 mol N2和0.3 mol H2,发生反应:N2(g)+3H2(g)
 2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:
2NH3(g)。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化关系如图所示:
①0~2min内,用NH3表示该反应的速率为
②N2的转化率为
③能说明上述反应已达到平衡状态的是
a.容器内N2、H2的浓度之比为1:3
b.3v(N2)=v(H2)
c.混合气体的密度保持不变
d.容器中气体的平均相对分子质量不随时间而变化
II.氢能源的利用。氢氧燃料碱性电池工作原理如图。

①M极为
②N极上发生反应的电极反应式为
③电池工作时,当外电路中流过0.2 mol电子时,消耗氧气在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g) △H<0。
①该反应中,反应物总能量_____ (填“>”、“<”或“=”)生成物总能量。
②当该反应有2mol N2(g)生成时,转移电子的物质的量为______ mol。
(2)也可以利用甲烷催化还原氮氧化物.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是______________ 。
(3)还可利用ClO2消除氮氧化物的污染,反应过程如下(部分反应物或生成物略去):
NO NO2
NO2 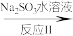 N2
N2
反应I的产物中还有两种强酸生成,且其中一种强酸为硝酸,且硝酸与NO2物质的量相等,则化学反应方程式为_____ ,反应中若生成22.4L N2(标准状况),则消耗ClO2_____ g。
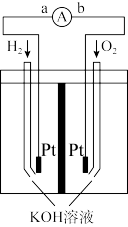
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。
①氢氧燃料电池的能量转化主要形式是_______ ,工作时电流方向为____ (用a、b和箭头表示)。
②负极的电极反应式为________________ 。
③电极表面镀铂粉的原因为____________ 。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g) △H<0。
①该反应中,反应物总能量
②当该反应有2mol N2(g)生成时,转移电子的物质的量为
(2)也可以利用甲烷催化还原氮氧化物.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是
(3)还可利用ClO2消除氮氧化物的污染,反应过程如下(部分反应物或生成物略去):
NO
 NO2
NO2  N2
N2反应I的产物中还有两种强酸生成,且其中一种强酸为硝酸,且硝酸与NO2物质的量相等,则化学反应方程式为
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。
①氢氧燃料电池的能量转化主要形式是
②负极的电极反应式为
③电极表面镀铂粉的原因为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】我国能够造出几百万一颗的卫星芯片,但是在智能手机芯片上却屡屡遭到美国垄断。制造手机芯片需要高纯硅,工业上制取高纯硅的流程如图。请根据所学知识回答下列问题。
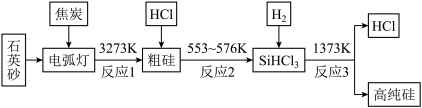
(1)石英砂的主要成分为____________ (填化学式),实验室不能用石英坩埚熔融氢氧化钠的原因是________________________ 。
(2)整个过程中可以循环利用的物质为____________ (填化学式)。
(3)晶体硅为灰黑色固体,溶于氢氟酸可生成氢气。写出晶体硅与氢氟酸反应的化学方程式:__________________ 。
(4)某科研团队设计了一种以硅作为基底的微型直接氢气酸性燃料电池,其工作原理如图所示:
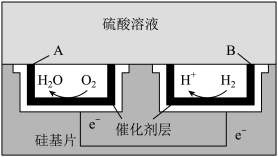
①电池工作时,电子由______ (填“A”或“B”,下同)电极流向______ 电极。
②电池工作时,B电极上的电极反应式为__________________ 。
③每转移 ,A电极消耗标准状况下的
,A电极消耗标准状况下的 的体积为
的体积为______ L。

(1)石英砂的主要成分为
(2)整个过程中可以循环利用的物质为
(3)晶体硅为灰黑色固体,溶于氢氟酸可生成氢气。写出晶体硅与氢氟酸反应的化学方程式:
(4)某科研团队设计了一种以硅作为基底的微型直接氢气酸性燃料电池,其工作原理如图所示:

①电池工作时,电子由
②电池工作时,B电极上的电极反应式为
③每转移
 ,A电极消耗标准状况下的
,A电极消耗标准状况下的 的体积为
的体积为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大。元素A、B、C、D、E的原子结构等信息如下:
请回答下列问题:(用A、B、C、D、E,所对应的元素符号作答)
(1)D位于周期表中_______ 区,E的核外电子排布式是_____________________ 。
(2)B、C、D第一电离能由大到小为__________________ 。
(3)A和C形成的常见分子中,中心原子的杂化方式为_________ 。
(4)1molABC分子中含有σ键数目为_________ 。
(5)与化合物BD互为等电子体的阴离子化学式为_________ 。
(6)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是__________________ 。
| 元素 | 元素性质或原子结构 |
| A | 周期表中原子半径最小的元素 |
| B | 原子核外有三种不同的能级且各个能级所填充的电子数相同 |
| C | 最外层p轨道半充满 |
| D | 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 |
| E | 位于ds区且原子的最外层电子数为偶数 |
请回答下列问题:(用A、B、C、D、E,所对应的元素符号作答)
(1)D位于周期表中
(2)B、C、D第一电离能由大到小为
(3)A和C形成的常见分子中,中心原子的杂化方式为
(4)1molABC分子中含有σ键数目为
(5)与化合物BD互为等电子体的阴离子化学式为
(6)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】短周期主族元素X、Y、Z、W、R原子序数依次增大,W原子次外层电子数比最外层电子数多2个,X与R同主族,其中部分元素的原子半径和主要化合价如下表所示:
请回答下列问题:
(1)W原子的价电子排布图为___________ 。
(2)Y元素最高价氧化物水化物的溶液与Z的最高价氧化物反应的离子方程为___________ 。
(3)W、R元素的最高价氧化物水化物的酸性较强的为___________ (填化学式),请从结构的角度解释其原因___________ 。
(4)在一定条件下,WR2与NH3反应生成W8、W4N4和一种仅由非金属元素组成的离子化合物,该离子化合物的电子式为___________ 。
| X | Y | Z | |
| 原子半径/pm | 71 | 186 | 143 |
| 主要化合价 | -1 | +1 | +3 |
(1)W原子的价电子排布图为
(2)Y元素最高价氧化物水化物的溶液与Z的最高价氧化物反应的离子方程为
(3)W、R元素的最高价氧化物水化物的酸性较强的为
(4)在一定条件下,WR2与NH3反应生成W8、W4N4和一种仅由非金属元素组成的离子化合物,该离子化合物的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。针对表中①-⑧号元素回答下列问题。
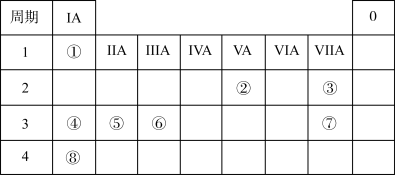
(1)②③元素中最高化合价更高的是___________ 。
(2)短周期元素中最高价氧化物对应水化物的酸性最强的是___________ 。
(3)下列事实不能证明④的金属性比⑤强的是___________(填序号)。
(4)请写出元素④、⑥最高价氧化物对应水化物相互反应的离子方程式___________ 。
(5)元素①和⑧的单质化合形成的化合物KH中H元素的化合价为___________ ;KH能与水反应生成一种气体,在反应后的溶液中滴入酚酞,溶液变红,反应的化学方程式为___________ 。

(1)②③元素中最高化合价更高的是
(2)短周期元素中最高价氧化物对应水化物的酸性最强的是
(3)下列事实不能证明④的金属性比⑤强的是___________(填序号)。
| A.④单质的密度小于⑤单质的密度 |
| B.④的单质能与冷水剧烈反应而⑤的单质不能 |
| C.④的最高价氧化物对应水化物的碱性比⑤强 |
| D.④的化合价小于⑤ |
(4)请写出元素④、⑥最高价氧化物对应水化物相互反应的离子方程式
(5)元素①和⑧的单质化合形成的化合物KH中H元素的化合价为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】TiCl4是一种重要的化工原料,其工业生产过程如下:
2FeTiO3(s) + 7Cl2(g) + 6C (s)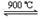 2TiCl4(g)+ 2FeCl3(g) + 6CO(g) – Q (Q>0)
2TiCl4(g)+ 2FeCl3(g) + 6CO(g) – Q (Q>0)
回答下列问题:
1.该反应达到平衡后,若使正反应速率增大可采取的方法有_________ 。(选填编号)
a.加压 b.加入碳 c.升温 d.及时移走CO
2.若上述反应在固定体积的密闭容器中发生,一定能说明反应已达平衡的是_______ 。(选填编号)
a. 反应物不再转化为生成物
b. 炉内FeTiO3与TiCl4的质量比保持不变
c. 反应的热效应不再改变
d. 单位时间内,n(FeTiO3)消耗:n(FeCl3)生成=1:1
3.上述反应中所有非金属元素原子的半径从大到小的顺序为_____________ ;其中不属于同周期又不属于相邻族的两元素形成_____ 分子(填“极性”或“非极性”),通过比较____________ 可以判断这两种元素的非金属性。
4.上述反应中,非金属性最弱的元素原子的电子共占据_______ 个原子轨道,最外层电子排布式为____________ 。它形成的固态单质中只含一种强烈的相互作用力,则该单质属于______ 晶体。
5.为方便获得氯气,工业制TiCl4厂可以和氯碱厂进行联合生产。CO可合成甲醇,若不考虑损失,上述联合生产在充分利用各种副产品的前提下,合成192 kg甲醇,至少需补充H2_______ mol。
2FeTiO3(s) + 7Cl2(g) + 6C (s)
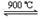 2TiCl4(g)+ 2FeCl3(g) + 6CO(g) – Q (Q>0)
2TiCl4(g)+ 2FeCl3(g) + 6CO(g) – Q (Q>0)回答下列问题:
1.该反应达到平衡后,若使正反应速率增大可采取的方法有
a.加压 b.加入碳 c.升温 d.及时移走CO
2.若上述反应在固定体积的密闭容器中发生,一定能说明反应已达平衡的是
a. 反应物不再转化为生成物
b. 炉内FeTiO3与TiCl4的质量比保持不变
c. 反应的热效应不再改变
d. 单位时间内,n(FeTiO3)消耗:n(FeCl3)生成=1:1
3.上述反应中所有非金属元素原子的半径从大到小的顺序为
4.上述反应中,非金属性最弱的元素原子的电子共占据
5.为方便获得氯气,工业制TiCl4厂可以和氯碱厂进行联合生产。CO可合成甲醇,若不考虑损失,上述联合生产在充分利用各种副产品的前提下,合成192 kg甲醇,至少需补充H2
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出R原子核外能量最高的电子的电子排布式:___________ 。
②常温下,不能与R单质发生反应的是___________ (选填序号)。
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高,不溶于水。可由下列反应制得:SiO2+C+N2 Si3N4+CO
Si3N4+CO
①C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:___________ 。
②配平上述反应的化学方程式:___________ 。
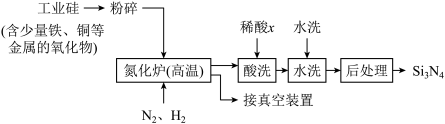
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:
适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。x可能是___________ (选填:“盐酸”“硝酸”或“硫酸”),理由是___________ 。
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出R原子核外能量最高的电子的电子排布式:
②常温下,不能与R单质发生反应的是
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高,不溶于水。可由下列反应制得:SiO2+C+N2
 Si3N4+CO
Si3N4+CO①C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:
②配平上述反应的化学方程式:
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:

适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。x可能是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z为三种元素,X能与氢形成气态XH4,其中X的质量分数为75%;且X与Y能形成XY2型化合物。Y的原子核内质子数和中子数相等,在Y的氢化物中,Y的质量分数为88.9%。Z的最高价氧化物的水化物是酸性最强的酸。
(1)X的单质叫做______ ,它属于______ 晶体。
(2)Y的氢化物属于______ 晶体,它的电子式是______ 。
(3)Z元素位于周期表的第______ 周期______ 族,它的氢化物是______ 性分子。
(4)X与Z形成的化合物可用电子式表示为______ ,其分子的空间构型是______ 体,属于______ 性分子,它的晶体属于______ 晶体。
(1)X的单质叫做
(2)Y的氢化物属于
(3)Z元素位于周期表的第
(4)X与Z形成的化合物可用电子式表示为
您最近一年使用:0次



