现有A、B、C、D、E五种元素,原子序数依次增大,且不超过36.A元素的基态原子最外层电子数是次外层的三倍;B元素的基态原子核外有13种不同运动状态的电子;C与B同一周期,原子中未成对电子数是同周期中最多的;D2-的核外电子排布与氩原子相同;E元素的基态原子价电子排布式为3d104s1.请根据相关信息,回答下列问题:
(1)在A、B、C、D四种元素中第一电离能最小的是___________ ,电负性最大的是___________ (用相应的元素符号表示)
(2)写出DA2的水化物在水中的电离方程式___________ .DA3是___________ 分子(填“极性”或“非极性”)
(3)A、C的简单氢化物中,哪种物质的沸点高,原因是什么?___________________________
(4)若[E(NH3)4]2+具有对称的空间构型,且当[E(NH3)4]2+中的两个NH3分子被两个Cl-取代时,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为_________ (填序号)
a.正四面体 b.平面正方形 c.三角锥形 d.V形
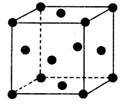
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为a pm,密度为dg·cm-3(1pm=10-10cm)写出阿伏加德罗常数NA的表达式___________ .(用M、a、d表示)
(1)在A、B、C、D四种元素中第一电离能最小的是
(2)写出DA2的水化物在水中的电离方程式
(3)A、C的简单氢化物中,哪种物质的沸点高,原因是什么?
(4)若[E(NH3)4]2+具有对称的空间构型,且当[E(NH3)4]2+中的两个NH3分子被两个Cl-取代时,能得到两种不同结构的产物,则[E(NH3)4]2+的空间构型为
a.正四面体 b.平面正方形 c.三角锥形 d.V形
(5)单质E晶胞如图所示,已知E元素相对原子质量为M,原子半径为a pm,密度为dg·cm-3(1pm=10-10cm)写出阿伏加德罗常数NA的表达式

更新时间:2016-12-09 16:24:04
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E五种短周期元素,原子序数依次增大,其中只有C为金属元素。A、C原子序数之和等于E的原子序数,D与B同主族且D原子序数是B原子序数的2倍。AB2和DB2溶于水得到酸性溶液,C2D溶于水得到碱性溶液。
(1)E元素在周期表中的位置为_______________ ;工业上制取C 单质的化学方程式为______ 。
(2)A的最低负价氢化物的空间构型为___ ;C、D、E 的简单离子的离子半径由大到小的顺序是__ (用离子符号表示)。
(3)化合物C2D3中,该化合物的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程____________________ 。
(1)E元素在周期表中的位置为
(2)A的最低负价氢化物的空间构型为
(3)化合物C2D3中,该化合物的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E五种元素的原子序数均小于18,其原子的电子层结构的信息如下表,请根据信息回答下列问题:
(1)C的元素名称是_______ 。
(2)元素B形成的正离子的结构示意图_______ 。
(3)元素E负离子的电子式可能是_______ 、_______
(4)写出比A离子的电子少8个的两核负离子和五核正离子的化学式_______ 、_______
(5)元素D与氮元素形成化合物的化学式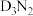 ,将此化合物投入水中,发生复分解反应,此反应的化学方程式是
,将此化合物投入水中,发生复分解反应,此反应的化学方程式是_______ 。
(6)若将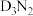 投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:
投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:_______ 、_______
(7)向 溶液中逐滴加入
溶液中逐滴加入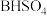 溶液,未看到有气泡产生,但溶液中
溶液,未看到有气泡产生,但溶液中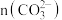 减小,此过程中反生的化学方程式是
减小,此过程中反生的化学方程式是_______ 。继续滴加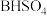 溶液,有气体放出,写出此时反生的化学方程式:
溶液,有气体放出,写出此时反生的化学方程式:_______ 。
| 元素符号 | 元素原子的电子层结构信息 |
| A | 原子M层比C原子L层多3个电子 |
| B | 带1个电荷的正离子的最外层电子数比电子层数多6 |
| C | 原子最外层电子数为K层电子数的2倍 |
| D | 原子M层和最内层电子数之和等于B原子L层电子数的1/2 |
| E | 原子最外层电子数是最内层的3倍 |
(2)元素B形成的正离子的结构示意图
(3)元素E负离子的电子式可能是
(4)写出比A离子的电子少8个的两核负离子和五核正离子的化学式
(5)元素D与氮元素形成化合物的化学式
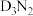 ,将此化合物投入水中,发生复分解反应,此反应的化学方程式是
,将此化合物投入水中,发生复分解反应,此反应的化学方程式是(6)若将
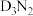 投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:
投入50 mL 1.8 mol/L盐酸中,生成两种盐。写出该两种盐的化学式:(7)向
 溶液中逐滴加入
溶液中逐滴加入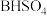 溶液,未看到有气泡产生,但溶液中
溶液,未看到有气泡产生,但溶液中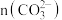 减小,此过程中反生的化学方程式是
减小,此过程中反生的化学方程式是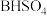 溶液,有气体放出,写出此时反生的化学方程式:
溶液,有气体放出,写出此时反生的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,根据下表相关信息完成以下问题:
(1)X的简单气态氢化物分子的空间结构名称为___________ 。
(2)X、Y对应的简单气态氢化物稳定性由大到小的顺序___________ (用物质化学式表示)。
(3)X、Y、Z、M四种元素的简单离子半径由大到小的顺序是___________ (用离子符号表示)。试从原子结构的角度解释,X的第一电离能比Y大的原因___________ 。
(4)请写出Q元素基态原子的价电子排布图___________ 。
(5)R元素可形成R2+和R3+离子,其中较稳定的是R3+,原因是___________ 。
(6)实验发现M的氯化物处于熔融状态时常以二聚态(M2Cl6)形式存在。其球棍模型如图。___________ 杂化。M的氟化物的熔点为1090℃,远高于M氯化物的熔点192℃,请解释原因___________ 。
| 元素 | 相关信息 |
| X | 原子核外有7种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 位于第三周期,原子半径在同周期元素中最大 |
| M | 逐级电离能(kJ·mol-1)依次为578、1817、2745、11575、14830、18376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有4个未成对电子 |
(2)X、Y对应的简单气态氢化物稳定性由大到小的顺序
(3)X、Y、Z、M四种元素的简单离子半径由大到小的顺序是
(4)请写出Q元素基态原子的价电子排布图
(5)R元素可形成R2+和R3+离子,其中较稳定的是R3+,原因是
(6)实验发现M的氯化物处于熔融状态时常以二聚态(M2Cl6)形式存在。其球棍模型如图。

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有七种元素A、B、C、D、E、F、G,其中A、B、C为三个不同周期的短周期元素,E、F、G为第四周期元素。请根据下列相关信息,回答问题。
(1)C基态原子中能量最高的电子,其电子云在空间有_________ 个方向,原子轨道呈________ 形,C简单离子核外有______ 种运动状态不同的电子。
(2)①一般情况下,同种物质为固态时密度大于其液态,但固态A2B的密度比其液态时小,原因是_______ ;
②A2B2难溶于CS2,简要说明理由:__________________________________________ 。
(3)G位于________ 族________ 区,它的一种氧化物常用于工业生产硫酸的催化剂,已知G在该氧化物中的化合价等于其价电子数,则该氧化物的化学式为_______________ ;F晶体的空间堆积方式为________ 。
(4)ED3分子的VSEPR模型名称为__________ ,其中E原子的杂化轨道类型为________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数与s电子数相等 |
| C基态原子的价电子排布为nsn-1npn+1 |
| D的能层数与C相同,且电负性比C大 |
| E元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第五列 |
(2)①一般情况下,同种物质为固态时密度大于其液态,但固态A2B的密度比其液态时小,原因是
②A2B2难溶于CS2,简要说明理由:
(3)G位于
(4)ED3分子的VSEPR模型名称为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】近日,中科院研究者制备了一种含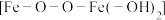 铁双核结构的催化剂,实现了常温下
铁双核结构的催化剂,实现了常温下 高效转化为
高效转化为 。回答下列问题:
。回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为___________ 。
(2)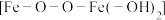 中
中 原子的杂化形式为
原子的杂化形式为___________ ,草酸铁铵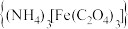 常用于摄影和蓝色印刷,其中
常用于摄影和蓝色印刷,其中 的空间构型为
的空间构型为___________ 。
(3)在无水状态下, 与
与 形成
形成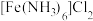 ,
, 含配位键的物质的量为
含配位键的物质的量为___________  ,
, 形成配合物后
形成配合物后 键角会
键角会___________ (填“变大”、“变小”或“不变”),原因是___________ 。
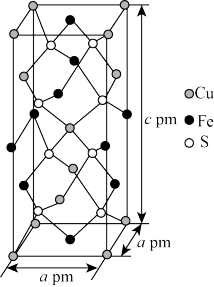
(4)黄铜矿是最重要的铜矿。黄铜矿的长方体晶胞结构及晶胞参数见下图。由图可知,黄铜矿的化学式为___________ ,金属离子占据___________ (填“四面体”或“八面体”)空隙,该晶体的密度为___________  (列出计算式)。设阿伏加德罗常数的值为
(列出计算式)。设阿伏加德罗常数的值为 。
。
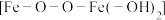 铁双核结构的催化剂,实现了常温下
铁双核结构的催化剂,实现了常温下 高效转化为
高效转化为 。回答下列问题:
。回答下列问题:(1)基态
 的价电子排布式为
的价电子排布式为(2)
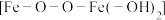 中
中 原子的杂化形式为
原子的杂化形式为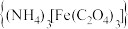 常用于摄影和蓝色印刷,其中
常用于摄影和蓝色印刷,其中 的空间构型为
的空间构型为(3)在无水状态下,
 与
与 形成
形成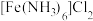 ,
, 含配位键的物质的量为
含配位键的物质的量为 ,
, 形成配合物后
形成配合物后 键角会
键角会(4)黄铜矿是最重要的铜矿。黄铜矿的长方体晶胞结构及晶胞参数见下图。由图可知,黄铜矿的化学式为
 (列出计算式)。设阿伏加德罗常数的值为
(列出计算式)。设阿伏加德罗常数的值为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、R、W 均为周期表中前四周期的元素,其原子序数依次增大;X2-和 Y+有相 同的核外电子排布;Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低;R 的基 态原子在前四周期元素的基态原子中单电子数最多;W 为金属元素,X 与 W 形成的某 种化合物与 Z 的氢化物的浓溶液加热时反应可用于实验室制取 Z 的气态单质。回答下 列问题(相关回答均用元素符号表示):
(1)R 的基态原子的核外电子排布式是__________________ 。
(2)Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是______________ 。
(3)X 与 Z 中电负性较大的是_____ 。Z 的某种含氧酸盐常用于实验室中 X 的单质的 制取,此酸根离子的空间构型是______________ ,此离子中含有的化学键类型 是_________ ,X—Z—X 的键角_______ 109.5°(填“>”、“=”或“<”)。
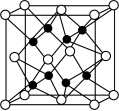
(4)X 与 Y 形成的化合物 Y2X 的晶胞如图。其中 X 离子的配位数 为___________ ,以相距一个 X 离子最近的所有 Y 离子为顶点构成的几何体为___________ 。该化合物与 MgO 相比,熔点较高的是____________ 。
(5)已知该化合物的晶胞边长为 a pm,则该化合物的密度为________________ g·cm-3(只要求列算式,不必计算出数值,阿伏加德岁常数的数值为 NA)。
(1)R 的基态原子的核外电子排布式是
(2)Z 的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是
(3)X 与 Z 中电负性较大的是

(4)X 与 Y 形成的化合物 Y2X 的晶胞如图。其中 X 离子的配位数 为
(5)已知该化合物的晶胞边长为 a pm,则该化合物的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于______ 晶体,俗名叫______ ;
(2)R的氢化物分子的空间构型是______ ,属于______ 分子(填“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是______ ;
(3)X的常见氢化物的空间构型是______ ,它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是______ ;
(4)Q分别与Y、Z形成的共价化合物的化学式是______ 和______ ,Q与Y形成的分子的电子式是______ ,属于______ 分子(填“极性”或“非极性”)。
(1)Q的最高价氧化物,其固态属于
(2)R的氢化物分子的空间构型是
(3)X的常见氢化物的空间构型是
(4)Q分别与Y、Z形成的共价化合物的化学式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】蒙脱石散对消化道内的病毒、病菌及其产生的毒素、气体等有极强的固定、抑制作用,常用于成人及儿童急性、慢性腹泻。蒙脱石散的有效成分可表示为(AlMg)2(SixOy)(OH)z·nH2O。
(1)基态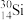 原子的核外电子排布式为
原子的核外电子排布式为___________ 。
(2)比较:①熔点高低:MgO___________ CaO,②键角大小:H2O___________ NH3(填“>”“<”或“=”)
(3)SiCl4是无色透明液体,可以与N-甲基咪唑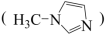 等物质反应。
等物质反应。
①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液体流___________ (填“会”或“不会”)发生偏转。
②一个N-甲基咪唑分子中含有________ 个σ键;SiCl4中硅原子的杂化方式为___________ 。
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成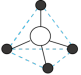 :其中
:其中 表示氧原子,中心
表示氧原子,中心 表示硅原子,其俯视图为
表示硅原子,其俯视图为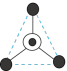 。
。
①SiO2晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在Si—Si之间插入O原子而形成。
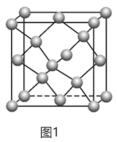
推测SiO2晶胞中含有___________ 个O原子,O—Si—O的键角为___________ 。
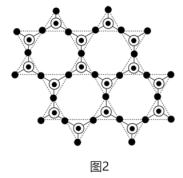
②蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图2所示,则x∶y=________ 。
(1)基态
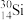 原子的核外电子排布式为
原子的核外电子排布式为(2)比较:①熔点高低:MgO
(3)SiCl4是无色透明液体,可以与N-甲基咪唑
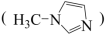 等物质反应。
等物质反应。①将用毛皮摩擦过的橡胶棒靠近SiCl4液流,液体流
②一个N-甲基咪唑分子中含有
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成
 :其中
:其中 表示氧原子,中心
表示氧原子,中心 表示硅原子,其俯视图为
表示硅原子,其俯视图为 。
。①SiO2晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在Si—Si之间插入O原子而形成。

推测SiO2晶胞中含有
②蒙脱石散中的“(SixOy)”是一种大片层状的多硅酸根,其可能结构如图2所示,则x∶y=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)钒(23V)元素价层电子的电子排布图为___________ 。第四周期末成对电子数最多的元素是___________ (填元素符号),该元素基态原子核外电子共有___________ 种不同能量的电子。
(2)丁二酮肟( )中
)中 键与
键与 键数目之比为
键数目之比为___________ 。
(3)下列关于物质结构的表述中正确的是___________ 。
①元素Br位于周期表第四周期VIIA族,核外电子排布式为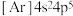 ,属于p区
,属于p区
②非极性分子往往具有高度对称性,如 、
、 、
、 、
、 分子
分子
③晶体与非晶体的本质区别为是否具有固定的熔点
④ 是极性分子,故
是极性分子,故 易溶于水
易溶于水
(4)向硫酸铜溶液中滴加浓氨水,先出现蓝色沉淀,继续滴加氨水,沉淀溶解,出现深蓝色溶液,用离子方程式解释沉淀溶解的原因:___________ 。
(5) 晶胞结构如图所示。D离子代表的是
晶胞结构如图所示。D离子代表的是___________ ,其配位数为___________ ,若晶胞参数为anm,则最近的D原子和B原子之间的距离为___________ nm。 的结构如图所示。
的结构如图所示。 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是___________ (填序号)。
(1)钒(23V)元素价层电子的电子排布图为
(2)丁二酮肟(
 )中
)中 键与
键与 键数目之比为
键数目之比为(3)下列关于物质结构的表述中正确的是
①元素Br位于周期表第四周期VIIA族,核外电子排布式为
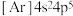 ,属于p区
,属于p区②非极性分子往往具有高度对称性,如
 、
、 、
、 、
、 分子
分子③晶体与非晶体的本质区别为是否具有固定的熔点
④
 是极性分子,故
是极性分子,故 易溶于水
易溶于水(4)向硫酸铜溶液中滴加浓氨水,先出现蓝色沉淀,继续滴加氨水,沉淀溶解,出现深蓝色溶液,用离子方程式解释沉淀溶解的原因:
(5)
 晶胞结构如图所示。D离子代表的是
晶胞结构如图所示。D离子代表的是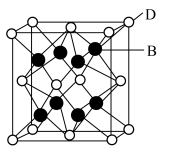
 的结构如图所示。
的结构如图所示。
 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】三卤化氮( )如
)如 、
、 等有广泛的用途。
等有广泛的用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌。回答下面问题:
可用于面粉的漂白和杀菌。回答下面问题:
(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式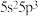 ,可知锑在元素周期表的位置是
,可知锑在元素周期表的位置是___________ 。基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是___________ ,原子半径由大到小的顺序是___________ 。
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为___________ 。液晶在放电过程中会产生 和
和 离子,其中N原子的杂化类型分别是
离子,其中N原子的杂化类型分别是___________ ,键角:
___________  (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。
(4)已知热稳定性 高于
高于 ,解释其原因是
,解释其原因是___________ 。常温常压下 为无色气体,
为无色气体, 为黄色油状液体,
为黄色油状液体, 和
和 价层电子对互斥模型均为
价层电子对互斥模型均为___________ , 和
和 的分子空间构型均为
的分子空间构型均为___________ 。
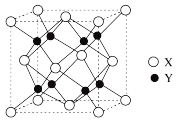
(5) 的晶胞结构如图所示,X代表的离子是
的晶胞结构如图所示,X代表的离子是___________ ;若该立方晶胞参数为apm, 的摩尔质量用
的摩尔质量用 ,阿伏加德罗常数用
,阿伏加德罗常数用 来表示,则
来表示,则 晶体的密度=
晶体的密度=___________  (写出表达式)。
(写出表达式)。
 )如
)如 、
、 等有广泛的用途。
等有广泛的用途。 是液晶显示器生产过程中常用的化学清洗剂,
是液晶显示器生产过程中常用的化学清洗剂, 可用于面粉的漂白和杀菌。回答下面问题:
可用于面粉的漂白和杀菌。回答下面问题:(1)锑是制造液晶显示器的一种原材料,基态锑的价层电子排布式
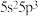 ,可知锑在元素周期表的位置是
,可知锑在元素周期表的位置是(2)元素F、O、N位于同一周期,其第一电离能由大到小的顺序是
(3)液晶显示器材料因含微量杂质元素铬(Cr)而呈浅红色。基态铬原子的价层电子排布式为
 和
和 离子,其中N原子的杂化类型分别是
离子,其中N原子的杂化类型分别是
 (填“<”或“=”或“>”)。
(填“<”或“=”或“>”)。(4)已知热稳定性
 高于
高于 ,解释其原因是
,解释其原因是 为无色气体,
为无色气体, 为黄色油状液体,
为黄色油状液体, 和
和 价层电子对互斥模型均为
价层电子对互斥模型均为 和
和 的分子空间构型均为
的分子空间构型均为(5)
 的晶胞结构如图所示,X代表的离子是
的晶胞结构如图所示,X代表的离子是 的摩尔质量用
的摩尔质量用 ,阿伏加德罗常数用
,阿伏加德罗常数用 来表示,则
来表示,则 晶体的密度=
晶体的密度= (写出表达式)。
(写出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钛被视为继铁、铝之后的第三金属,也有人说“21世纪将是钛的世纪”,钛和钛的化合物在航天、化工、建筑、医疗中都有着广泛的用途。回答下列问题:
(1)基态钛原子核外有_______ 种能量不同的电子,其能量最高的电子所在的能层符号为_______ 。
(2)钛与卤素形成的化合物TiX4熔点如下表
TiCl4、TiBr4、TiI4熔点依次升高的原因_______ 。
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①Ti(BH4)3中所含元素电负性由小到大的顺序为_______ 。
②TiCl4 与SiCl4结构相似,TiCl4的中心原子价层电子对数_______ 。
③LiBH4 由Li+和BH 构成,BH
构成,BH 中B原子的杂化类型是
中B原子的杂化类型是_______ 。
④LiBH4存在_______ (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
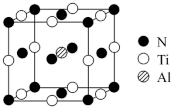
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,已知该晶体的晶胞参数(棱边边长)为a pm,用Al掺杂TiN后,其晶胞结构如下图所示,距离Al最近的Ti有_______ 个,掺杂Al后的晶体密度是TiN晶体的_______ 倍(写出含a的表达式)。
(1)基态钛原子核外有
(2)钛与卤素形成的化合物TiX4熔点如下表
| TiX4 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点℃ | 377 | -24 | 38.3 | 153 |
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①Ti(BH4)3中所含元素电负性由小到大的顺序为
②TiCl4 与SiCl4结构相似,TiCl4的中心原子价层电子对数
③LiBH4 由Li+和BH
 构成,BH
构成,BH 中B原子的杂化类型是
中B原子的杂化类型是④LiBH4存在
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,已知该晶体的晶胞参数(棱边边长)为a pm,用Al掺杂TiN后,其晶胞结构如下图所示,距离Al最近的Ti有

您最近一年使用:0次
【推荐3】中科院大连化物所的科学家在乙酰酮修饰锰氧化物L酸催化胺选择氧化方面的研究取得新进展。回答下列问题:
(1)Mn元素的价层电子排布式为_______ ;Mn元素的一种配合物K3[Mn(CN)6]具有反磁性,配体CN-的电子式为_______ 。
(2)乙腈(CH3CN)分子中碳原子的杂化类型有_______ ,该分子中σ键和π键的个数比为_______ 。
(3)苯胺(C6H5NH2)的晶体类型是_______ ,苯胺与甲苯的相对分子质量相近,但苯胺的熔、沸点分别高于甲苯的熔、沸点,原因是_______ 。
(4)锰的某种氧化物的晶胞结构如图所示:

该锰元素的氧化物化学式为_______ ,晶体的密度为_______  (用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(1)Mn元素的价层电子排布式为
(2)乙腈(CH3CN)分子中碳原子的杂化类型有
(3)苯胺(C6H5NH2)的晶体类型是
(4)锰的某种氧化物的晶胞结构如图所示:

该锰元素的氧化物化学式为
 (用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
(用含a、b和NA的代数式表示,NA为阿伏加德罗常数的值)。
您最近一年使用:0次



