反应CH3OH(l)+NH3(g)→CH3NH2(g)+H2O(g)在某温度时才能自发向右进行,若该反应的ΔH=+17 kJ/mol,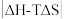 =17 kJ/mol,则下列关系中正确的是
=17 kJ/mol,则下列关系中正确的是
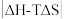 =17 kJ/mol,则下列关系中正确的是
=17 kJ/mol,则下列关系中正确的是| A.ΔS>0,ΔH-TΔS<0 | B.ΔS<0,ΔH-TΔS>0 |
| C.ΔS>0,ΔH-TΔS>0 | D.ΔS<0,ΔH-TΔS<0 |
2016高二·全国·课时练习 查看更多[2]
更新时间:2017-11-27 16:00:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知:
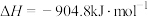 ,下列说法正确的是
,下列说法正确的是

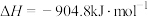 ,下列说法正确的是
,下列说法正确的是A.该反应 |
| B.反应物的总煡能小于生成物的总煡能 |
C.反应平衡常数 |
D.平衡后升高温度, 增大, 增大,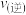 减小,平衡向逆反应方向移动 减小,平衡向逆反应方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】气态 的一种工业制法流程如图:
的一种工业制法流程如图: 为阿伏加德罗常数的值②
为阿伏加德罗常数的值② 时,次磷酸(
时,次磷酸( )的电离常数
)的电离常数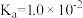 ,下列说法错误的是
,下列说法错误的是
 的一种工业制法流程如图:
的一种工业制法流程如图: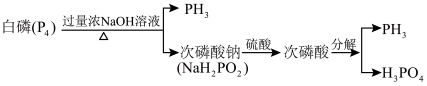
 为阿伏加德罗常数的值②
为阿伏加德罗常数的值② 时,次磷酸(
时,次磷酸( )的电离常数
)的电离常数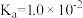 ,下列说法错误的是
,下列说法错误的是| A.液态次磷酸分解反应为熵增过程 |
B. 是非极性分子, 是非极性分子, 所含价层电子对数为 所含价层电子对数为 |
C.白磷与浓 溶液反应生成 溶液反应生成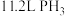 (标准状况下)时,转移电子的数目为 (标准状况下)时,转移电子的数目为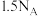 |
D.常温下,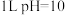 的 的 溶液中由水电离出的 溶液中由水电离出的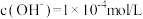 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将E(s)和F(g)加入密闭容器中,在一定条件下发生反应E(s)+4F(g) G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是
 G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.上述反应是熵增反应 |
B.25℃时,反应G(g) E(s)+4F(g)的平衡常数是0.5 E(s)+4F(g)的平衡常数是0.5 |
| C.在80℃时,测得某时刻F、G的浓度均为0.5mol·L-1,则此时v正>v逆 |
| D.恒温恒容下,向容器中再充入少量G(g),达到新平衡时,G的体积百分含量将增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应的方向问题对于理论研究与生产实践都有重要的意义。下列说法错误的是
A. 时,熵减小 时,熵减小 |
B.恒温恒压下, 且 且 的反应一定能自发进行 的反应一定能自发进行 |
C. 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的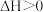 |
D.反应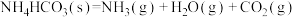 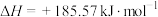 能自发进行,原因是熵增效应大于焓增效应 能自发进行,原因是熵增效应大于焓增效应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,反应2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行。下列说法正确的是
| A.该反应为吸热反应 |
| B.该反应中,SO2为还原剂 |
| C.1 mol H2S中含有的共价键的数目为3 mol |
| D.常温下,H2S的还原性强于S的还原性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
A. 在常温下可自发进行,则该反应的 在常温下可自发进行,则该反应的 |
B.一定条件下反应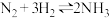 达到平衡时,3v正(H2)=2v逆(NH3) 达到平衡时,3v正(H2)=2v逆(NH3) |
C.向 溶液中加入少量水,溶液中 溶液中加入少量水,溶液中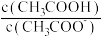 比值减小 比值减小 |
| D.Na2O2与足量的水反应生成0.2 mol O2,转移电子数目为0.8 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.恒温恒压下,△H < 0 且△S > 0 的反应一定不能自发进行 |
| B.1 mol H2O 在不同状态时的熵值:S[H2O(s)] < S[H2O(g)] |
| C.反应 NH3(g) + HCl(g) = NH4Cl(s)在室温下可自发进行,则该反应的△H < 0 |
| D.反应 CaCO3(s) = CaO(s) + CO2(g) △H > 0,能否自发进行与温度有关 |
您最近一年使用:0次



