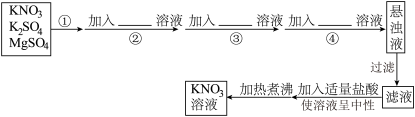
现有三种可溶物质A、B、C,其中A、B是盐,一种是酸式盐,一种是正盐,C是碱,它们溶于水后电离产生的所用离子如下表所示:
请根据下列叙述回答问题:
(1)C的化学式为_________________ 。
(2)A溶液与B溶液反应可生成气体X,则X的化学式为_______________ ,该反应的化学反应方程式为___________________ 。
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为____________ ,鉴别溶液中B的阴离子的方法是___________________ 。
②D溶于稀硝酸的离子方程式为___________________________ 。
| 阳离子 | Na+、H+、Ba2+ |
| 阴离子 | OH-、 、 、 |
(1)C的化学式为
(2)A溶液与B溶液反应可生成气体X,则X的化学式为
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸。
①B的化学式为
②D溶于稀硝酸的离子方程式为
更新时间:2016-12-09 17:20:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硒是人体不可缺少的微量元素,硒的应用范围非常广泛。以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)提取硒一种工艺流程如下:
等)提取硒一种工艺流程如下:
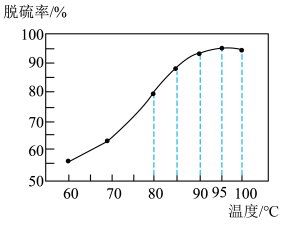
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;_______ ,最佳脱硫温度为_______ 。 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可采用硫脲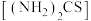 联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原 ,该过程的还原反应(半反应)式为
,该过程的还原反应(半反应)式为_______ ,为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_______ V以上。
(4)“精制”过程中 先将Se浸出转化成硒代硫酸钠(
先将Se浸出转化成硒代硫酸钠(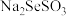 ),
),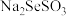 再被
再被 酸化生成硒的离子方程式为
酸化生成硒的离子方程式为_______ 。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg⋅g ,则精硒中铁的质量分数为
,则精硒中铁的质量分数为_______ %。
 、CuO、ZnO、
、CuO、ZnO、 等)提取硒一种工艺流程如下:
等)提取硒一种工艺流程如下: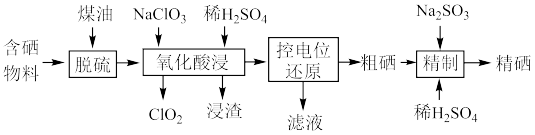
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;
 ,该反应的化学方程式为
,该反应的化学方程式为(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可采用硫脲
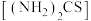 联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。名称 |
|
|
|
|
|
|
中位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
 ,该过程的还原反应(半反应)式为
,该过程的还原反应(半反应)式为(4)“精制”过程中
 先将Se浸出转化成硒代硫酸钠(
先将Se浸出转化成硒代硫酸钠(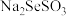 ),
), 再被
再被 酸化生成硒的离子方程式为
酸化生成硒的离子方程式为(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg⋅g
 ,则精硒中铁的质量分数为
,则精硒中铁的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组在实验室用63%的浓 HNO3 (其密度为1.39g/cm³,已知 ,配制480 mL 0.50 mol/L 稀 HNO3,并探究稀 HNO3 与物质的反应。①石灰石 ②氧化铜 ③二氧化硫 ④NaOH溶液 ⑤铁丝 ⑥碳酸氢钠 ⑦氯化银,回答下列问题:
,配制480 mL 0.50 mol/L 稀 HNO3,并探究稀 HNO3 与物质的反应。①石灰石 ②氧化铜 ③二氧化硫 ④NaOH溶液 ⑤铁丝 ⑥碳酸氢钠 ⑦氯化银,回答下列问题:
(1)该浓硝酸的物质的量浓度为___________ mol/L。
(2)用该浓 HNO3 配制480 mL0.50 mol/L 稀 HNO3需要使用的玻璃仪器有量筒、烧杯、玻璃棒、___________ 和___________ mL容量瓶,应量取浓硝酸的体积为___________ mL(保留三位有效数字)。
(3)如图为溶液配制过程,正确的操作顺序为___________ (用字母表示),操作 d 为洗涤烧杯和玻璃榨并将洗涤液转入容量瓶的过程,若省略该操作将会导致配制的稀硝酸的浓度___________ (填“偏低”“偏高”或“无影响”)。
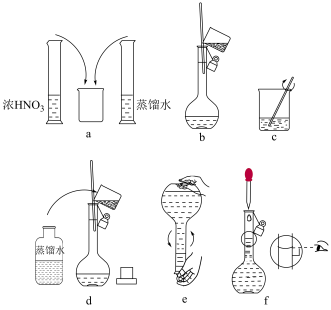
(4)物质①~⑦中,常温下可导电的物质为___________ (填序号,下同),属于非电解质的为___________ 。
(5)基于HNO3的类别推测,其能与碳酸氢钠发生反应,写出稀硝酸与碳酸氢钠溶液反应的离子方程式:___________ 。
(6)该小组同学推测稀 HNO3可与物质③反应,其将一定量二氧化硫通入3mL 稀 HNO3中并在反应后的溶液中检出了 ,查阅资料知稀硝酸被还原为 NO,试写出该反应的离子方程式:
,查阅资料知稀硝酸被还原为 NO,试写出该反应的离子方程式:___________ 。
 ,配制480 mL 0.50 mol/L 稀 HNO3,并探究稀 HNO3 与物质的反应。①石灰石 ②氧化铜 ③二氧化硫 ④NaOH溶液 ⑤铁丝 ⑥碳酸氢钠 ⑦氯化银,回答下列问题:
,配制480 mL 0.50 mol/L 稀 HNO3,并探究稀 HNO3 与物质的反应。①石灰石 ②氧化铜 ③二氧化硫 ④NaOH溶液 ⑤铁丝 ⑥碳酸氢钠 ⑦氯化银,回答下列问题:(1)该浓硝酸的物质的量浓度为
(2)用该浓 HNO3 配制480 mL0.50 mol/L 稀 HNO3需要使用的玻璃仪器有量筒、烧杯、玻璃棒、
(3)如图为溶液配制过程,正确的操作顺序为

(4)物质①~⑦中,常温下可导电的物质为
(5)基于HNO3的类别推测,其能与碳酸氢钠发生反应,写出稀硝酸与碳酸氢钠溶液反应的离子方程式:
(6)该小组同学推测稀 HNO3可与物质③反应,其将一定量二氧化硫通入3mL 稀 HNO3中并在反应后的溶液中检出了
 ,查阅资料知稀硝酸被还原为 NO,试写出该反应的离子方程式:
,查阅资料知稀硝酸被还原为 NO,试写出该反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯气是一种重要的化工原料,呈黄绿色,有毒,能与多种物质反应。用下图装置可制取氯气,并对其性质进行一系列的实验探究。
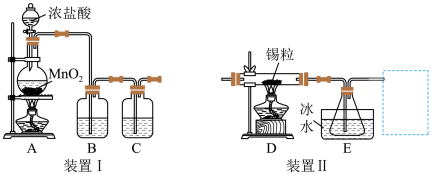

回答下列问题:
(1)①装置Ⅰ中盛装浓盐酸的仪器名称是___________ 。
(2)利用纯净、干燥的氯气与熔融金属锡反应可制备SnCl4,将装置Ⅰ与装置Ⅱ连接起来可制备SnCl4。已知:金属锡熔点为231 ℃,活泼性与铁相似;SnCl4的沸点为114 ℃;SnCl4易与水反应。
①装置E的作用是___________ 。
②装置D中反应的方程式是___________ 。
③虚线框可选用下列装置中的___________ (填“甲”、“乙”或“丙”)。

(3)将装置Ⅰ与装置Ⅲ连接起来探究氯气的漂白性及氧化性。
①实验开始后,观察到洗气瓶H中的现象是___________ 。
②装置J中发生的离子方程式是:___________ 。
③装置K的作用是___________ 。


回答下列问题:
(1)①装置Ⅰ中盛装浓盐酸的仪器名称是
(2)利用纯净、干燥的氯气与熔融金属锡反应可制备SnCl4,将装置Ⅰ与装置Ⅱ连接起来可制备SnCl4。已知:金属锡熔点为231 ℃,活泼性与铁相似;SnCl4的沸点为114 ℃;SnCl4易与水反应。
①装置E的作用是
②装置D中反应的方程式是
③虚线框可选用下列装置中的

(3)将装置Ⅰ与装置Ⅲ连接起来探究氯气的漂白性及氧化性。
①实验开始后,观察到洗气瓶H中的现象是
②装置J中发生的离子方程式是:
③装置K的作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色溶液,其中有可能存在的离子如下:Na+、Ag+、 Ba2+、Al3+、AlO 、S2-、CO
、S2-、CO 、SO
、SO 、SO
、SO ,现取该溶液进行有关实验,实验结果如下图所示:
,现取该溶液进行有关实验,实验结果如下图所示:

试回答下列问题:
(1)淡黄色沉淀是:___________ ;
(2)沉淀乙是:___________ ,由溶液甲生成沉淀乙的离子方程式为:___________ ;
(3)沉淀丙一定含有___________ ,可能含有___________ ;
(4)气体甲成分可能有哪几种?(可以不填满也可以补充)___________
(5)综合上述信息,可以肯定存在的离子:___________ 。
 、S2-、CO
、S2-、CO 、SO
、SO 、SO
、SO ,现取该溶液进行有关实验,实验结果如下图所示:
,现取该溶液进行有关实验,实验结果如下图所示:
试回答下列问题:
(1)淡黄色沉淀是:
(2)沉淀乙是:
(3)沉淀丙一定含有
(4)气体甲成分可能有哪几种?(可以不填满也可以补充)
| 1 | 2 | 3 | 4 | 5 | 6 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe2+、Mg2+、Ba2+、NH4+、Cl-、 、
、 ,现取两份100mL溶液进行如下实验:
,现取两份100mL溶液进行如下实验:
①第一份加过量NaOH溶液加热后,只收集到气体0.02mol,无沉淀生成,同时得到溶液甲。
②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g。
③第二份加足量BaCl2溶液后,得白色沉淀,加盐酸不溶解,经过滤、洗涤、干燥后,称得沉淀质量为13.98g。
(1)由上述实验可确定溶液中一定不存在的离子是______________ ,不能确定是否存在的离子是_______ ,检验该离子需使用何种试剂或方法______________ 。
(2)由题意可知此溶液呈________ 性(答酸性、碱性或中性),上述金属离子中既能被氧化又能被还原的离子是___________ 。
(3)钾离子是否存在(是或否):_______ ,若存在其浓度范围为(没有则不答):_________ 。
 、
、 ,现取两份100mL溶液进行如下实验:
,现取两份100mL溶液进行如下实验:①第一份加过量NaOH溶液加热后,只收集到气体0.02mol,无沉淀生成,同时得到溶液甲。
②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g。
③第二份加足量BaCl2溶液后,得白色沉淀,加盐酸不溶解,经过滤、洗涤、干燥后,称得沉淀质量为13.98g。
(1)由上述实验可确定溶液中一定不存在的离子是
(2)由题意可知此溶液呈
(3)钾离子是否存在(是或否):
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.有一白色固体粉末,可能含有NaCl、Na2SO4、Na2CO3、KNO3、BaCl2和CuSO4中的一种或几种,按以下步骤进行实验:
①将该固体粉末放入足量水中得到无色溶液和白色不溶物。
②过滤,在不溶物中加入足量稀盐酸,有气泡产生。充分反应后仍有不溶物存在。
③取②的滤液于试管中。加入Cu粉,微热,一段时间后试管口出现红棕色。
根据以上实验现象判断:
(1)混合物中一定没有___________ ;可能有___________ 。(均填化学式)
(2)写出②中反应的化学方程式:___________
(3)写出③中溶液里反应的离子方程式:___________
Ⅱ. A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去)。请回答下列问题:

(4)若X是强氧化性单质,则A不可能是___________ (填序号)。
a.C b.N2 c.S d.Mg e.Al
(5)若A能使湿润的红色石蕊试纸变蓝,C为红棕色的气体。A转化为B的化学方程式为___________ 。
①将该固体粉末放入足量水中得到无色溶液和白色不溶物。
②过滤,在不溶物中加入足量稀盐酸,有气泡产生。充分反应后仍有不溶物存在。
③取②的滤液于试管中。加入Cu粉,微热,一段时间后试管口出现红棕色。
根据以上实验现象判断:
(1)混合物中一定没有
(2)写出②中反应的化学方程式:
(3)写出③中溶液里反应的离子方程式:
Ⅱ. A、B、C、X是中学化学中常见的物质,它们之间的转化关系如图所示(部分产物已略去)。请回答下列问题:

(4)若X是强氧化性单质,则A不可能是
a.C b.N2 c.S d.Mg e.Al
(5)若A能使湿润的红色石蕊试纸变蓝,C为红棕色的气体。A转化为B的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工业废水中存在大量的 Na+、Cl-、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计工艺流程如图所示:
,设计工艺流程如图所示:

(1)试剂c溶液为___________ ,试剂 b 溶液为___________ ,试剂 a 溶液为___________ 。
(2)NaOH的作用是___________ ,流程图中,操作 X 所需玻璃仪器为___________ 。
(3)试剂 a、b 能否对调___________ ?(填“能”或“否”),原因是___________ 。
(4)如何检验废水中的 已沉淀完全:
已沉淀完全:___________ 。
(5)如果在工业废水中直接加入氢氧化钡溶液,写出发生反应的离子方程式:___________ 。
 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计工艺流程如图所示:
,设计工艺流程如图所示:
(1)试剂c溶液为
(2)NaOH的作用是
(3)试剂 a、b 能否对调
(4)如何检验废水中的
 已沉淀完全:
已沉淀完全:(5)如果在工业废水中直接加入氢氧化钡溶液,写出发生反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业烟气的主要成分有:空气、固体颗粒物、 、
、 ,可能含有
,可能含有 。工业上使用“钠钙双碱法”净化工业烟气,取得了很好的除污效果。某兴趣小组在实验室对这一方法进行了简化模拟,吸收顺序是“先钠(NaOH)后钙(
。工业上使用“钠钙双碱法”净化工业烟气,取得了很好的除污效果。某兴趣小组在实验室对这一方法进行了简化模拟,吸收顺序是“先钠(NaOH)后钙( )”。模拟的流程如下:
)”。模拟的流程如下:
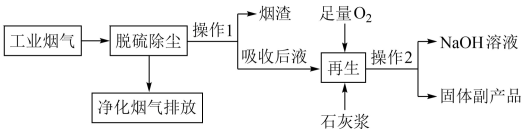
已知: 属于酸性氧化物。
属于酸性氧化物。
(1)在“脱硫除尘”环节中, 与NaOH溶液反应的化学方程式为
与NaOH溶液反应的化学方程式为___________ 。
(2)操作1、2的名称为___________ 。
(3)实验测得操作1得到的“吸收后液”中主要含有 (还有少量NaOH、
(还有少量NaOH、 和
和 )
)
①请写出 的电离方程式
的电离方程式___________ 。
②能否确定 一定来自于反应
一定来自于反应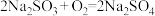 ,理由是
,理由是___________ 。
③确定“吸收后液”含有 的实验操作是
的实验操作是___________ 。
(4)若“再生”阶段石灰浆恰好反应完全,则流程中可循环利用的物质为___________ 。
(5)净化 烟气,
烟气, 浓度为
浓度为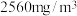 、完全被吸收(忽略
、完全被吸收(忽略 和
和 ),需要消耗
),需要消耗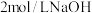 溶液的体积为多少?“再生”时,理论上至少需
溶液的体积为多少?“再生”时,理论上至少需 质量为多少
质量为多少___________ ?(必须有计算过程,无过程不得分)
 、
、 ,可能含有
,可能含有 。工业上使用“钠钙双碱法”净化工业烟气,取得了很好的除污效果。某兴趣小组在实验室对这一方法进行了简化模拟,吸收顺序是“先钠(NaOH)后钙(
。工业上使用“钠钙双碱法”净化工业烟气,取得了很好的除污效果。某兴趣小组在实验室对这一方法进行了简化模拟,吸收顺序是“先钠(NaOH)后钙( )”。模拟的流程如下:
)”。模拟的流程如下:
已知:
 属于酸性氧化物。
属于酸性氧化物。(1)在“脱硫除尘”环节中,
 与NaOH溶液反应的化学方程式为
与NaOH溶液反应的化学方程式为(2)操作1、2的名称为
(3)实验测得操作1得到的“吸收后液”中主要含有
 (还有少量NaOH、
(还有少量NaOH、 和
和 )
)①请写出
 的电离方程式
的电离方程式②能否确定
 一定来自于反应
一定来自于反应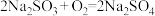 ,理由是
,理由是③确定“吸收后液”含有
 的实验操作是
的实验操作是(4)若“再生”阶段石灰浆恰好反应完全,则流程中可循环利用的物质为
(5)净化
 烟气,
烟气, 浓度为
浓度为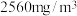 、完全被吸收(忽略
、完全被吸收(忽略 和
和 ),需要消耗
),需要消耗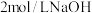 溶液的体积为多少?“再生”时,理论上至少需
溶液的体积为多少?“再生”时,理论上至少需 质量为多少
质量为多少
您最近一年使用:0次

 /Cu
/Cu /Zn
/Zn /Fe
/Fe
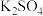 、
、 的
的 固体提纯,并制得纯净的
固体提纯,并制得纯净的