目前全球范围内环境污染备受关注,化工生产中应大力倡导“绿色化学”和“原子经济”的理念,工业生产中的废物利用尤为重要。工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:
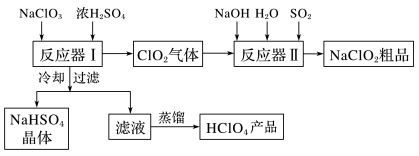
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为_______ ,冷却的目的是____________ 。
(2)反应器Ⅱ中发生反应的离子方程式为__________________________ 。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是_________________________ 。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,请写出工业上用氯气和消石灰生产漂粉精的化学方程式:___________________________________ 。

已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为
(2)反应器Ⅱ中发生反应的离子方程式为
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,请写出工业上用氯气和消石灰生产漂粉精的化学方程式:
更新时间:2017-03-03 21:26:59
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】锶(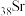 )元素广泛存在于矿泉水中,是一种人体必需的微量元素。碳酸锶(
)元素广泛存在于矿泉水中,是一种人体必需的微量元素。碳酸锶( )是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%
)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% ,少量
,少量 、
、 、
、 等)制备高纯碳酸锶的工艺流程如下:
等)制备高纯碳酸锶的工艺流程如下: 在水中的溶解度
在水中的溶解度
(1)①碱性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
②用原子结构的观点解释锶的化学性质与钡差异的原因:___________ 。
(2)菱锶矿、焦炭混合粉碎的目的是___________ 。
(3)“立窑煅烧”中 与焦炭反应的化学方程式为
与焦炭反应的化学方程式为___________ ,进行煅烧反应的立窑衬里应选择___________ (填“石英砂砖”或“碱性耐火砖”)。
(4)“浸取”中用热水浸取而不用冷水的原因是___________ ,滤渣1含有焦炭、 和
和___________ 。
(5)“沉锶”中反应的化学方程式为___________ 。
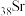 )元素广泛存在于矿泉水中,是一种人体必需的微量元素。碳酸锶(
)元素广泛存在于矿泉水中,是一种人体必需的微量元素。碳酸锶( )是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%
)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% ,少量
,少量 、
、 、
、 等)制备高纯碳酸锶的工艺流程如下:
等)制备高纯碳酸锶的工艺流程如下:
 在水中的溶解度
在水中的溶解度| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度/( ) ) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |

 (填“>”或“<”)。
(填“>”或“<”)。②用原子结构的观点解释锶的化学性质与钡差异的原因:
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中
 与焦炭反应的化学方程式为
与焦炭反应的化学方程式为(4)“浸取”中用热水浸取而不用冷水的原因是
 和
和(5)“沉锶”中反应的化学方程式为
您最近一年使用:0次
【推荐2】芜湖市某便利店销售的一种食用碘盐包装袋上有如下标签:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,请配平化学方程式:____ KIO3+____ KI+____ H2SO4=____ K2SO4+_____ I2+____ H2O
(2)实验室可分离获取单质碘,其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把适量碘水和CCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口玻璃塞是否漏液;
D.倒转漏斗,用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.从分液漏斗的上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开;
H.静置、分层;
①正确的操作顺序是(用编号字母填写)____ →____ → ___ →A → __ → ___ →E→F。
②下列物质,不能作为从水溶液中萃取碘的溶剂是____ 。
A.苯 B.汽油 C.酒精
(3)若向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。理论上Na2SO3与I2反应的物质的量之比为____ 。
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,请配平化学方程式:
(2)实验室可分离获取单质碘,其实验操作可分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把适量碘水和CCl4加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口玻璃塞是否漏液;
D.倒转漏斗,用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.从分液漏斗的上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开;
H.静置、分层;
①正确的操作顺序是(用编号字母填写)
②下列物质,不能作为从水溶液中萃取碘的溶剂是
A.苯 B.汽油 C.酒精
(3)若向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。理论上Na2SO3与I2反应的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】I.亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂。在NaOH溶液中ClO2与H2O2反应可以得到亚氯酸钠。
(1)在制备亚氯酸钠的反应中ClO2作_ (填“氧化剂”或“还原剂”);若反应中生成1 mol NaClO2,转移电子的物质的量为__ 。
(2)该反应的化学方程式为__ 。
II.有一瓶澄清的溶液,其中可能含有 、K+、Ba2+、Al3+、Fe3+、I-、
、K+、Ba2+、Al3+、Fe3+、I-、 、
、 、
、 、[Al(OH)4]-。取该溶液进行以下实验:
、[Al(OH)4]-。取该溶液进行以下实验:
①用pH试纸检测,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性;
b.溶液中逐渐产生沉淀;
c.沉淀完全溶解;
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除_______ 的存在。
(2)由②可以证明_______ 的存在;同时排除_______ 的存在。
(3)由③可以证明_______ 的存在。
(4)由④可以排除 的存在,同时证明Ba2+的存在。
的存在,同时证明Ba2+的存在。
(5)写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:
c._______ ;d._______ 。
(1)在制备亚氯酸钠的反应中ClO2作
(2)该反应的化学方程式为
II.有一瓶澄清的溶液,其中可能含有
 、K+、Ba2+、Al3+、Fe3+、I-、
、K+、Ba2+、Al3+、Fe3+、I-、 、
、 、
、 、[Al(OH)4]-。取该溶液进行以下实验:
、[Al(OH)4]-。取该溶液进行以下实验:①用pH试纸检测,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性;
b.溶液中逐渐产生沉淀;
c.沉淀完全溶解;
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题。
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以排除
 的存在,同时证明Ba2+的存在。
的存在,同时证明Ba2+的存在。(5)写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:
c.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室用如图装置制备并收集干燥纯净 的 。
。

(1)装置A中反应的化学方程式是_______ 。
(2)装置B的作用是_______ 。
(3)装置C中盛放的物质是_______ 。
(4)装置E用于吸收尾气,E中反应的离子方程式是_______ 。
(5)漂粉精常用于游泳池的消毒,起消毒作用的是HClO;池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会_______ (填“增强”或“减弱”)。
②池水酸性过强,会刺激眼睛和皮肤。有时加入 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是_______ (填离子符号)。
 。
。
(1)装置A中反应的化学方程式是
(2)装置B的作用是
(3)装置C中盛放的物质是
(4)装置E用于吸收尾气,E中反应的离子方程式是
(5)漂粉精常用于游泳池的消毒,起消毒作用的是HClO;池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会
②池水酸性过强,会刺激眼睛和皮肤。有时加入
 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】含氯消毒剂、医用酒精、过氧化物等均能有效灭活病毒,为抗击新型冠状肺炎 (COVID-19)作出了贡献。请回答下列问题∶
(1)下列物质用作消毒剂时,原理与其它不同的是___________ (填字母)。
A. NaClO B. ClO2 C. 医用酒精 D. H2O2
(2)兴趣小组欲探究过氧化钠样品是否变质,进行下列操作∶取少量样品,溶解,加入_________ ,振荡,有白色沉淀产生,证明 Na2O2已变质。
(3)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由ClO2与Cl2O按一定比例混合后在NaOH溶液中反应制得。
① NaClO2中氯元素的化合价是___________ 。
② 制备时 Cl2O 与 ClO2完全反应的物质的量理论比为___________ 。
③ 在一定条件下,将Cl2通入填充有固体NaClO2的反应柱内将其氧化为ClO2.当消耗标准状况下 1.12 L Cl2时,可制得 ClO2___________ g。
(4)兴趣小组设计如下图实验装置制取少量漂白液。
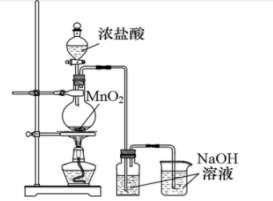
① MnO2与浓 HCl 反应的离子方程式为___________ 。
② 充分反应后,测得漂白液中NaClO质量分数偏低。经分析可能的原因有∶
I.___________ (用文字简述)。
Ⅱ.氯气与NaOH反应放热,温度较高时生成NaClO3,该反应方程式为___________ 。
(1)下列物质用作消毒剂时,原理与其它不同的是
A. NaClO B. ClO2 C. 医用酒精 D. H2O2
(2)兴趣小组欲探究过氧化钠样品是否变质,进行下列操作∶取少量样品,溶解,加入
(3)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可由ClO2与Cl2O按一定比例混合后在NaOH溶液中反应制得。
① NaClO2中氯元素的化合价是
② 制备时 Cl2O 与 ClO2完全反应的物质的量理论比为
③ 在一定条件下,将Cl2通入填充有固体NaClO2的反应柱内将其氧化为ClO2.当消耗标准状况下 1.12 L Cl2时,可制得 ClO2
(4)兴趣小组设计如下图实验装置制取少量漂白液。

① MnO2与浓 HCl 反应的离子方程式为
② 充分反应后,测得漂白液中NaClO质量分数偏低。经分析可能的原因有∶
I.
Ⅱ.氯气与NaOH反应放热,温度较高时生成NaClO3,该反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气,并模拟工业制漂白粉。请回答下列问题:

(1)装置G的名称为___________ 。
(2)图中制氯气的化学方程式___________ 。
(3)从上图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序为(用仪器下方字母表示,如A→B→…)___________ 。
Ⅱ.漂白粉的制备
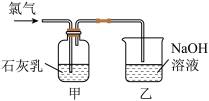
已知:①氯气和石灰乳在反应的过程中会放出热量。
②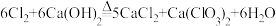
(4)写出制取漂白粉的化学方程式,并用双线桥标注电子转移的方向和数目___________ 。
(5)兴趣小组制得的漂白粉中 的含量远超过预期,而
的含量远超过预期,而 含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)
含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)___________ 。
(6)为提高产品中有效成分 的含量,在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)
的含量,在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)___________ 。
(7)漂粉精常用于游泳池的消毒,起消毒作用的是HClO,其在水中释放HClO的途径如下。
①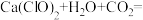
___________ +___________ (把反应补充完整)
②游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投了过氧化氢(H2O2)消毒剂。消毒剂为什么不起作用了?试写出反应的化学方程式:___________ 。

(1)装置G的名称为
(2)图中制氯气的化学方程式
(3)从上图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序为(用仪器下方字母表示,如A→B→…)
Ⅱ.漂白粉的制备

已知:①氯气和石灰乳在反应的过程中会放出热量。
②
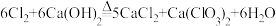
(4)写出制取漂白粉的化学方程式,并用双线桥标注电子转移的方向和数目
(5)兴趣小组制得的漂白粉中
 的含量远超过预期,而
的含量远超过预期,而 含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)
含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)(6)为提高产品中有效成分
 的含量,在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)
的含量,在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)(7)漂粉精常用于游泳池的消毒,起消毒作用的是HClO,其在水中释放HClO的途径如下。
①
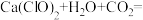
②游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投了过氧化氢(H2O2)消毒剂。消毒剂为什么不起作用了?试写出反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ. 有一瓶澄清溶液,可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl―、I―现进行如下实验:
①测知溶液显强酸性;②取样加少量CCl4和数滴新制氯水,CCl4层为紫红色;
③另取样滴加稀NaOH溶液,使溶液变为碱性,此过程中均无沉淀生成;
④取少量上述碱性溶液,加Na2CO3溶液出现白色沉淀;
⑤将实验③中的碱性溶液加热,有气体放出,该气体能使湿润红色石蕊试纸变蓝。
请回答:(1)原溶液中肯定存在的离子是____________________
(2)不能确定是否存在的离子是____________________
Ⅱ.(1)某兴趣小组同学汲取热电厂附近的雨水进行实验。雨水样品在空气中放置2小时后,通过测定发现雨水样品的酸性会增强,你认为会形成溶液酸性这一变化的原因是(用离子方程式表示)________________________________________________
(2)正常雨水的溶液也是偏酸性,这是因为_____________________________________
(3)该兴趣小组同学为测定空气中二氧化硫的体积分数,做了如下实验:取标准状况下的空气1.000L(内含氮气 、氧气 、二氧化硫、二氧化碳等),慢慢通过足量氯水,(反应的化学方程式为SO2+Cl2+H2O=2HCl+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。计算该空气样品中二氧化硫的体积分数_____________________
①测知溶液显强酸性;②取样加少量CCl4和数滴新制氯水,CCl4层为紫红色;
③另取样滴加稀NaOH溶液,使溶液变为碱性,此过程中均无沉淀生成;
④取少量上述碱性溶液,加Na2CO3溶液出现白色沉淀;
⑤将实验③中的碱性溶液加热,有气体放出,该气体能使湿润红色石蕊试纸变蓝。
请回答:(1)原溶液中肯定存在的离子是
(2)不能确定是否存在的离子是
Ⅱ.(1)某兴趣小组同学汲取热电厂附近的雨水进行实验。雨水样品在空气中放置2小时后,通过测定发现雨水样品的酸性会增强,你认为会形成溶液酸性这一变化的原因是(用离子方程式表示)
(2)正常雨水的溶液也是偏酸性,这是因为
(3)该兴趣小组同学为测定空气中二氧化硫的体积分数,做了如下实验:取标准状况下的空气1.000L(内含氮气 、氧气 、二氧化硫、二氧化碳等),慢慢通过足量氯水,(反应的化学方程式为SO2+Cl2+H2O=2HCl+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。计算该空气样品中二氧化硫的体积分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组为探究 和
和 的性质,按如图所示装置进行实验(省略部分夹持装置)。
的性质,按如图所示装置进行实验(省略部分夹持装置)。
(1)A中发生反应的化学方程式为___________ 。
(2)使用可抽动铜丝的优点是___________ 。
(3)B处的实验现象是___________ ,由此推测硫元素从 价变为
价变为 价。
价。
(4)C处观察到蘸有 溶液的棉花上出现黄色固体,该反应的氧化剂为
溶液的棉花上出现黄色固体,该反应的氧化剂为___________ (填化学式)。
(5)D装置的作用是___________ 。
(6)将A中产生的气体通入 溶液中,生成的白色沉淀为
溶液中,生成的白色沉淀为___________ (填化学式)。
(7)探究 的酸性强于
的酸性强于 ,该小组同学用下图所示装置达成实验目的。
,该小组同学用下图所示装置达成实验目的。
___________ (填标号)。
 和
和 的性质,按如图所示装置进行实验(省略部分夹持装置)。
的性质,按如图所示装置进行实验(省略部分夹持装置)。
(1)A中发生反应的化学方程式为
(2)使用可抽动铜丝的优点是
(3)B处的实验现象是
 价变为
价变为 价。
价。(4)C处观察到蘸有
 溶液的棉花上出现黄色固体,该反应的氧化剂为
溶液的棉花上出现黄色固体,该反应的氧化剂为(5)D装置的作用是
(6)将A中产生的气体通入
 溶液中,生成的白色沉淀为
溶液中,生成的白色沉淀为(7)探究
 的酸性强于
的酸性强于 ,该小组同学用下图所示装置达成实验目的。
,该小组同学用下图所示装置达成实验目的。a.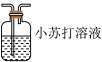 b.
b.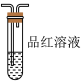 c.
c. d.
d.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】I.实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。
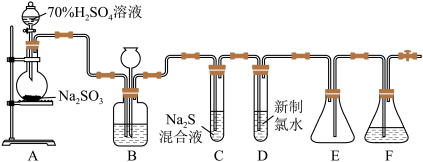
(1)盛装70%H2SO4溶液的仪器名称为____ 。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若____ ,则整个装置气密性良好。
(2)装置B作用之一是通过观察产生气泡多少判断SO2生成的快慢,其中液体最好选择____ 。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为____ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:方案合理的是____ (填“I”“II”或“III”)
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案II:向第二份溶液中加入品红溶液,红色褪去;
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
(5)装置E的作用是_____ 。
II.氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程示意图。

(6)写出氧化炉中的化学反应方程式_____ 。
(7)向吸收塔通入A的作用_____ 。
(8)工业制硝酸的尾气是酸性气体,为防止环境污染,最好选用_____ (填化学式)溶液吸收。

(1)盛装70%H2SO4溶液的仪器名称为
(2)装置B作用之一是通过观察产生气泡多少判断SO2生成的快慢,其中液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:方案合理的是
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案II:向第二份溶液中加入品红溶液,红色褪去;
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
(5)装置E的作用是
II.氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程示意图。

(6)写出氧化炉中的化学反应方程式
(7)向吸收塔通入A的作用
(8)工业制硝酸的尾气是酸性气体,为防止环境污染,最好选用
您最近一年使用:0次
【推荐1】工业碱式砷酸钙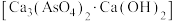 是一种粉红色粉末,难溶于水,可溶于盐酸,主要用于防治地下虫害。工业上以铜冶金烟气净化除砷后得到的硫化砷渣(主要成分
是一种粉红色粉末,难溶于水,可溶于盐酸,主要用于防治地下虫害。工业上以铜冶金烟气净化除砷后得到的硫化砷渣(主要成分 ,含少量FeS、CuS)为原料生产高纯度碱式砷酸钙的工艺流程如下图:
,含少量FeS、CuS)为原料生产高纯度碱式砷酸钙的工艺流程如下图:
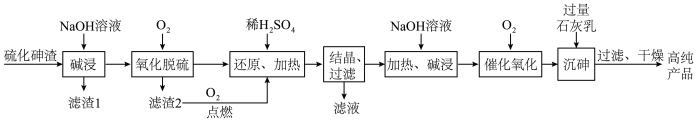
已知: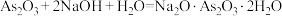
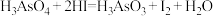
回答下列问题:
(1)碱浸可将 转化为
转化为 、
、 ,滤渣1的主要成分是
,滤渣1的主要成分是_______ (填化学式),“氧化脱硫”生成滤渣2的离子方程式为_______ 。
(2)“还原”反应 被还原为
被还原为 ,则“还原”反应中氧化剂与还原剂的物质的量之比为
,则“还原”反应中氧化剂与还原剂的物质的量之比为_______ ,为检验“还原”反应后的溶液中是否存在 ,应采取的操作方法是
,应采取的操作方法是_______ 。
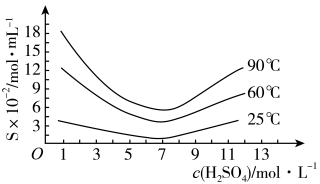
(3)在不同温度和不同浓度硫酸中 的溶解度(S)曲线如图所示。为了提高粗
的溶解度(S)曲线如图所示。为了提高粗 的结晶析出率,在此过程中应控制的条件为
的结晶析出率,在此过程中应控制的条件为_______ 。
(4)“加热碱浸”应控制温度为80℃~90℃和合适的碱度,NaOH与 合理的物质的量之比为
合理的物质的量之比为_______ ,若加入NaOH的量不足带来的不利影响是_______ 。
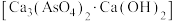 是一种粉红色粉末,难溶于水,可溶于盐酸,主要用于防治地下虫害。工业上以铜冶金烟气净化除砷后得到的硫化砷渣(主要成分
是一种粉红色粉末,难溶于水,可溶于盐酸,主要用于防治地下虫害。工业上以铜冶金烟气净化除砷后得到的硫化砷渣(主要成分 ,含少量FeS、CuS)为原料生产高纯度碱式砷酸钙的工艺流程如下图:
,含少量FeS、CuS)为原料生产高纯度碱式砷酸钙的工艺流程如下图:
已知:
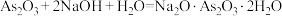
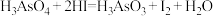
回答下列问题:
(1)碱浸可将
 转化为
转化为 、
、 ,滤渣1的主要成分是
,滤渣1的主要成分是(2)“还原”反应
 被还原为
被还原为 ,则“还原”反应中氧化剂与还原剂的物质的量之比为
,则“还原”反应中氧化剂与还原剂的物质的量之比为 ,应采取的操作方法是
,应采取的操作方法是(3)在不同温度和不同浓度硫酸中
 的溶解度(S)曲线如图所示。为了提高粗
的溶解度(S)曲线如图所示。为了提高粗 的结晶析出率,在此过程中应控制的条件为
的结晶析出率,在此过程中应控制的条件为
(4)“加热碱浸”应控制温度为80℃~90℃和合适的碱度,NaOH与
 合理的物质的量之比为
合理的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如图:

(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90℃时水解生成A的化学方程式为:__ ,“水解”采用90℃而不在室温下进行的原因是___ 。
(2)“酸溶”时,生成气体B的离子方程式为___ 。
(3)“氧化”时反应的离子方程式为___ 。
(4)“除杂”中反应的离子方程式为__ 。
(5)“喷雾干燥”是将需干燥的物料,分散成很细的像雾一样的微粒,与热空气接触,在瞬间将大部分水分除去,使物料中的固体物质干燥成粉末。采用喷雾干燥而不用蒸发可有效防止产品的水解或分解,写出Al(OH)2Cl在较高温度下分解的化学方程式___ 。“喷雾干燥”中将需干燥的物料,分散成很细的微粒的目的是___ 。

(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90℃时水解生成A的化学方程式为:
(2)“酸溶”时,生成气体B的离子方程式为
(3)“氧化”时反应的离子方程式为
(4)“除杂”中反应的离子方程式为
(5)“喷雾干燥”是将需干燥的物料,分散成很细的像雾一样的微粒,与热空气接触,在瞬间将大部分水分除去,使物料中的固体物质干燥成粉末。采用喷雾干燥而不用蒸发可有效防止产品的水解或分解,写出Al(OH)2Cl在较高温度下分解的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硒(Se)和碲(Te)均为第ⅥA族元素,原子序数分别为34、52,它们的单质和化合物在电子、冶金、材料等领域有广阔的发展前景。科研小组以精炼铜的阳极泥为原料(含有CuS、Cu2Se、Cu2Te 和少量金属单质Ag)回收Se、Te并制备胆矾的一种流程如图:
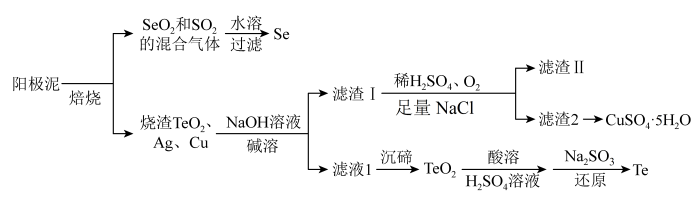
回答下列问题:
(1)Te原子结构示意图为_______ ;TeO2属于_______ (填“酸性”“碱性”或 “两性”)氧化物。Cu2Se中Cu元素的化合价为_______ 。
(2)“水溶”反应的离子方程式为_______ 。
(3)“碱溶”的目的为_______ 。
(4)“分离”过程加入稀H2SO4、O2的作用为_______ ;此步操作需控制适当温度,不宜过高或过低的理由为_______ 。
(5)若滤液2的pH=2,其中c(Cu2+)=0.5 mol·L-1、c(Na+)=0.02 mol·L-1、c(Cl-)=0.01mol·L-1,通过计算说明“分离”过程中_______ (填“能”或“不能”)生成Ag2SO4沉淀[已知Ksp(Ag2SO4)=1.4×10-5、Ksp(AgCl)=1.6×10-10]
(6)用滤液2制备CuSO4·5H2O的操作为_______ 。

回答下列问题:
(1)Te原子结构示意图为
(2)“水溶”反应的离子方程式为
(3)“碱溶”的目的为
(4)“分离”过程加入稀H2SO4、O2的作用为
(5)若滤液2的pH=2,其中c(Cu2+)=0.5 mol·L-1、c(Na+)=0.02 mol·L-1、c(Cl-)=0.01mol·L-1,通过计算说明“分离”过程中
(6)用滤液2制备CuSO4·5H2O的操作为
您最近一年使用:0次



