电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为______________________________ 。
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)______________ (填“>”“<”或“=”)c(CH3COO-)。
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为___________________________________ 。
(4) 25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-) =__________________ 。
| 化学式 | 电离平衡常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为
(4) 25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-) =
更新时间:2017-08-13 06:12:34
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。
(1)草酸( )是一种二元弱酸。写出它在水中的电离方程式:
)是一种二元弱酸。写出它在水中的电离方程式:_______ 。
(2)试比较 草酸溶液中
草酸溶液中 、
、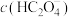 、
、 的大小:
的大小:_______ 。
(3)要使溶液中 的电离程度增大,可以采取的措施是
的电离程度增大,可以采取的措施是_______ 。
(1)草酸(
 )是一种二元弱酸。写出它在水中的电离方程式:
)是一种二元弱酸。写出它在水中的电离方程式:(2)试比较
 草酸溶液中
草酸溶液中 、
、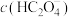 、
、 的大小:
的大小:(3)要使溶液中
 的电离程度增大,可以采取的措施是
的电离程度增大,可以采取的措施是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】水体中的含氮化合物是引起富营养化的主要污染物,分析监测水体中的硝酸(盐)和亚硝酸(盐)含量,控制水体中的含氮污染物,对水资源的循环利用意义重大。
(1)亚硝酸(HNO2)是一种弱酸,其电离方程式为___________ ,其电离平衡常数的表达式为___________ 。
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为___________ 。
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为___________ ,其中氧化产物为___________ (写化学式)。
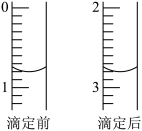
③取20mL含NaNO2的水样,酸化后用0.001mol/L的KI标准溶液滴定(反应中含N的生成物为NO),滴定前和滴定后的滴定管内液面高度如图所示,由此可知水样中NaNO2的浓度为___________ mg/L。
(1)亚硝酸(HNO2)是一种弱酸,其电离方程式为
(2)水体中亚硝酸的含量可以利用KI溶液进行分析测定。该测定反应中,含氮的生成物可以是NO、N2O、NH2OH、NH3等。
①NH2OH中,氮元素的化合价为
②某水样中含有亚硝酸盐,加入少量稀硫酸酸化后,用KI溶液测定,且选用淀粉溶液作指示剂,反应中含N的生成物为NO,反应的离子方程式为
③取20mL含NaNO2的水样,酸化后用0.001mol/L的KI标准溶液滴定(反应中含N的生成物为NO),滴定前和滴定后的滴定管内液面高度如图所示,由此可知水样中NaNO2的浓度为

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】请回答下列问题:
(1)在常温常压下, 完全燃烧生成液态水,放出142.9kJ热量。则
完全燃烧生成液态水,放出142.9kJ热量。则 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
(2)25℃时将 的稀硫酸
的稀硫酸 与
与 的苛性钠溶液
的苛性钠溶液 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则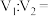
___________ 。
(3)浓度均为 的盐酸和
的盐酸和 溶液各1mL,加入等体积的水稀释后则
溶液各1mL,加入等体积的水稀释后则
___________ 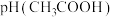 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
(4)根据下表提供的数据,写出往 溶液中通入少量
溶液中通入少量 的离子方程式
的离子方程式___________ 。
(1)在常温常压下,
 完全燃烧生成液态水,放出142.9kJ热量。则
完全燃烧生成液态水,放出142.9kJ热量。则 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)25℃时将
 的稀硫酸
的稀硫酸 与
与 的苛性钠溶液
的苛性钠溶液 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则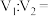
(3)浓度均为
 的盐酸和
的盐酸和 溶液各1mL,加入等体积的水稀释后则
溶液各1mL,加入等体积的水稀释后则
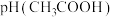 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。(4)根据下表提供的数据,写出往
 溶液中通入少量
溶液中通入少量 的离子方程式
的离子方程式| 化学式 | 电离常数 |
 | 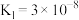 |
 |   |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】结合CH3COOH或NH3·H2O电离方程式,根据平衡移动原理,分析电离平衡状态是如何建立的?电离平衡的特征有哪些?
CH3COOH
___
NH3·H2O
____
CH3COOH

NH3·H2O

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列问题。
(1)某浓度的氨水中存在平衡:NH3·H2O⇌ +OH-。如想增大
+OH-。如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___________ (填字母)。
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
(1)某浓度的氨水中存在平衡:NH3·H2O⇌
 +OH-。如想增大
+OH-。如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】物质A—E都是由下表中的离子组成或生成的,常温下各物质从lmL稀释到1000mL,pH的变化如图l所示,其中A与D反应得到E。请回答:
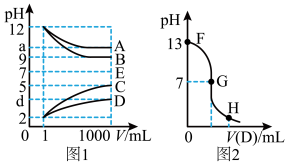
(1)根据图1中各物质的pH变化关系,写出下列物质的化学式:B:___ 。
(2)图l中a>9的理由是___ 。
(3)另取浓度为C1的B溶液25ml,向其中逐滴滴加0.2mol/L的D溶液,滴定过程中溶液pH的变化曲线如图2所示。
①C1为___ 。
②G点溶液呈中性,则加入D溶液的体积V___ (填“>”、“<’’或“=”)12.5mL。
③常温下B、C溶液的pH分别是a、b且a+b=13,则将B、C混合恰好完全反应时所消耗B、C溶液的体积比VB:VC=___ 。
| 阳离子 | NH 、H+、Na+ 、H+、Na+ |
| 阴离子 | OH-、CH3COO-、Cl- |

(1)根据图1中各物质的pH变化关系,写出下列物质的化学式:B:
(2)图l中a>9的理由是
(3)另取浓度为C1的B溶液25ml,向其中逐滴滴加0.2mol/L的D溶液,滴定过程中溶液pH的变化曲线如图2所示。
①C1为
②G点溶液呈中性,则加入D溶液的体积V
③常温下B、C溶液的pH分别是a、b且a+b=13,则将B、C混合恰好完全反应时所消耗B、C溶液的体积比VB:VC=
您最近一年使用:0次



