某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,
已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是__________ 。
(2)该反应中,发生还原反应的过程是_____________________ 。
(3)写出该反应的化学方程式,并用单线桥或双线桥标出电子转移的方向和数目________________________________________________________
(4)若反应转移了0.3mol电子,则产生的气体在标准状况下体积为_______ 。
已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用单线桥或双线桥标出电子转移的方向和数目
(4)若反应转移了0.3mol电子,则产生的气体在标准状况下体积为
更新时间:2017-08-24 17:50:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素化合物在日常生活、化工生产和环境科学中有着重要的用途。
(1)当皮肤划破时可用FeCl3溶液应急止血,用氯化铁固体配制成450 mL 0.1mol·L-1的溶液,配制过程中所需要的玻璃仪器有量筒、玻璃棒、烧杯、______________ 。
(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子______________ (填离子符号)。
(3)高铁酸钾(K2FeO4)是一种既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反Fe(OH)3+ClO-+OH-→FeO +Cl-+H2O(未配平),每生成1 mol K2FeO4,转移的电子数
+Cl-+H2O(未配平),每生成1 mol K2FeO4,转移的电子数________ NA。
(4) 要将纯碱高温熔化,下列坩埚中可选用的是___________ .
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚.
(5)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、NO 、Cl-、SO
、Cl-、SO 中的4种离子,且均为1 mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
中的4种离子,且均为1 mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是____________ 。
(1)当皮肤划破时可用FeCl3溶液应急止血,用氯化铁固体配制成450 mL 0.1mol·L-1的溶液,配制过程中所需要的玻璃仪器有量筒、玻璃棒、烧杯、
(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子
(3)高铁酸钾(K2FeO4)是一种既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反Fe(OH)3+ClO-+OH-→FeO
 +Cl-+H2O(未配平),每生成1 mol K2FeO4,转移的电子数
+Cl-+H2O(未配平),每生成1 mol K2FeO4,转移的电子数(4) 要将纯碱高温熔化,下列坩埚中可选用的是
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚.
(5)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、NO
 、Cl-、SO
、Cl-、SO 中的4种离子,且均为1 mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
中的4种离子,且均为1 mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2↑中(已知:BrF3中F为-1价。):氧化产物是___ ;若生成1个O2分子,则此时反应过程中转移电子数目为___ 个。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求书写下列方程式。
(1)当用 CaSO3 水悬浮液吸收经 O3 预处理的烟气时,清液(pH 约为 8)中 将 NO2转化为
将 NO2转化为 ,其离子方程式为
,其离子方程式为__________________ 。
(2)H3PO2 的工业制法是:将白磷(P4)与 Ba(OH)2 溶液反应生成PH3 气体和Ba(H2PO2)2, 后者再与H2SO4 反应。写出白磷与 Ba(OH)2 溶液反应的化学方程式___________________ 。
(3)在酸性NaClO溶液中,HClO氧化NO生成Cl-和 ,其离子方程式为
,其离子方程式为______________ 。
(4)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:____________________ 。
(5)+6 价铬的化合物毒性较大,常用 NaHSO3 将废液中的 还原成 Cr3+,该反应的离子方程式为
还原成 Cr3+,该反应的离子方程式为_______________________ 。
(1)当用 CaSO3 水悬浮液吸收经 O3 预处理的烟气时,清液(pH 约为 8)中
 将 NO2转化为
将 NO2转化为 ,其离子方程式为
,其离子方程式为(2)H3PO2 的工业制法是:将白磷(P4)与 Ba(OH)2 溶液反应生成PH3 气体和Ba(H2PO2)2, 后者再与H2SO4 反应。写出白磷与 Ba(OH)2 溶液反应的化学方程式
(3)在酸性NaClO溶液中,HClO氧化NO生成Cl-和
 ,其离子方程式为
,其离子方程式为(4)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:
(5)+6 价铬的化合物毒性较大,常用 NaHSO3 将废液中的
 还原成 Cr3+,该反应的离子方程式为
还原成 Cr3+,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.现有下列物质:
①铁、②硫酸溶液、③ 、④熔融的
、④熔融的 、⑤
、⑤ 固体、⑥蔗糖、⑦
固体、⑥蔗糖、⑦ 晶体、⑧氧气、⑨氨水、⑩稀硝酸。
晶体、⑧氧气、⑨氨水、⑩稀硝酸。
(1)上述物质中属于电解质的有___________ (填编号,下同),属于非电解质的有___________ ,能导电的有___________ 。
(2) 电离方程式为
电离方程式为___________ 。
II.利用氧化还原反应原理可处理污水。
(3)高铁酸钠 是一种新型的净水剂,其中一种制备方法如下:
是一种新型的净水剂,其中一种制备方法如下:
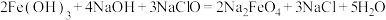 。
。
用单线桥标出该反应电子转移的方向和数目___________ 。
(4)电镀废水中含有剧毒的 (C为
(C为 价),加入
价),加入 溶液处理该碱性废水时生成
溶液处理该碱性废水时生成 、
、 和
和 。该反应的离子方程式为
。该反应的离子方程式为___________ 。
①铁、②硫酸溶液、③
 、④熔融的
、④熔融的 、⑤
、⑤ 固体、⑥蔗糖、⑦
固体、⑥蔗糖、⑦ 晶体、⑧氧气、⑨氨水、⑩稀硝酸。
晶体、⑧氧气、⑨氨水、⑩稀硝酸。(1)上述物质中属于电解质的有
(2)
 电离方程式为
电离方程式为II.利用氧化还原反应原理可处理污水。
(3)高铁酸钠
 是一种新型的净水剂,其中一种制备方法如下:
是一种新型的净水剂,其中一种制备方法如下: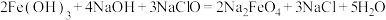 。
。用单线桥标出该反应电子转移的方向和数目
(4)电镀废水中含有剧毒的
 (C为
(C为 价),加入
价),加入 溶液处理该碱性废水时生成
溶液处理该碱性废水时生成 、
、 和
和 。该反应的离子方程式为
。该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫酸是当今世界上最重要的化工产品之一、
(1)《新修本草》中关于“青矾(FeSO4•7H2O)”的描述:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中说:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
①赤色固体可能是___________ (填化学式)。
②为确认“青矾厂气”含有SO2和SO3,将其通入依次以下装置。
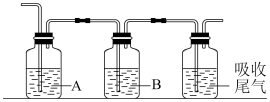
A、B中供选择的试剂有a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 c.浓硫酸
A中溶液为___________ (填标号),可观察到的现象为___________ 。
(2)工业制硫酸主要采用接触法,以黄铁矿(FeS2)为原料制备硫酸的主要设备和流程如图。
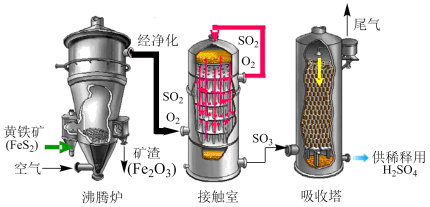
①“沸腾炉”中主要发生的反应为 。每反应消耗1molFeS2,转移的电子数为
。每反应消耗1molFeS2,转移的电子数为___________ 。
②“接触室”中生成SO3的化学方程式为___________ 。
③“吸收塔”中用于吸收SO3的试剂为___________ (填“水”或“浓硫酸”)。
④环保部门为了测定某硫酸厂周围空气中的SO2含量进行了如下实验。取标准状况下1.000L空气(含N2、O2、CO2、SO2),缓慢通过足量碘水。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.233g。则空气样品中SO2的体积分数为___________ 。
(1)《新修本草》中关于“青矾(FeSO4•7H2O)”的描述:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中说:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
①赤色固体可能是
②为确认“青矾厂气”含有SO2和SO3,将其通入依次以下装置。

A、B中供选择的试剂有a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 c.浓硫酸
A中溶液为
(2)工业制硫酸主要采用接触法,以黄铁矿(FeS2)为原料制备硫酸的主要设备和流程如图。

①“沸腾炉”中主要发生的反应为
 。每反应消耗1molFeS2,转移的电子数为
。每反应消耗1molFeS2,转移的电子数为②“接触室”中生成SO3的化学方程式为
③“吸收塔”中用于吸收SO3的试剂为
④环保部门为了测定某硫酸厂周围空气中的SO2含量进行了如下实验。取标准状况下1.000L空气(含N2、O2、CO2、SO2),缓慢通过足量碘水。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.233g。则空气样品中SO2的体积分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
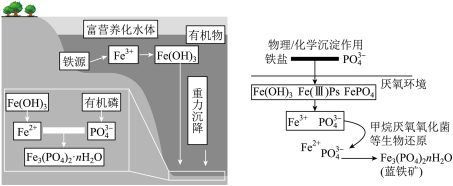
【推荐3】一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元素。因此在污水处理生物污泥中的蓝铁矿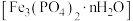 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾( )作为净水消毒剂,发生反应的化学方程式为
)作为净水消毒剂,发生反应的化学方程式为 。
。
① 中Fe的化合价为
中Fe的化合价为_______ 价,上述反应涉及的物质中属于盐的是_______ 。
②高铁酸钾可用于净水消毒的原因是_______
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:_______ 。
_______ _______
_______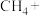 _______
_______ _______
_______ _______
_______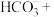 _______
_______
该反应中的氧化产物为_______ (填离子符号),被氧化的原子与被还原的原子的数目之比为_______ 。
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解: ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=_______ 。
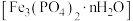 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾(
 )作为净水消毒剂,发生反应的化学方程式为
)作为净水消毒剂,发生反应的化学方程式为 。
。①
 中Fe的化合价为
中Fe的化合价为②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:
_______
 _______
_______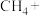 _______
_______ _______
_______ _______
_______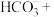 _______
_______
该反应中的氧化产物为
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:
 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我们知道,电解质在溶液中的反应实质是离子之间的反应。通常,离子反应有两种情况,一种是没有电子转移的,是离子互换反应;另一种是有电子转移的,属于氧化还原反应。
在溶液中发生的离子互换反应一般总是向离子浓度减小的方向进行。取4mL1mol·L-1醋酸溶液在试管中,逐滴滴入1mL1mol·L-1碳酸钠溶液。
(1)写出该反应的离子方程式______________ 。
随着碳酸钠溶液的滴加,溶液的pH___________ (填“增大”、“减小”或“不变”)。
(2)这一离子互换反应是否向离子浓度减小方向进行?请应用平衡移动原理进行说明。___________ 。
(3)当碳酸钠溶液全部滴加完后,测得该溶液显酸性,比较该溶液中除H2O以外的微粒浓度大小(不考虑CO2的溶解)_____________________ 。
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO +4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
+4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
(4)写出并配平该氧化还原反应的离子方程式,用单线桥法标出电子转移方向和数目。_________ 。
在溶液中发生的离子互换反应一般总是向离子浓度减小的方向进行。取4mL1mol·L-1醋酸溶液在试管中,逐滴滴入1mL1mol·L-1碳酸钠溶液。
(1)写出该反应的离子方程式
随着碳酸钠溶液的滴加,溶液的pH
(2)这一离子互换反应是否向离子浓度减小方向进行?请应用平衡移动原理进行说明。
(3)当碳酸钠溶液全部滴加完后,测得该溶液显酸性,比较该溶液中除H2O以外的微粒浓度大小(不考虑CO2的溶解)
氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO
 +4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。
+4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质能使上述还原过程发生。(4)写出并配平该氧化还原反应的离子方程式,用单线桥法标出电子转移方向和数目。
您最近一年使用:0次
【推荐2】过氧化氢(H2O2)俗名双氧水,医疗上利用它杀菌消毒的作用来清洗伤口。根据下列反应回答问题:
A.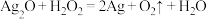
B.
C.
(1)上述三个反应中H2O2分别表现什么性质:
A:_______ ,B:_______ ,C:_______ 。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序_______ 。
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为_______ 。
A.
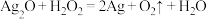
B.

C.

(1)上述三个反应中H2O2分别表现什么性质:
A:
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序
(3)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、
 、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为
、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。写出该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)NaClO中Cl的化合价为_______ ,NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的“84”消毒剂的有效成分。工业上将Cl2溶于一定浓度的NaOH溶液,可制得“84”消毒液,反应的离子方程式为_______ 。
(2)某届奥运会期间,由于工作人员将84消毒液(有效成分NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO_______  的(填“>”或“<);当参加反应的NaClO和
的(填“>”或“<);当参加反应的NaClO和 分子的物质的量比为1:1时,该反应的还原产物为
分子的物质的量比为1:1时,该反应的还原产物为_______ (填字母序号)。
A. B.
B. C.
C. D.NaCl E.NaClO F.
D.NaCl E.NaClO F.
 在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂。实验室可用如图所示装置制备
在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂。实验室可用如图所示装置制备 (夹持装置略)。
(夹持装置略)。
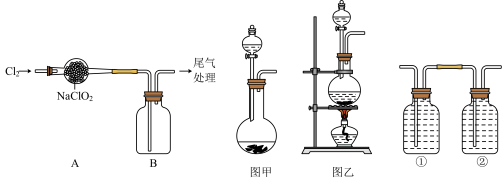
(3)某同学利用一定浓度的盐酸和MnO2制备Cl2,选择_______ (填“图甲”“图乙”),发生反应的离子方程式为_______ 。制备得到的氯气依次通入①和②中进行净化后通入A中,①和②中的试剂分别为_______ 、_______ 。
(4)在用ClO2进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+,生成 和MnO2的离子方程式为
和MnO2的离子方程式为_______ 。
(1)NaClO中Cl的化合价为
(2)某届奥运会期间,由于工作人员将84消毒液(有效成分NaClO)与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与
 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:NaClO
促进藻类快速生长。该反应说明氧化性:NaClO 的(填“>”或“<);当参加反应的NaClO和
的(填“>”或“<);当参加反应的NaClO和 分子的物质的量比为1:1时,该反应的还原产物为
分子的物质的量比为1:1时,该反应的还原产物为A.
 B.
B. C.
C. D.NaCl E.NaClO F.
D.NaCl E.NaClO F.
 在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂。实验室可用如图所示装置制备
在常温下为黄色气体,熔点为-59.5℃,沸点为11℃,易溶于水,其水溶液是一种广谱杀菌剂。实验室可用如图所示装置制备 (夹持装置略)。
(夹持装置略)。
(3)某同学利用一定浓度的盐酸和MnO2制备Cl2,选择
(4)在用ClO2进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+,生成
 和MnO2的离子方程式为
和MnO2的离子方程式为
您最近一年使用:0次



