决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
A通常显_____ 价,A的电负性_______ B的电负性(填“>”、“<”或“=”)。
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(已知3种离子晶体的晶格能数据如下表:
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:_________________ 。
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有________________ 个。
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是______________ 。
(4)某配合物的分子结构如图所示,其分子内不含有__________ (填序号)。
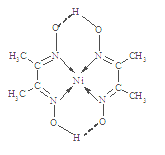
A.离子键 B.极性键 C.金属键 D.配位键 E.氢键 F.非极性键
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A通常显
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(已知3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(4)某配合物的分子结构如图所示,其分子内不含有

A.离子键 B.极性键 C.金属键 D.配位键 E.氢键 F.非极性键
更新时间:2017-09-25 23:53:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】完成下列问题
(1)元素Mn与Fe的部分电离能数据如下表所示:
根据表中数据可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此,你的解释是
再失去1个电子难,对此,你的解释是___________ 。
(2)已知18g葡萄糖固体在人体组织中被O2完全氧化为CO2气体和液态水,能产生280kJ热量。写出该反应的热化学方程式___________ 。
(1)元素Mn与Fe的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
| 电离能/(kJ/mol) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此,你的解释是
再失去1个电子难,对此,你的解释是(2)已知18g葡萄糖固体在人体组织中被O2完全氧化为CO2气体和液态水,能产生280kJ热量。写出该反应的热化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有核电荷数小于18的元素A,其电离能数据如表所示[I1表示失去第1个电子的电离能,In(n=2,3,4,5,6,7,8,9,10,11)表示失去第n个电子的电离能,单位为eV]。
(1)外层电子离核越远,能量越高,电离能越________ (填“大”或“小”);阳离子电荷数越多,在失去电子时,电离能越_______ (填“大”或“小”)。
(2)上述11个电子分属_______ 个电子层。
(3)去掉11个电子后,该元素还有_______ 个电子。
(4)该元素的最高价氧化物对应的水化物的化学式是_______ 。
| 符号 | I1 | I2 | I3 | I4 | I5 | I6 |
| 电离能 | 7.64 | 15.03 | 80.12 | 109.3 | 141.2 | 186.5 |
| 符号 | I7 | I8 | I9 | I10 | I11 | |
| 电离能 | 224.9 | 226.0 | 327.9 | 367.4 | 1 761 |
(1)外层电子离核越远,能量越高,电离能越
(2)上述11个电子分属
(3)去掉11个电子后,该元素还有
(4)该元素的最高价氧化物对应的水化物的化学式是
您最近半年使用:0次
【推荐3】地球上的元素大多数是金属,Na、Mg、Al是常见的主族金属元素,Fe和Cu是常见的过渡金属元素。它们在化学中占有极其重要的地位。
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为___________
②金属钠原子的堆积方式是体心立方,其配位数为___________
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈___________ 色的物质是水合铜离子,请写出它的结构简式,并标明其中配位键___________
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式___________
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有___________ molσ键。
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:___________ (要求:仅写1个总的离子方程式)
(1)①Na、Mg、Al三种元素第一电离能由大到小的顺序为
②金属钠原子的堆积方式是体心立方,其配位数为
(2)选修三课本第42页实验2-2:向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
①硫酸铜溶液中呈
②请写出难溶物溶解得到深蓝色的透明溶液的离子方程式
③结构测定的实验证明,无论在氨水溶液中还是在晶体中,深蓝色都是由于存在某种离子,1mol该离子含有
(3)写出少量Na2O2与氯化铁溶液反应的离子反应方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】从金矿石提炼黄金往往采用氰化法提金。用稀的氰化钠溶液处理粉碎的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的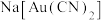 ,这与钢铁的电化学腐蚀相似,其反应方程式为
,这与钢铁的电化学腐蚀相似,其反应方程式为 ,最后再用Zn将
,最后再用Zn将 置换成金单质。
置换成金单质。
(1)下列关于氰化法说法不正确的是___________(复选)
(2)NaCN的电子式为___________ 。
(3)在空气中用氰化钠溶液提取金的正极反应式为 ,则负极反应式为
,则负极反应式为___________ 。
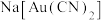 ,这与钢铁的电化学腐蚀相似,其反应方程式为
,这与钢铁的电化学腐蚀相似,其反应方程式为 ,最后再用Zn将
,最后再用Zn将 置换成金单质。
置换成金单质。(1)下列关于氰化法说法不正确的是___________(复选)
| A.Au是一种活泼金属 |
B.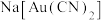 中存在离子键、配位键和非极性共价键 中存在离子键、配位键和非极性共价键 |
C.若无NaCN作用,Au难被 氧化 氧化 |
| D.氰化法的废液直接排放会带来环境污染问题 |
(3)在空气中用氰化钠溶液提取金的正极反应式为
 ,则负极反应式为
,则负极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,振荡;然后在此碘水溶液中加入约1 mL四氯化碳,振荡试管;再向试管里加入1 mL浓碘化钾水溶液,振荡试管,此时现象为___________ ,原因是___________ (写出相应的离子方程式)。
(2)向盛有少量氯化钠溶液的试管中滴入少量硝酸银溶液,生成白色的氯化银沉淀,继续向试管里加入氨水,沉淀溶解了,试写出沉淀溶解的化学方程式_____
(3)向盛有氯化铁溶液的试管中滴加1滴KSCN溶液,写出相应的离子方程式_____
(4)向硫酸铜水溶液中逐滴加入足量氨水,发现先生成蓝色沉淀,然后沉淀溶解,写出沉淀溶解的离子方程式为___________ 。向硫酸铜溶液中加入过量的NaOH溶液可生成 ,不考虑空间构型,
,不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为_____
(1)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,振荡;然后在此碘水溶液中加入约1 mL四氯化碳,振荡试管;再向试管里加入1 mL浓碘化钾水溶液,振荡试管,此时现象为
(2)向盛有少量氯化钠溶液的试管中滴入少量硝酸银溶液,生成白色的氯化银沉淀,继续向试管里加入氨水,沉淀溶解了,试写出沉淀溶解的化学方程式
(3)向盛有氯化铁溶液的试管中滴加1滴KSCN溶液,写出相应的离子方程式
(4)向硫酸铜水溶液中逐滴加入足量氨水,发现先生成蓝色沉淀,然后沉淀溶解,写出沉淀溶解的离子方程式为
 ,不考虑空间构型,
,不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】工业上常利用铜萃取剂,使溶液中的Cu2+富集进入有机相,再经过进一步的反萃取实现金属铜的沉积、再生,铜萃取剂富集Cu2+的原理如下:
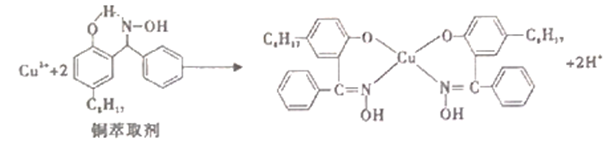
(1)基态铜原子所失去的第一个电子所占据的能层符号是______ , 价铜离 子的简化电子排布式为_________ 。
(2)铜萃取剂中所含 元素的电负性由大到小顺序为______ ,N原子以_____ 杂化轨道与O原子形成σ键。
(3)铜萃取剂与 Cu2+形成的配合物在水相的溶解度______ 有机相的溶解度(填“>”、“<”、“=”),该配合物晶体类型为_____ 。
(4)某学生用硫酸铜溶液与氨水做了一组实 验:CuSO4溶液 蓝色沉淀
蓝色沉淀 沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式_________ ;沉淀溶解后溶液中的阳离子内存在的化学键类型有________ 。
(5)铜的一种氯化物的晶胞如图所示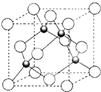 ,该氯化物的化学式
,该氯化物的化学式_____ ,Cu 和Cl之间最短距离为460.0pm,则晶体密度为______ g/cm3。(列式表示)

(1)基态铜原子所失去的第一个电子所占据的能层符号是
(2)铜萃取剂中所含 元素的电负性由大到小顺序为
(3)铜萃取剂与 Cu2+形成的配合物在水相的溶解度
(4)某学生用硫酸铜溶液与氨水做了一组实 验:CuSO4溶液
 蓝色沉淀
蓝色沉淀 沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式
沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式(5)铜的一种氯化物的晶胞如图所示
 ,该氯化物的化学式
,该氯化物的化学式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有几组物质的熔点(℃)的数据:

据此回答下列问题:
(1)A组属于___________ 晶体,其熔化时克服的微粒间的作用力是__________________ 。
(2)B组晶体共同的物理性质是___________________ (填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于_______________________________________ 。
(4)D组晶体可能具有的性质是_________________ (填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因解释为_______________________________ 。

据此回答下列问题:
(1)A组属于
(2)B组晶体共同的物理性质是
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于
(4)D组晶体可能具有的性质是
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体的熔点由高到低的顺序为NaCl>KCl>RbCl>CsCl,其原因解释为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钾和碘是人体内的必需元素,两者的化合物也有着广泛的应用。回答下列问题:
(1)某化合物的晶胞结构如图所示,该晶胞的边长为a。
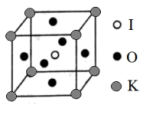
则该晶体的化学式为___ ,K与Ⅰ间的最短距离为___ (用a表示),与Ⅰ紧邻的O个数为__ 。
(2)该晶胞结构的另一种表示中,Ⅰ处于各顶角位置,则K处于__ 位置,O处于__ 位置。
(3)碳元素的单质有多种形式,如图依次是C60、石墨和金刚石的结构图:

回答下列问题:
①上述三种单质互称为___ 。
②在石墨晶体中,碳原子数与共价键数之比为___ 。
③上述三种晶体的熔点由高到低的顺序为___ ,解释原因__ 。
(1)某化合物的晶胞结构如图所示,该晶胞的边长为a。

则该晶体的化学式为
(2)该晶胞结构的另一种表示中,Ⅰ处于各顶角位置,则K处于
(3)碳元素的单质有多种形式,如图依次是C60、石墨和金刚石的结构图:

回答下列问题:
①上述三种单质互称为
②在石墨晶体中,碳原子数与共价键数之比为
③上述三种晶体的熔点由高到低的顺序为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】正交硫和单斜硫是硫元素的两种常见单质,其晶状结构如左下图所示;构成晶体的微粒均是S8分子,其分子结构如右下图所示。回答下列问题:
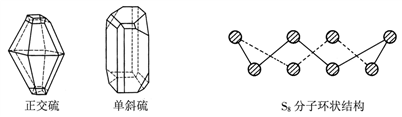
(1)正交硫和单斜硫互称为硫元素的________________ 。
(2)S8分子中,硫原子之间形成的化学键是_____ (填“离子键”或“共价键”)。
(3)已知正交硫的熔点为112.8 ℃,沸点为444.6 ℃,硬度较小。晶状的正交硫是________ 晶体,构成晶体的微粒间的相互作用力是___________________ 。
(4)已知:S8(正交) =S8(单斜) ΔH=+2.64 kJ·molˉ1。正交硫与单斜硫相比,相对比较稳定的是_______________ 。正交硫转化为单斜硫时,发生________ (填“物理变化”或“化学变化”)。
(5)已知通常状况下4g 硫粉完全燃烧放出37 kJ的热量,写出该反应的热化学方程式___________________________________________________ 。

(1)正交硫和单斜硫互称为硫元素的
(2)S8分子中,硫原子之间形成的化学键是
(3)已知正交硫的熔点为112.8 ℃,沸点为444.6 ℃,硬度较小。晶状的正交硫是
(4)已知:S8(正交) =S8(单斜) ΔH=+2.64 kJ·molˉ1。正交硫与单斜硫相比,相对比较稳定的是
(5)已知通常状况下4g 硫粉完全燃烧放出37 kJ的热量,写出该反应的热化学方程式
您最近半年使用:0次



