为了除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,然后进行下列五项操作:
①过滤 ②加过量NaOH溶液 ③加适量HCl ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
通过教材中“粗盐的提纯”及你做过的该实验回答下列问题:
(1)以上五步操作中,最后进行的是________ 。
(2)实验室进行NaCl溶液的蒸发时,一般有以下操作过程:
①固定铁圈位置 ②放置酒精灯 ③放上蒸发皿(蒸发皿中盛有NaCl溶液) ④加热搅拌 ⑤停止加热
正确的操作顺序为___________________ 。
(3)在粗盐经过一系列操作后的溶液中滴加过量饱和Na2CO3溶液。请问这步操作的目的是___________________________________________ 。判断Na2CO3溶液已经过量的方法是_________________________________________________________________ 。
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:_________________________________________ 。
过滤时:_________________________________________ 。
蒸发时:_________________________________________ 。
①过滤 ②加过量NaOH溶液 ③加适量HCl ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
通过教材中“粗盐的提纯”及你做过的该实验回答下列问题:
(1)以上五步操作中,最后进行的是
(2)实验室进行NaCl溶液的蒸发时,一般有以下操作过程:
①固定铁圈位置 ②放置酒精灯 ③放上蒸发皿(蒸发皿中盛有NaCl溶液) ④加热搅拌 ⑤停止加热
正确的操作顺序为
(3)在粗盐经过一系列操作后的溶液中滴加过量饱和Na2CO3溶液。请问这步操作的目的是
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:
过滤时:
蒸发时:
17-18高一上·湖北宜昌·阶段练习 查看更多[3]
湖北省宜昌市金东方高级中学2017-2018学年高一9月月考化学试题(已下线)2019年8月21日《每日一题》必修1 ——粗盐的提纯河南省周口中英文学校2019-2020学年高一上学期第一次月考化学试题
更新时间:2017-10-11 22:33:44
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】以FeSO4溶液为主要原料制取废水处理剂FeOOH,其流程如下:
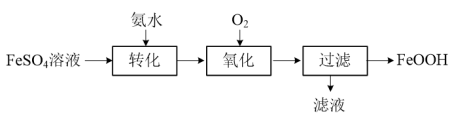
(1)检验FeSO4溶液是否被氧化可选用的试剂是_______ (填化学式)。“转化”时适量氨水将Fe2+部分转化为Fe(OH)2,每生成1 mol Fe(OH)2,理论上参加该反应的NH3·H2O的物质的量为_______ mol。
(2)“氧化”时以一定流速向所得固液混合物中通入O2,反应生成FeOOH。过程中溶液的pH随时间的变化情况如图所示:

已知:pH =-lg c(H+) 。
①0~t1时,Fe(OH)2转化为FeOOH时发生反应的化学方程式为_______ 。
②t1~t2时,FeOOH继续增加,溶液pH减小,原因是_______ (用离子方程式表示)。
(3)通过下列方法测定产品中FeOOH的质量分数:准确称取2.000 g产品,加适量盐酸溶解,再加入适量SnCl2溶液,发生反应2Fe3+ + Sn2+ = 2Fe2+ + Sn4+;除去过量的SnCl2,再向其中加入0.1000 mol·L−1 K2Cr2O7溶液至反应恰好完全,发生反应Cr2O + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,消耗K2Cr2O7溶液36.00 mL。计算该产品中FeOOH的质量分数(写出计算过程)
+ 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,消耗K2Cr2O7溶液36.00 mL。计算该产品中FeOOH的质量分数(写出计算过程) _______ 。

(1)检验FeSO4溶液是否被氧化可选用的试剂是
(2)“氧化”时以一定流速向所得固液混合物中通入O2,反应生成FeOOH。过程中溶液的pH随时间的变化情况如图所示:

已知:pH =-lg c(H+) 。
①0~t1时,Fe(OH)2转化为FeOOH时发生反应的化学方程式为
②t1~t2时,FeOOH继续增加,溶液pH减小,原因是
(3)通过下列方法测定产品中FeOOH的质量分数:准确称取2.000 g产品,加适量盐酸溶解,再加入适量SnCl2溶液,发生反应2Fe3+ + Sn2+ = 2Fe2+ + Sn4+;除去过量的SnCl2,再向其中加入0.1000 mol·L−1 K2Cr2O7溶液至反应恰好完全,发生反应Cr2O
 + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,消耗K2Cr2O7溶液36.00 mL。计算该产品中FeOOH的质量分数(写出计算过程)
+ 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O,消耗K2Cr2O7溶液36.00 mL。计算该产品中FeOOH的质量分数(写出计算过程)
您最近一年使用:0次
【推荐2】硼及其化合物在工业、医药、农业等部门有许多用途。某工厂以铁硼精矿(主要成分为B2O3·2MgO,还有SiO2、CaO、FeO等杂质)制取制硼酸、金属镁的工艺流程图为:
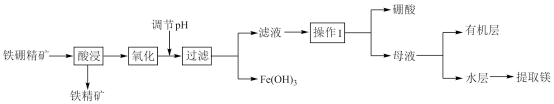
已知:硼酸在不同温度下的溶解度:
回答下列问题:
(1)使用盐酸酸浸,过程中主要反应的化学方程式为_________ ,为提高浸出速率,可采取的措施有_________ (写出两条)。
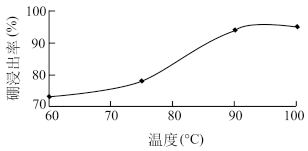
(2)酸浸时,温度与硼浸出率的关系如图所示,则合适的酸浸温度为_________ 。
(3)浸出液“氧化”的是将溶液中的Fe2+用_______ 试剂氧化为Fe3+,反应的离子方程式为_________ 。
(4)从滤液中获得H3BO3晶体的“操作I”具体操作是_________ 。
(5)向滤液中加入有机萃取剂萃取分液,此时硼酸处于_________ 层中(填“有机”或“无机”)。实验室模拟萃取操作使用的玻璃仪器除烧杯外,另一主要玻璃仪器是_________ 。
(6)某工厂用 m1 kg的铁硼精矿制备硼酸,得到纯度为99.8%的硼酸m2 kg,则铁硼精矿中硼的质量分数是__________ (列式表达)。

已知:硼酸在不同温度下的溶解度:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度(g/100g水) | 3 | 3 | 5 | 7 | 9 | 11 | 15 | 18 | 23 | 29 |
(1)使用盐酸酸浸,过程中主要反应的化学方程式为
(2)酸浸时,温度与硼浸出率的关系如图所示,则合适的酸浸温度为

(3)浸出液“氧化”的是将溶液中的Fe2+用
(4)从滤液中获得H3BO3晶体的“操作I”具体操作是
(5)向滤液中加入有机萃取剂萃取分液,此时硼酸处于
(6)某工厂用 m1 kg的铁硼精矿制备硼酸,得到纯度为99.8%的硼酸m2 kg,则铁硼精矿中硼的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如图:

已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110∼120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为________________________________________ 。
(2)加入碳酸钠调节pH至a,a的范围是________________________ ;
(3)操作Ⅰ包含3个基本实验操作,它们是_______ 、__________ 和过滤。
(4)制得的CoCl2·6H2O需减压烘干的原因是______________________ 。
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是_______________________ 。
(6)在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,通常先将产品溶解于乙醚中,除去不溶性杂质后,再进行___________________________________ 。

已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110∼120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为
(2)加入碳酸钠调节pH至a,a的范围是
(3)操作Ⅰ包含3个基本实验操作,它们是
(4)制得的CoCl2·6H2O需减压烘干的原因是
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
(6)在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,通常先将产品溶解于乙醚中,除去不溶性杂质后,再进行
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】钛有强度高和质地轻的优点,广泛应用于飞机制造业等。工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备钛金属,工业流程如下:(已知: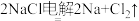 )
)

(1)请写出FeTiO3与稀盐酸反应的离子方程式:________________ 。
(2)请写出“熔融氧化”的化学方程式:_______________________ 。
(3)补充写出实现上述方框内过程A所需的实验操作:___________ 、__________ 过滤、洗涤、在干燥的HCl气流中加热→FeCl2固体
(4)热还原法中能否改用钠代替镁作还原剂:_____________ (填“能”或“不能”);
(5)上流程中可循环利用的物质为:____________________ (填化学式)。
 )
)
(1)请写出FeTiO3与稀盐酸反应的离子方程式:
(2)请写出“熔融氧化”的化学方程式:
(3)补充写出实现上述方框内过程A所需的实验操作:
(4)热还原法中能否改用钠代替镁作还原剂:
(5)上流程中可循环利用的物质为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】根据如图所示实验装置,回答下列问题:

(1)写出下列仪器的名称:①___________ ,②___________ ,③___________ ,⑦___________ 。
(2)上述仪器中实验之前需检查装置是否会漏水的有___________ (填仪器名称)。
(3)利用装置Ⅰ制备蒸馏水时,冷凝水应从___________ (填“f”或“g”)口进入。
(4)利用装置Ⅱ从碘水中萃取碘,可选择的萃取剂为___________ (填“酒精”或“汽油”)
(5)装置Ⅲ有一处明显的错误是___________ 。
(6)利用装置Ⅳ进行实验时,应注意的操作事项有___________ 。

(1)写出下列仪器的名称:①
(2)上述仪器中实验之前需检查装置是否会漏水的有
(3)利用装置Ⅰ制备蒸馏水时,冷凝水应从
(4)利用装置Ⅱ从碘水中萃取碘,可选择的萃取剂为
(5)装置Ⅲ有一处明显的错误是
(6)利用装置Ⅳ进行实验时,应注意的操作事项有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为除去粗盐中的MgCl2、CaCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
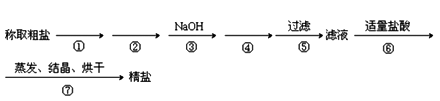
(1)第①步操作的名称是_____________ ,第②步加入的试剂化学式为______________ 。
(2)第④步加入试剂的化学式为___________________ ,相关的化学反应的离子方程式是____________________ 、____________________ 。
(3)第⑤步操作所需玻璃仪器是:烧杯、玻璃棒和__________ (填名称)。
(4)实验过程中多次用到玻璃棒,其作用分别为①________ ;⑤____________ ;⑦____________ 、_____________ 。

(1)第①步操作的名称是
(2)第④步加入试剂的化学式为
(3)第⑤步操作所需玻璃仪器是:烧杯、玻璃棒和
(4)实验过程中多次用到玻璃棒,其作用分别为①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】海藻中富含碘元素。某小组同学在实验室里用灼烧海藻的灰分提取碘,流程如下图。
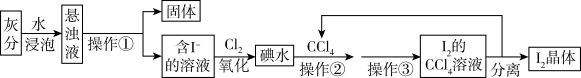
(1)写出操作名称:操作①__________ ,操作③________ 。
(2)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件:3I2+6NaOH=5NaI+NaIO3+3H2O,
酸性条件:5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+3H2O。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的________ (填仪器名称)中加入少量1mol·L-1 NaOH溶液;
②振荡至溶液的_________ 色消失,静置、分层,则_______ (填“上”、“下”)层为CCl4;
③将含碘的碱溶液从仪器的_________ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1 mol·L-1 H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(3)本实验中可以循环利用的物质是___________________________ 。

(1)写出操作名称:操作①
(2)用NaOH浓溶液反萃取后再加稀酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件:3I2+6NaOH=5NaI+NaIO3+3H2O,
酸性条件:5NaI+NaIO3+3H2SO4=3Na2SO4+3I2+3H2O。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的
②振荡至溶液的
③将含碘的碱溶液从仪器的
④边搅拌边加入几滴1 mol·L-1 H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体;
(3)本实验中可以循环利用的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某化学小组对当地化工厂排出的废水成分进行研究,经检测其中含有大量 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。

回答下列问题:
(1)经检测,该废水呈酸性,用石蕊试纸检验该溶液酸碱性的方法是_____ 。
(2)试剂X是_____ ;加入试剂X发生反应的离子方程式为_____ 。
(3)试剂Y是_____ ;白色固体的成分是_____ (填化学式)。
(4)向“溶液b”中加入盐酸的作用是_____ 。
(5)下列有关“操作Ⅰ”的说法错误的是_____(填标号)。
 、
、 、
、 、
、 、
、 。除去废水样品中的
。除去废水样品中的 和
和 ,回收NaCl、
,回收NaCl、 的实验流程如下。
的实验流程如下。
回答下列问题:
(1)经检测,该废水呈酸性,用石蕊试纸检验该溶液酸碱性的方法是
(2)试剂X是
(3)试剂Y是
(4)向“溶液b”中加入盐酸的作用是
(5)下列有关“操作Ⅰ”的说法错误的是_____(填标号)。
| A.需要的玻璃仪器有烧杯、漏斗和玻璃棒 |
| B.用“操作Ⅰ”装置可以除去粗盐中的不溶性杂质 |
| C.为加快“操作Ⅰ”速度,可用玻璃棒搅拌 |
| D.若溶液a仍浑浊,需重复进行“操作Ⅰ” |
您最近一年使用:0次


 已除尽的方法是:
已除尽的方法是:

