工业上用某种氧化铝矿石(含Fe2O3杂质)为原料冶炼铝的工艺流程如图:对上述流程中的判断正确的是
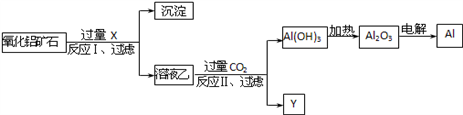

| A.试剂X可以为氨水,沉淀中含有铁的化合物 |
| B.CO2可以用H2SO4溶液或稀盐酸代替 |
| C.工业上还可采用Fe还原Al2O3的方法制Al,成本更低 |
| D.反应II中的反应为:CO2+AlO2-+2H2O=Al(OH)3↓+HCO3- |
17-18高三上·甘肃白银·阶段练习 查看更多[3]
甘肃省白银市会宁县第一中学2018届高三上学期第二次月考理科综合化学试题河南省信阳市罗山县2021届高三第一次调研(8月联考)化学试题(已下线)小题必刷16 金属元素为载体的化工流程选择题——2021年高考化学一轮复习小题必刷(通用版)
更新时间:2017-10-21 18:11:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于金属冶炼的说法正确的是
| A.由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al |
| B.可以用钠加入氯化镁饱和溶液中制取镁 |
| C.炼铁高炉中所发生的反应都是放热的,故无需加热 |
| D.金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 A、B、C、D是原子序数依次增大的前四周期元素,A 元素原子最高能级的不同轨道都有电子且自旋方向相同; B元素原子的价层电子排布式是 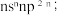 其中C元素的部分电离能如下表; 含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法正确的是
其中C元素的部分电离能如下表; 含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法正确的是
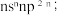 其中C元素的部分电离能如下表; 含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法正确的是
其中C元素的部分电离能如下表; 含D元素的化合物焰色试验火焰呈紫色(透过蓝色钴玻璃)。下列说法正确的是| 元素 | 电离能(kJ·mol ) | |||
I | I₂ | I₃ | I₄ | |
| C | 578 | 1817 | 2745 | 11575 |
| A.离子半径大小:C>A>B |
| B.工业上可以用热还原法冶炼C |
| C.化合物DB3中只含有离子 |
| D.元素 D的核外电子运动具有10种不同的空间运动状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
A. 溶液( 溶液( ):通入过量的 ):通入过量的 |
B.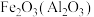 :加入NaOH溶液再过滤 :加入NaOH溶液再过滤 |
C. 溶液( 溶液( ):加入足量铁粉再过滤 ):加入足量铁粉再过滤 |
D. :将气体通过盛有饱和 :将气体通过盛有饱和 溶液的洗气瓶 溶液的洗气瓶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用相同的铝片、6mol/L稀盐酸、3mol/L稀硫酸、6mol/L氢氧化钠溶液分别进行以下实验:
对上述实验的相关说法不正确的是
| 实验方案 | 实验现象 |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,有少量气泡产生 |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大气泡产生 |
A.刚开始无现象是因为铝片表面的 在反应,说明 在反应,说明 是一种碱性氧化物 是一种碱性氧化物 |
B.对比实验(1)、(2)的酸的浓度,是为了消除 浓度对反应体系的影响 浓度对反应体系的影响 |
C.对比实验(1)、(2)后来产生气泡的现象,可得出: 对Al与 对Al与 的反应可能有阻碍作用 的反应可能有阻碍作用 |
D.对比三个实验产生的现象和酸碱挥发性可推知:上述方案中实验(3)最适宜于实验室制备 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组在实验室中利用菱镁矿设计制备氧化镁的流程如下。已知菱镁矿主要成分为 ,含有少量
,含有少量 和难溶性杂质。下列说法错误的是
和难溶性杂质。下列说法错误的是

 ,含有少量
,含有少量 和难溶性杂质。下列说法错误的是
和难溶性杂质。下列说法错误的是
| A.步骤(1)前需将菱镁矿粉碎,以提高原料利用率 |
| B.步骤(1)和步骤(2)中要用到的玻璃仪器有漏斗、玻璃棒、烧杯 |
C.步骤(2)中获得 沉淀,说明 沉淀,说明 不与NaOH溶液反应。 不与NaOH溶液反应。 |
| D.步骤(3)中需使用到坩埚等仪器 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】NH4Al(SO4)2·12H2O俗称铵明矾,其性质稳定,是化学实验常用的基准试剂,借助碳酸氢铵与硫酸钠可以制备纯净的铵明矾,制备过程如图,下列说法不正确 的是( )
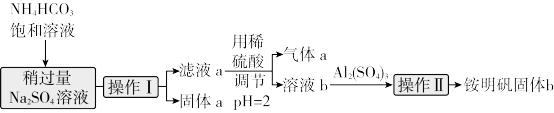

| A.操作I中用到的玻璃仪器有漏斗、烧杯、玻璃棒 |
| B.操作Ⅱ的基本过程为蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| C.滤液a中加稀硫酸调节pH=2的目的是抑制NH4+的水解 |
| D.若气体a通入到饱和的纯碱溶液中会有晶体析出,该晶体与固体a相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氨基甲酸铵(H2NCOONH4)是一种氨化剂,易水解,难溶于CCl4。某小组设计下图所示装置制备氨基甲酸铵。已知:2NH3(g) + CO2(g) H2NCOONH4(s) H<0。
H2NCOONH4(s) H<0。
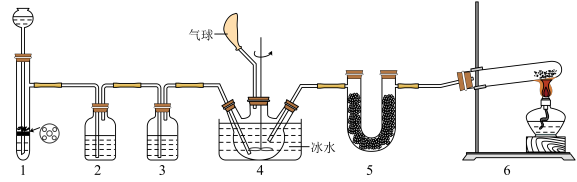
下列分析不正确 的是
 H2NCOONH4(s) H<0。
H2NCOONH4(s) H<0。
下列分析
| A.2中的试剂为饱和NaHCO3溶液 |
| B.冰水浴能提高H2NCOONH4的产率 |
| C.1和4中发生的反应均为非氧化还原反应 |
| D.5中的仪器(含试剂)可用3中仪器(含试剂)代替 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:

下列说法正确的是( )

下列说法正确的是( )
| A.为将溶液A中的Fe2+氧化为Fe3+,试剂①可选用双氧水、氯气等 |
| B.流程中所加的CuO可以用Cu2(OH)2CO3代替 |
| C.溶液C通过蒸发结晶即可获得CuSO4·5H2O |
| D.制备CaCO3时,应向CaCl2溶液中先加入氨水,再通入过量CO2 |
您最近一年使用:0次

 Ca+H2O
Ca+H2O 4Al+3O2↑
4Al+3O2↑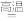 2Cu+SO2
2Cu+SO2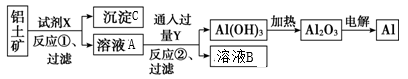

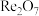 、
、 ,含
,含 、
、 、
、 等杂质)制备铼单质的流程如图所示:
等杂质)制备铼单质的流程如图所示:
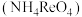 是白色片状晶体,微溶于冷水,溶于热水。
是白色片状晶体,微溶于冷水,溶于热水。 和
和
 可循环使用
可循环使用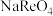 溶液再加入
溶液再加入 ,经冰水冷却、过滤得
,经冰水冷却、过滤得 晶体
晶体

