(1)实验室中常用加热分解氯酸钾制取氧气,写出反应的化学方程式,并用双线桥法仅标出电子转移情况___________________________________________________________ 。
(2))实验室制取Cl2的反应方程式之一为:
___ KMnO4 + ____ HCl —— ____ KCl +____ MnCl2 + ___ C12↑ + ___ H2O
请①配平方程式;②用单线桥法仅标出电子转移情况_________ ;
③浓盐酸表现出来的性质是:_______________ ;
④当有5摩HCl被氧化时,求产生的氯气在标准状况下的体积:___________ 。
(3)KClO3+6HCl===KCl+3Cl2↑+3H2O写出氧化产物还原产物物质的量的比为_________ ,当氧化产物比还原产物多71克时,参加反应的还原剂为________ 摩。
(2))实验室制取Cl2的反应方程式之一为:
请①配平方程式;②用单线桥法仅标出电子转移情况
③浓盐酸表现出来的性质是:
④当有5摩HCl被氧化时,求产生的氯气在标准状况下的体积:
(3)KClO3+6HCl===KCl+3Cl2↑+3H2O写出氧化产物还原产物物质的量的比为
更新时间:2017-11-10 10:53:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)有以下六种物质:①乙醇;②0.1mol/LNa2CO3溶液;③NaOH固体;④液态氯化氢;⑤纯CH3COOH;⑥石墨。上述状态下的物质中,能导电的有________ (填序号,下同),属于电解质的有_______ 。
(2)请写出Na与水反应的方程式,并用双线桥法标出电子转移方向和数目:________
(3)配平下列化学方程式,在横线上填写化学计量数________
____MnO + ____Cl- + _____H+= _____Mn2+ + _____Cl2 + _____H2O
+ ____Cl- + _____H+= _____Mn2+ + _____Cl2 + _____H2O
(2)请写出Na与水反应的方程式,并用双线桥法标出电子转移方向和数目:
(3)配平下列化学方程式,在横线上填写化学计量数
____MnO
 + ____Cl- + _____H+= _____Mn2+ + _____Cl2 + _____H2O
+ ____Cl- + _____H+= _____Mn2+ + _____Cl2 + _____H2O
您最近一年使用:0次
【推荐2】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是_____ (填写字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为______ mol。
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目_________ 。
(1)浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目
您最近一年使用:0次
【推荐1】实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4 +16HCl(浓)=2KCl + 2MnCl2 + 5Cl2↑ +8H2O
(1)用双线桥法标出电子转移的方向和数目_______ 。
(2)该反应中的氧化剂与还原剂物质的量之比是_______ 。
(3)KMnO4的氧化性比Cl2的氧化性_______ (选填“强”或“弱”)。
(4)若反应中转移了2个电子,则产生的Cl2_______ 个。
(5)配平下列氧化还原方程式_______ 。
KMnO4+FeSO4+H2SO4——Fe2(SO4)3+K2SO4+MnSO4+H2O
(6)用单线桥法标出电子转移的方向和数目_______ 。
6MnO +5CuS+28H+→5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+→5Cu2++5SO2↑+6Mn2++14H2O
(1)用双线桥法标出电子转移的方向和数目
(2)该反应中的氧化剂与还原剂物质的量之比是
(3)KMnO4的氧化性比Cl2的氧化性
(4)若反应中转移了2个电子,则产生的Cl2
(5)配平下列氧化还原方程式
KMnO4+FeSO4+H2SO4——Fe2(SO4)3+K2SO4+MnSO4+H2O
(6)用单线桥法标出电子转移的方向和数目
6MnO
 +5CuS+28H+→5Cu2++5SO2↑+6Mn2++14H2O
+5CuS+28H+→5Cu2++5SO2↑+6Mn2++14H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】近年来,我国研究储氢碳管获得重大进展,用电弧法合成碳纳米管,常伴有大量碳纳米颗粒生成,这种碳纳米颗粒可用氧化气化法除去,其反应的化学方程式为:
C +K2Cr2O7 +H2SO4(稀) → CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)此反应的氧化剂________ ,还原剂___________ ;
(2)硫酸在上述反应中表现出的性质是__________ (填选项编号);
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目__________ 。
C +K2Cr2O7 +H2SO4(稀) → CO2+K2SO4+Cr2(SO4)3+H2O(未配平)
(1)此反应的氧化剂
(2)硫酸在上述反应中表现出的性质是
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
(3)上述反应若产生11克气体物质,则转移电子的数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮元素及其化合物的转化关系如图所示。___________ 。
(2)氮元素在元素周期表中的位置是___________ 。
(3)已知1molNH3发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是___________ 。
(4)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。___________ 。
②催化转化过程中,理论上每生成1mol 时,转移的电子为
时,转移的电子为___________ mol。
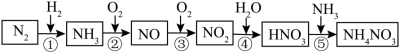
(2)氮元素在元素周期表中的位置是
(3)已知1molNH3发生反应②,完全反应生成NO和水蒸气时放出226 kJ的热,该反应的热化学方程式是
(4)汽车尾气净化装置中,气体在催化剂表面吸附与解吸作用的过程如图所示。
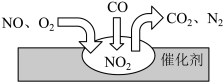
②催化转化过程中,理论上每生成1mol
 时,转移的电子为
时,转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作_______ 极(填“阴”或“阳”)。
(2)Se与S处于同一主族,比S原子多1个电子层,Se的原子序数为____________ ;其最高价氧化物的化学式为________ ;该族 2~5周期元素单质分别与H2反应生成1 mol气态氢化物的反应热如下:
a.+99.7 kJ·mol−1 b.+29.7 kJ·mol−1 c.-20.6 kJ·mol−1 d.-241.8 kJ·mol−1
表示生成 1 mol硒化氢反应热的是________________ (填字母代号)。
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
① 请写出CuSe与浓H2SO4反应的化学方程式___________ 。
② 焙烧过程产生的烟气中含有少量SeO2,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为_________ 。
③ 写出步骤ⅱ中的化学方程式______________________ 。
(1)粗铜精炼时,通常用精铜作
(2)Se与S处于同一主族,比S原子多1个电子层,Se的原子序数为
a.+99.7 kJ·mol−1 b.+29.7 kJ·mol−1 c.-20.6 kJ·mol−1 d.-241.8 kJ·mol−1
表示生成 1 mol硒化氢反应热的是
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
① 请写出CuSe与浓H2SO4反应的化学方程式
② 焙烧过程产生的烟气中含有少量SeO2,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为
③ 写出步骤ⅱ中的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】含氮化合物( 、
、 等)是主要的污染物之一,消除含氮化合物的污染备受关注。
等)是主要的污染物之一,消除含氮化合物的污染备受关注。
(1) 还原技术是当今最有效、最成熟的去除
还原技术是当今最有效、最成熟的去除 的技术之一、使用
的技术之一、使用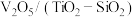 催化剂能有效脱除电厂烟气中的氮氧化物,发生脱硝的主要反应为
催化剂能有效脱除电厂烟气中的氮氧化物,发生脱硝的主要反应为 。在相同的气体流速、
。在相同的气体流速、 条件下,随温度升高,NO转化率先升高后降低(在温度为T℃时达到最大)的可能原因是
条件下,随温度升高,NO转化率先升高后降低(在温度为T℃时达到最大)的可能原因是___________ 。
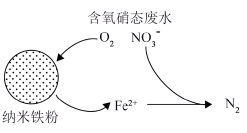
(2)纳米铁粉可用于去除废水中的硝态氮(用 表示),反应原理如图所示。有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除,其原因是
表示),反应原理如图所示。有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除,其原因是___________ 。在纳米铁粉中添加适量的活性炭,能提高单位时间硝态氮去除率的原因是___________ 。
(3)Cu基催化剂是 技术脱除NO中性能较为优异的新型催化剂,但若烟气中含有
技术脱除NO中性能较为优异的新型催化剂,但若烟气中含有 ,则会造成Cu基催化剂的催化性能下降。加入
,则会造成Cu基催化剂的催化性能下降。加入 {基态Ce原子核外电子排布式为
{基态Ce原子核外电子排布式为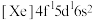 }可抑制
}可抑制 对Cu基催化剂的影响,其作用机理如图所示(含Ce化合物的比例系数均未标定)。
对Cu基催化剂的影响,其作用机理如图所示(含Ce化合物的比例系数均未标定)。
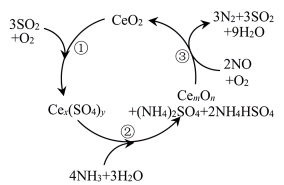
①从整个反应机理来看,总反应中起还原作用的物质是___________ (填化学式)。
②在上述反应机理图中, 的化学式为
的化学式为___________ 。
(4)工业上可采用NaClO和NaOH混合溶液作为吸收剂,在如图所示喷淋吸收塔中进行烟气脱硝。
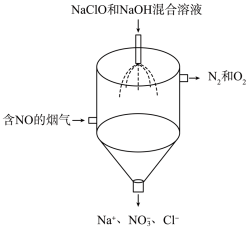
①写出喷淋吸收塔中发生反应的离子方程式:___________ 。
②该装置的优点是___________ 。
 、
、 等)是主要的污染物之一,消除含氮化合物的污染备受关注。
等)是主要的污染物之一,消除含氮化合物的污染备受关注。(1)
 还原技术是当今最有效、最成熟的去除
还原技术是当今最有效、最成熟的去除 的技术之一、使用
的技术之一、使用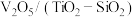 催化剂能有效脱除电厂烟气中的氮氧化物,发生脱硝的主要反应为
催化剂能有效脱除电厂烟气中的氮氧化物,发生脱硝的主要反应为 。在相同的气体流速、
。在相同的气体流速、 条件下,随温度升高,NO转化率先升高后降低(在温度为T℃时达到最大)的可能原因是
条件下,随温度升高,NO转化率先升高后降低(在温度为T℃时达到最大)的可能原因是(2)纳米铁粉可用于去除废水中的硝态氮(用
 表示),反应原理如图所示。有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除,其原因是
表示),反应原理如图所示。有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除,其原因是
(3)Cu基催化剂是
 技术脱除NO中性能较为优异的新型催化剂,但若烟气中含有
技术脱除NO中性能较为优异的新型催化剂,但若烟气中含有 ,则会造成Cu基催化剂的催化性能下降。加入
,则会造成Cu基催化剂的催化性能下降。加入 {基态Ce原子核外电子排布式为
{基态Ce原子核外电子排布式为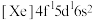 }可抑制
}可抑制 对Cu基催化剂的影响,其作用机理如图所示(含Ce化合物的比例系数均未标定)。
对Cu基催化剂的影响,其作用机理如图所示(含Ce化合物的比例系数均未标定)。
①从整个反应机理来看,总反应中起还原作用的物质是
②在上述反应机理图中,
 的化学式为
的化学式为(4)工业上可采用NaClO和NaOH混合溶液作为吸收剂,在如图所示喷淋吸收塔中进行烟气脱硝。

①写出喷淋吸收塔中发生反应的离子方程式:
②该装置的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请按要求填空:
(1)简单原子的原子结构如图:
①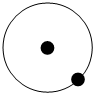 ②
② ③
③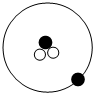
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
(2)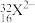 的质子数为
的质子数为___________ ,中子数为___________ ,电子数为___________ ,该元素在元素周期表中的位置是第___________ 周期___________ 族,该元素的最高价氧化物对应水化物的化学式是___________
(3)1828年,德国化学家维勒通过蒸发氰酸铵( )水溶液得到尿素[
)水溶液得到尿素[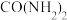 ]。
]。
①氰酸铵和尿素之间的关系是___________ (填标号)。
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为___________ 。
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为___________ 。
(1)简单原子的原子结构如图:
①
 ②
② ③
③
其中“●”表示质子或电子,“○”表示中子。则下列有关①②③的叙述正确的是___________(填标号)。
| A.①②③是三种不同的核素 | B.①②③具有相同的质量数 |
| C.①②③互为同位素 | D.①②③是三种化学性质不同的粒子 |
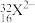 的质子数为
的质子数为(3)1828年,德国化学家维勒通过蒸发氰酸铵(
 )水溶液得到尿素[
)水溶液得到尿素[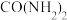 ]。
]。①氰酸铵和尿素之间的关系是
A.同位素B.同素异形体C.同分异构体D.同系物
②尿素在尿素酶的作用下能够水解生成碳酸铵,该反应的化学方程式为
③现代工业上用氨和二氧化碳在200个大气压和180℃时反应合成尿素,该反应的化学方程式为
您最近一年使用:0次

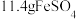 固体,加入足量
固体,加入足量 溶液,使
溶液,使 全部转化成
全部转化成 ,并放出NO气体。
,并放出NO气体。 恰好完全反应时,转移电子的物质的量是
恰好完全反应时,转移电子的物质的量是 ,
,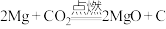 ,
,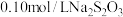 溶液恰好把标准状况下
溶液恰好把标准状况下 完全转化为
完全转化为 ,则
,则 将转化成
将转化成

