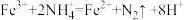已知常温下二氯化二硫(S2Cl2)为红棕色液体,(其结构式为Cl-S-S-C1)。其制备反应及与水反应的化学方程式如下:①CS2+3Cl2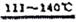 CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2+ S↓,则下列说法正确的是
CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2+ S↓,则下列说法正确的是
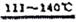 CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2+ S↓,则下列说法正确的是
CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2+ S↓,则下列说法正确的是| A.反应①中CS2 作氧化剂 |
| B.反应①中每生成lmol S2Cl2转移4mol 电子 |
| C.反应②中氧化产物与还原产物的物质的量之比为3:1 |
| D.反应②中S2Cl2 既作氧化剂又作还原剂 |
更新时间:2017-11-19 14:21:13
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知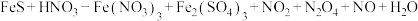 (未配平),当产物中
(未配平),当产物中 时,下列说法错误的是
时,下列说法错误的是
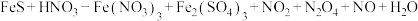 (未配平),当产物中
(未配平),当产物中 时,下列说法错误的是
时,下列说法错误的是A.反应中FeS是还原剂, 、 、 、NO是还原产物 、NO是还原产物 |
B.氧化性: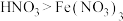 |
C.参加反应的 |
| D.1mol FeS参加反应时有9mol电子转移 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列转化中,需要加入氧化剂才能实现的是
A.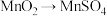 | B.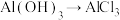 |
C.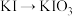 | D.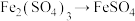 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】一种从废钛酸锂电极材料[含 、铝箔、碳粉、
、铝箔、碳粉、 (聚偏二氟乙烯)等]中回收某些资源的流程如图所示:
(聚偏二氟乙烯)等]中回收某些资源的流程如图所示:
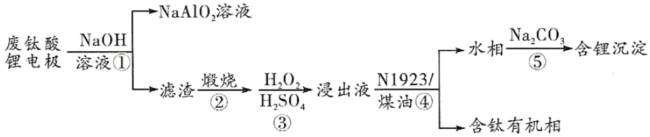
已知: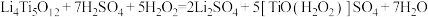 。下列叙述错误的是
。下列叙述错误的是
 、铝箔、碳粉、
、铝箔、碳粉、 (聚偏二氟乙烯)等]中回收某些资源的流程如图所示:
(聚偏二氟乙烯)等]中回收某些资源的流程如图所示:
已知:
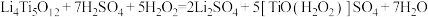 。下列叙述错误的是
。下列叙述错误的是A.步骤②的目的是除去碳粉与 |
B.步骤③中 的作用是氧化剂 的作用是氧化剂 |
C.上述流程中不可用乙醇代替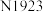 /煤油 /煤油 |
| D.合理处理废旧电池有利于保护环境和资源再利用 |
您最近半年使用:0次
【推荐2】著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性: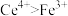 。下列说法正确的是
。下列说法正确的是
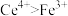 。下列说法正确的是
。下列说法正确的是A.铈能从硫酸铜溶液中置换出铜: |
| B.工业上可以采用惰性电极电解氯化铈水溶液,在阴极得到铈 |
C.用少量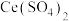 溶液滴定碘化亚铁溶液,其离子方程式为 溶液滴定碘化亚铁溶液,其离子方程式为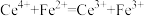 |
| D.金属铈可浸于煤油中保存,要储存在阴凉的地方,远离火种和热源 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知反应:6HCl(浓)+KClO3=KCl+3Cl2↑+3H2O,下列说法正确的是
| A.浓盐酸全部表现还原性 |
| B.生成3molCl2转移的电子数为6NA |
| C.氧化产物和还原产物的个数比为5:1 |
| D.可以利用氯气的漂白性漂白发黄的衣服 |
您最近半年使用:0次
【推荐2】用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新方法。高铁酸钠可通过湿法或干法来制备,反应原理如下:
湿法:
干法:
下列说法不正确的是
湿法:

干法:

下列说法不正确的是
| A.Na2FeO4中铁元素为+6价,具有强氧化性,能消毒杀菌 |
| B.湿法中每生成1mol Na2FeO4转移3 mol e- |
| C.湿法中氧化产物与还原产物的物质的量之比为3∶2 |
| D.干法中Na2O2既是氧化剂又是还原剂 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用FeSO4还原MnO ,若还原5×10-3 mol MnO
,若还原5×10-3 mol MnO ,消耗10 mL 2.5 mol·L-1 FeSO4溶液,则Mn元素在还原产物中的化合价是
,消耗10 mL 2.5 mol·L-1 FeSO4溶液,则Mn元素在还原产物中的化合价是
 ,若还原5×10-3 mol MnO
,若还原5×10-3 mol MnO ,消耗10 mL 2.5 mol·L-1 FeSO4溶液,则Mn元素在还原产物中的化合价是
,消耗10 mL 2.5 mol·L-1 FeSO4溶液,则Mn元素在还原产物中的化合价是| A.+1 | B.+2 | C.+4 | D.+5 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断不正确的是
| A.参与反应的氯气为0.15 mol |
| B.溶液中氯离子的物质的量取值范围是0.10 < n(Cl-)< 0.25 |
| C.n(Na+)∶n(Cl-)可能为15∶8 |
| D.n(NaCl):n(NaClO)∶n(NaClO3)可能为8∶3∶1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】碘化钾为白色固体,可用作分析试剂、感光材料、制药和食品添加剂等,可通过碘酸钾与硫化氢反应制备。实验装置如图所示(夹持及加热装置已省略),下列说法错误的是
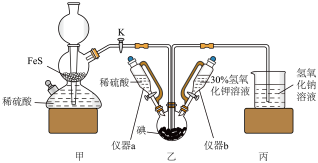

| A.实验中应先关闭K,打开仪器b的活塞,制备碘酸钾 |
| B.滴入30%氢氧化钾溶液后,乙装置中紫黑色固体溶解,棕黄色溶液逐渐变为无色 |
| C.乙装置中稀硫酸主要作用是减小硫化氢溶解度,以利于其逸出在丙装置中被吸收 |
| D.如果乙装置中最终生成4.8g黄色沉淀,则理论上可制得碘化钾的质量为8.3g |
您最近半年使用:0次

 +3Cl-+5H2O,关于该反应说法正确的是
+3Cl-+5H2O,关于该反应说法正确的是 中铁元素显+2价
中铁元素显+2价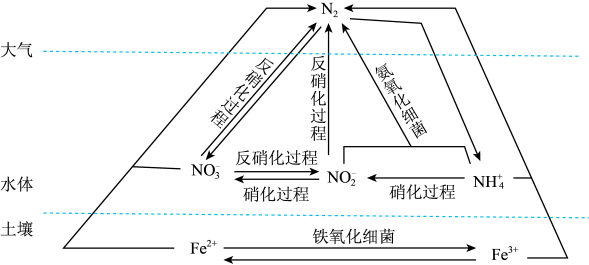
 将
将 转化为
转化为 的离子方程式为
的离子方程式为