室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为∆H1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为∆H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) △ CuSO4(s)+5H2O(l),热效应为∆H3。则下列判断正确的是
| A.∆H2>∆H3 | B.∆H1+∆H3=∆H2 | C.∆H1>∆H2 | D.∆H1+∆H2>∆H3 |
更新时间:2017-11-29 11:56:03
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知下列反应:CO(g)+2H2(g) CH3OH(g) ΔH1①;2H2(g)+O2(g)
CH3OH(g) ΔH1①;2H2(g)+O2(g) 2H2O(l) ΔH2 ②;2CO(g)+O2(g)
2H2O(l) ΔH2 ②;2CO(g)+O2(g)  2CO2(g) ΔH3 ③;2CH3OH(g)+3O2(g)
2CO2(g) ΔH3 ③;2CH3OH(g)+3O2(g) 2CO2(g)+4H2O(l) ΔH4 ④。下列关系正确的是
2CO2(g)+4H2O(l) ΔH4 ④。下列关系正确的是
 CH3OH(g) ΔH1①;2H2(g)+O2(g)
CH3OH(g) ΔH1①;2H2(g)+O2(g) 2H2O(l) ΔH2 ②;2CO(g)+O2(g)
2H2O(l) ΔH2 ②;2CO(g)+O2(g)  2CO2(g) ΔH3 ③;2CH3OH(g)+3O2(g)
2CO2(g) ΔH3 ③;2CH3OH(g)+3O2(g) 2CO2(g)+4H2O(l) ΔH4 ④。下列关系正确的是
2CO2(g)+4H2O(l) ΔH4 ④。下列关系正确的是| A.ΔH4=ΔH3+ΔH2+ΔH1 | B.ΔH4=ΔH3+2ΔH2+2ΔH1 |
| C.ΔH4=ΔH3+2ΔH2−2ΔH1 | D.ΔH4=ΔH3+2ΔH2−ΔH1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】已知:
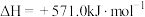 。以太阳能为热源分解
。以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下:
的过程如下:
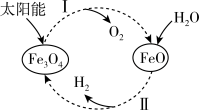
过程Ⅰ: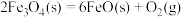
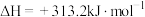
过程Ⅱ:∙∙∙∙∙∙
下列说法不正确的是

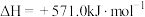 。以太阳能为热源分解
。以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下:
的过程如下:
过程Ⅰ:
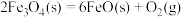
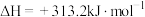
过程Ⅱ:∙∙∙∙∙∙
下列说法不正确的是
A.过程Ⅰ中每消耗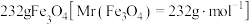 转移 转移 电子 电子 |
| B.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
C.铁氧化合物循环制 具有成本低、产物易分离等优点 具有成本低、产物易分离等优点 |
D.过程Ⅱ的热化学方程式为 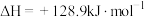 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】已知H2(g)、CO(g)、CH3OH(l)的燃烧热△H分别是-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。下列有关叙述正确的是
| A.甲醇不完全燃烧生成CO和液态水的热化学方程式:CH3OH(l)+O2 (g)=CO(g)+2H2O(l) △H1=-1009.5kJ·mol-1 |
| B.CH3OH(l)+1/2O2 (g)=CO2(g)+2H2 (g) △H1=-440.7kJ·mol-1 |
| C.2H2O(g) =2H2(g)+O2(g) △H1=+571.6 kJ·mol-1 |
| D.已知:S(s)+O2(g) = SO2(g) △H1;S(g)+O2(g) = SO2(g) △H2;则△H1>△H2 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】利用图中实验装置进行的相应实验,能达到实验目的的是
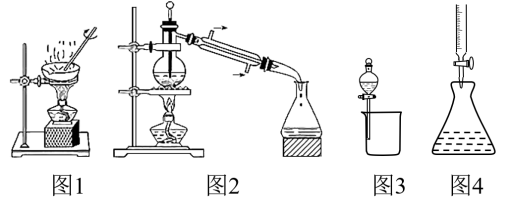

| A.利用图1装置可从胆矾晶体中获得无水硫酸铜 |
| B.利用图2装置可分离石油,得到汽油、煤油和柴油等各种馏分 |
| C.利用图3装置可分离CH3CH2OH和CH3COOC2H5混合液 |
| D.利用图4装置可进行酸碱中和滴定 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列实验的操作、现象、结论或解释均合理的是
| A.酸碱中和滴定时,未用标准液润洗滴定管可导致最终计算结果偏大 |
| B.向Na2SiO3 溶液中滴加稀盐酸,产生白色沉淀可说明非金属性:Cl>Si |
| C.用已检查不漏液的分液漏斗分离苯和水的混合物,需在分液漏斗下端放出苯 |
| D.向某溶液中滴加盐酸酸化的氯化钡,产生白色沉淀可说明原溶液中含有SO42- |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】测定“84”消毒液中次氯酸钠的浓度可用下面方法:取10.00 mL消毒液,调节pH后,以淀粉为指示剂,用0.100mol·L-1 KI溶液进行滴定,当溶液出现稳定浅蓝色时为滴定终点。反应原理为:3ClO-+I-=3Cl-+IO ;IO
;IO +5I-+6H+=3H2O+3I2;三次平行实验中消耗KI的平均体积为20.00mL,由此可知原消毒液中NaClO的物质的量浓度为
+5I-+6H+=3H2O+3I2;三次平行实验中消耗KI的平均体积为20.00mL,由此可知原消毒液中NaClO的物质的量浓度为
 ;IO
;IO +5I-+6H+=3H2O+3I2;三次平行实验中消耗KI的平均体积为20.00mL,由此可知原消毒液中NaClO的物质的量浓度为
+5I-+6H+=3H2O+3I2;三次平行实验中消耗KI的平均体积为20.00mL,由此可知原消毒液中NaClO的物质的量浓度为| A.0.04mol·L-1 | B.0.10mol·L-1 | C.0.25mol·L-1 | D.0.60mol·L-1 |
您最近半年使用:0次



