卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如图:
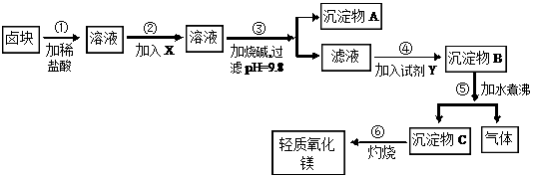
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
(1)在步骤②中加入的试剂X(从表2中选择)是_______ 而不是双氧水,其原因是_______________________ 。写出加入X发生反应的离子方程式_______________________ 。
(2)在步骤③中控制pH=9.8,其目的是____________________________ 。
(3)沉淀物A的成分为______________ ,试剂Y(从表2中选择)应该是_______ 。
(4)在步骤⑤中发生反应的化学方程式是________________________ 。
(5)若在实验室中完成步骤⑥,则沉淀物C必需在_______ (填仪器名称)中灼烧。

已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
| 表1 生成氢氧化物沉淀的pH | 表2 化学试剂价格表 | ||||
| 物质 | 开始沉淀 | 沉淀完全 | 试剂 | 价格(元/吨) | |
| Fe(OH)3 | 2.7 | 3.7 | 漂液(含25.2% NaClO) | 450 | |
| Fe(OH)2 | 7.6 | 9.6 | 双氧水(含30% H2O2) | 2400 | |
| Mn(OH)2 | 8.3 | 9.8 | 烧碱(含98% NaOH) | 2100 | |
| Mg(OH)2 | 10.0 | 11.1 | 纯碱(含99.5% Na2CO3) | 600 | |
(1)在步骤②中加入的试剂X(从表2中选择)是
(2)在步骤③中控制pH=9.8,其目的是
(3)沉淀物A的成分为
(4)在步骤⑤中发生反应的化学方程式是
(5)若在实验室中完成步骤⑥,则沉淀物C必需在
更新时间:2017-12-11 09:59:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硼酸( )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含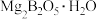 、
、 及少量
及少量 、
、 )为原料生产硼酸及轻质氧化镁的工艺流程如下:
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
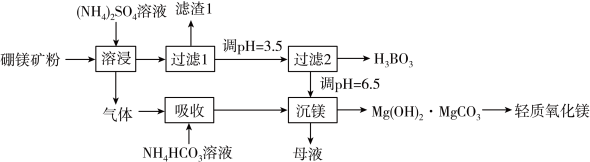
已知:
回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式___________ 。
(2)“滤渣1”的主要成分有___________ (填化学式)。为检验“过滤1”后的滤液中是否含有 离子,可选用的化学试剂是
离子,可选用的化学试剂是___________ (填化学式)。
(3)已知 的电离方程式为
的电离方程式为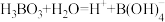 ,可知
,可知 为
为___________ 元弱酸,请写出 与足量
与足量 溶液反应的离子方程式
溶液反应的离子方程式___________ ;“过滤2”前,将溶液pH调节至3.5的目的是___________ 。
(4)“沉镁”后分离生成的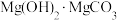 沉淀的操作为
沉淀的操作为___________ ,母液经加热后可返回___________ (填“溶浸”“吸收”或“沉镁”)工序循环使用。高温焙烧碱式碳酸镁可制备轻质氧化镁,写出化学方程式___________ 。
 )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含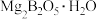 、
、 及少量
及少量 、
、 )为原料生产硼酸及轻质氧化镁的工艺流程如下:
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
已知:

回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式
(2)“滤渣1”的主要成分有
 离子,可选用的化学试剂是
离子,可选用的化学试剂是(3)已知
 的电离方程式为
的电离方程式为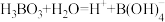 ,可知
,可知 为
为 与足量
与足量 溶液反应的离子方程式
溶液反应的离子方程式(4)“沉镁”后分离生成的
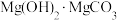 沉淀的操作为
沉淀的操作为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
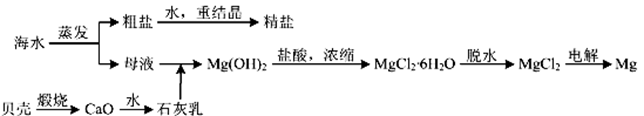
(1)在实验室中由粗盐“重结晶”的操作包括溶解、过滤、蒸发、_________ (填操作方法)、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________ 。
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________ 。
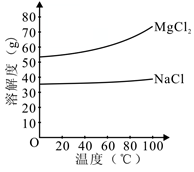
a. 得到热饱和溶液 b. 析出晶体
(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:__________ 。
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____________________________________ 。
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和H2O,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a∶b为______________ (取整数值)。

(1)在实验室中由粗盐“重结晶”的操作包括溶解、过滤、蒸发、
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是

a. 得到热饱和溶液 b. 析出晶体
(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和H2O,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a∶b为
您最近一年使用:0次
【推荐3】MgSO4·7H2O医药上用作泻剂。工业上用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。主要工艺如下:
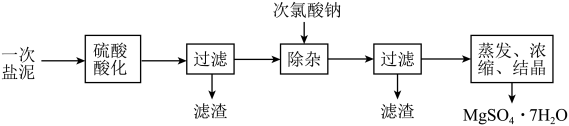
(1)用硫酸调整溶液pH到1~2,硫酸的作用是________________________ 。
(2)加次氯酸钠溶液至pH=5~6并加热煮沸约5~10分钟,滤渣中主要含MnO2和另两种沉淀,另两种沉淀是___________________ (写化学式)。其中次氯酸钠溶液将MnSO4转化为MnO2的离子方程式为:____________________ 。
(3)若除杂后过滤,发现滤液发黄,需采取的措施是__________________ 。
(4)过滤后晶体常用丙酮代替蒸馏水洗涤的目的是______________________ 。
(5)晶体中结晶水含量的测定:准确称取0.20g MgSO4·7H2O样品,放入已干燥至恒重的瓷坩埚,置于马弗炉中,在200℃脱水1小时。为准确确定脱水后的质量,还需要经过的操作有:冷却(干燥器中)至室温→_______________________ 。
(6)硫酸根离子质量分数的测定:准确称取自制的样品0.50g,用200mL水溶液,加入2mol·L-1HCl溶液5mL,将溶液加热至沸,在不断搅拌下逐滴加入5~6mL0.5mol·L-1BaCl2溶液,充分沉淀后,得沉淀0.466g,则样品中w(SO )=
)=____________ 。

(1)用硫酸调整溶液pH到1~2,硫酸的作用是
(2)加次氯酸钠溶液至pH=5~6并加热煮沸约5~10分钟,滤渣中主要含MnO2和另两种沉淀,另两种沉淀是
(3)若除杂后过滤,发现滤液发黄,需采取的措施是
(4)过滤后晶体常用丙酮代替蒸馏水洗涤的目的是
(5)晶体中结晶水含量的测定:准确称取0.20g MgSO4·7H2O样品,放入已干燥至恒重的瓷坩埚,置于马弗炉中,在200℃脱水1小时。为准确确定脱水后的质量,还需要经过的操作有:冷却(干燥器中)至室温→
(6)硫酸根离子质量分数的测定:准确称取自制的样品0.50g,用200mL水溶液,加入2mol·L-1HCl溶液5mL,将溶液加热至沸,在不断搅拌下逐滴加入5~6mL0.5mol·L-1BaCl2溶液,充分沉淀后,得沉淀0.466g,则样品中w(SO
 )=
)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫酰氯(SO2Cl2)熔点-54.1℃,沸点在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。

(1)SO2Cl2中的S的化合价为_______________ ,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为_______________ 。
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(部分夹持装置未画出)。
①仪器A的名称为_______________ ,装置乙中装入的试剂是_______________ ,装置B的作用是_______________ 。
②装置丙分液漏斗中盛装的最佳试剂是_______________ (选填编号)。
A.蒸馏水B.l0.0mol·L-1浓盐酸
C.浓氢氧化钠溶液D.饱和食盐水
③滴定法测定硫酰氯的纯度:取1.800g产品,加入到100mL0.50000mol·L-1NaOH溶液中加热充分水解,冷却后加蒸馏水准确稀释至250mL,取25mL溶液于锥形瓶中,滴加2滴甲基橙,用0.1000mol·L-1标准HCl滴定至终点,重复实验三次取平均值,消耗HCl l0.00mL。达到滴定终点的现象为_______________ ,产品的纯度为_______________ 。

(1)SO2Cl2中的S的化合价为
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(部分夹持装置未画出)。
①仪器A的名称为
②装置丙分液漏斗中盛装的最佳试剂是
A.蒸馏水B.l0.0mol·L-1浓盐酸
C.浓氢氧化钠溶液D.饱和食盐水
③滴定法测定硫酰氯的纯度:取1.800g产品,加入到100mL0.50000mol·L-1NaOH溶液中加热充分水解,冷却后加蒸馏水准确稀释至250mL,取25mL溶液于锥形瓶中,滴加2滴甲基橙,用0.1000mol·L-1标准HCl滴定至终点,重复实验三次取平均值,消耗HCl l0.00mL。达到滴定终点的现象为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
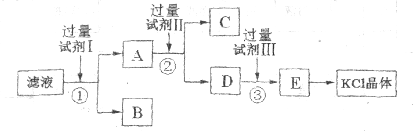
回答下列问题:
(1)检验滤液中的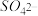 的方法是
的方法是____________ 。
(2)试剂I的化学式为__________ ,加入试剂I后,①对应的实验操作是____ ,①中发生反应的离子方程式为__________ 。
(3)试剂II的化学式为_________ ,②中加入试剂II的目的是______ 。
(4)试剂III的名称是________ ,③中发生反应的离子方程式为____________ 。

回答下列问题:
(1)检验滤液中的
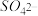 的方法是
的方法是(2)试剂I的化学式为
(3)试剂II的化学式为
(4)试剂III的名称是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】一种利用含AgCl的废渣制取AgNO3的工艺流程如下:
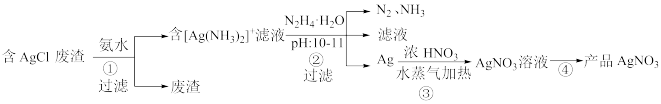
(1)步骤①用氨水浸取时,温度不宜超过35℃,其原因是___ 。在氨水浓度、固液质量比和温度均一定时,为提高银的浸取率还可采取的措施是____ ;浸取时发生反应的离子方程式为____ 。
(2)步骤②中发生反应的离子方程式为______ 。
(3)步骤③中,银与浓硝酸反应生成等物质的量的NO和NO2,当消耗了10.8g Ag时,有______ molHNO3参与了反应。
(4)步骤④的操作为______ ,100℃下烘干得产品AgNO3。
(5)上述流程中发生了氧化还原反应的步骤有______ (用“①”“②”“③”“④”填空)。
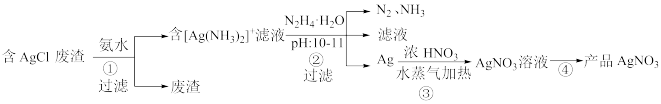
(1)步骤①用氨水浸取时,温度不宜超过35℃,其原因是
(2)步骤②中发生反应的离子方程式为
(3)步骤③中,银与浓硝酸反应生成等物质的量的NO和NO2,当消耗了10.8g Ag时,有
(4)步骤④的操作为
(5)上述流程中发生了氧化还原反应的步骤有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】高锰酸钾生产过程中产生的废锰渣(主要成分为 、KOH、MgO和
、KOH、MgO和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
回答以下问题:
(1)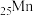 的电子排布式:
的电子排布式:___________ 。
(2)提高“反应Ⅰ”速率可采取的措施是___________ (除“加热”外,任写一种),滤渣A的主要成分为___________ (填化学式)。
(3)“反应Ⅱ”中硫铁矿(FeS₂)的作用为___________ 。
(4)“反应Ⅲ”的离子方程式为___________ 。
(5)“调pH”步骤中,应调节pH的范围是___________ 。
 、KOH、MgO和
、KOH、MgO和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下: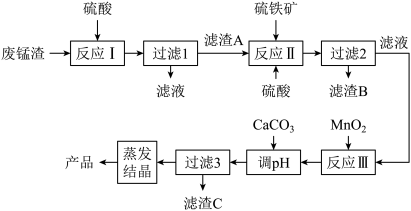
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 2.10 | 7.45 | 9.27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
(1)
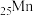 的电子排布式:
的电子排布式:(2)提高“反应Ⅰ”速率可采取的措施是
(3)“反应Ⅱ”中硫铁矿(FeS₂)的作用为
(4)“反应Ⅲ”的离子方程式为
(5)“调pH”步骤中,应调节pH的范围是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】高纯硅制备过程中会产生副产物 ,某同学在实验室以
,某同学在实验室以 和硅镁石(含
和硅镁石(含 、
、 及少量Fe的氧化物)为原料,制备氯化镁晶体(
及少量Fe的氧化物)为原料,制备氯化镁晶体( )并回收
)并回收 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)写出 “水溶”过程中发生反应的化学方程式:
“水溶”过程中发生反应的化学方程式:_______ 。
(2)“氧化”时加 发生反应的离子方程式为
发生反应的离子方程式为_______ ,反应温度不易过高,主要原因是_______ 。
(3)试剂X的作用为“调pH”将杂质转化为沉淀而除去,同时不引入杂质,试剂X可以是下列试剂中的_______ (填字母),“调pH”的范围为_______ 。
A.NaOH B. C.
C. D.MgO
D.MgO
(4)“沉淀1”灼烧后所得固体与“沉淀2”共同用于回收 ,“沉淀1”灼烧时应在
,“沉淀1”灼烧时应在_______ (填仪器名称)中进行。
(5)若以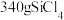 为原料,理论上制得
为原料,理论上制得 的质量为
的质量为_______ g(假设反应过程中Cl元素无损耗)。
 ,某同学在实验室以
,某同学在实验室以 和硅镁石(含
和硅镁石(含 、
、 及少量Fe的氧化物)为原料,制备氯化镁晶体(
及少量Fe的氧化物)为原料,制备氯化镁晶体( )并回收
)并回收 的工艺流程如图所示:
的工艺流程如图所示: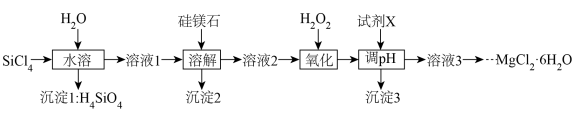
 |  | |
| 开始沉淀的pH | 2.2 | 9.6 |
| 沉淀完全的pH | 3.5 | 11.6 |
(1)写出
 “水溶”过程中发生反应的化学方程式:
“水溶”过程中发生反应的化学方程式:(2)“氧化”时加
 发生反应的离子方程式为
发生反应的离子方程式为(3)试剂X的作用为“调pH”将杂质转化为沉淀而除去,同时不引入杂质,试剂X可以是下列试剂中的
A.NaOH B.
 C.
C. D.MgO
D.MgO(4)“沉淀1”灼烧后所得固体与“沉淀2”共同用于回收
 ,“沉淀1”灼烧时应在
,“沉淀1”灼烧时应在(5)若以
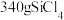 为原料,理论上制得
为原料,理论上制得 的质量为
的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酰氯(SO2C12)和氯化亚砜(SOC12)在空气中遇水蒸气发生剧烈反应,并产生大量白雾。硫酰氯(SO2C12)常用作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。合成的反应式为:SO2(g) + Cl2(g) SO2Cl2(l) △H=-197.3 kJ·mol-1。
SO2Cl2(l) △H=-197.3 kJ·mol-1。
合成SO2C12的装置如下图所示(夹持仪器已省略),请回答有关问题:
(1)从下表中选择相应的装置完成填空:
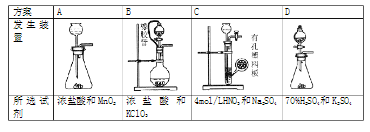
①制备SO2选________ (填字母)。
②写出用所选装置制取Cl2的离子方程式_________________ 。
(2)合成SO2C12的装置图中仪器B的名称为_________________ ;丁中盛放的是_____________ 。
(3)反应结束后,将乙中混合物分离开的实验操作名称是_______________ 。
(4)图中装置C的作用是__________________ 。
(5)为提高本实验中的产率,在实验操作中还需要注意的事项有(只答—条即可)__________ 。
(6)氯化亚砜(SOCl2)与水反应的化学方程式为_____ ,蒸干A1C13溶液不能得到无水AlCl3,用SOC12与AlCl3 • 6H2O的混合加热,可得到无水A1C13,试解释原因__________ 。
 SO2Cl2(l) △H=-197.3 kJ·mol-1。
SO2Cl2(l) △H=-197.3 kJ·mol-1。| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2C12 | -54.1 | 69.1 | 易分解:SO2C12 SO2↑+Cl2↑ SO2↑+Cl2↑ |

(1)从下表中选择相应的装置完成填空:

①制备SO2选
②写出用所选装置制取Cl2的离子方程式
(2)合成SO2C12的装置图中仪器B的名称为
(3)反应结束后,将乙中混合物分离开的实验操作名称是
(4)图中装置C的作用是
(5)为提高本实验中的产率,在实验操作中还需要注意的事项有(只答—条即可)
(6)氯化亚砜(SOCl2)与水反应的化学方程式为
您最近一年使用:0次



