某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
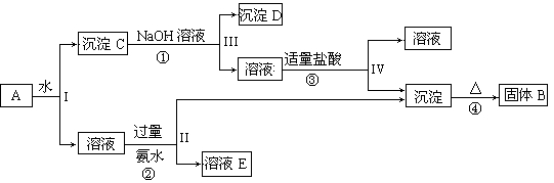
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________ 。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式:
沉淀固体B______________ ;C_____________ ;溶液E________________ 。
(3)写出①、②反应的离子反应化学方程式:
①___________________________________ ;
②______________________________________ ;
写出③、④反应的化学方程式:
③___________________________________ ;
④_______________________________________ 。

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式:
沉淀固体B
(3)写出①、②反应的离子反应化学方程式:
①
②
写出③、④反应的化学方程式:
③
④
更新时间:2017-12-21 20:14:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W、P、Q为中学化学中的常见物质,且X由一种或两种短周期元素组成,一定条件下有如图转化关系,请完成下列问题:
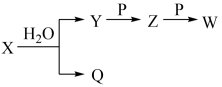
(1)若X为淡黄色固体,P为硫酸盐,W为白色难溶于水的物质,且物质X和W的摩尔质量相等。W中的金属元素基态原子核外电子具有_______ 种能量状态;物质P在生活中常用作_______ (列举两种)。
(2)若物质X中一种元素原子的最外层电子数为内层电子总数的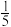 ,将Y和W分别溶于水,所得溶液按恰当比例混合,可得到一种不含金属元素的盐溶液。请写出X与H2O反应的化学方程式:
,将Y和W分别溶于水,所得溶液按恰当比例混合,可得到一种不含金属元素的盐溶液。请写出X与H2O反应的化学方程式:_______ ;Y转化为Z的化学方程式为:_______ 。
(3)若常温下X为有色气体
①若P一种金属单质,请写出Y和适量P反应生成Z与气体Q的离子方程式:_______ 。
②若Z为直线形分子,Q具有漂白性,物质P焰色试验呈黄色,则P的化学式为_______ ;W与(1)(3)题设所指Y_______ (填“一定”或“不一定”)都能发生反应。
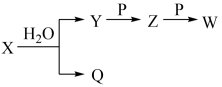
(1)若X为淡黄色固体,P为硫酸盐,W为白色难溶于水的物质,且物质X和W的摩尔质量相等。W中的金属元素基态原子核外电子具有
(2)若物质X中一种元素原子的最外层电子数为内层电子总数的
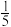 ,将Y和W分别溶于水,所得溶液按恰当比例混合,可得到一种不含金属元素的盐溶液。请写出X与H2O反应的化学方程式:
,将Y和W分别溶于水,所得溶液按恰当比例混合,可得到一种不含金属元素的盐溶液。请写出X与H2O反应的化学方程式:(3)若常温下X为有色气体
①若P一种金属单质,请写出Y和适量P反应生成Z与气体Q的离子方程式:
②若Z为直线形分子,Q具有漂白性,物质P焰色试验呈黄色,则P的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行):
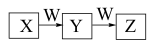
(1)若W是O2,则X不可能是________ (填代号)
a.NH3 b.Mg c.H2S d.Al
(2)若Z为淡黄色粉末,常用作呼吸面具中的供氧剂
①Z与CO2反应的化学方程式为_______ ;
②78g Z与水发生反应时转移电子的物质的量为________ mol。
(3)若X、Y、Z三种物质都含有一种金属元素,且Y为两性物质
①X溶液一步转化为Z溶液的反应离子方程式为________ ;
②将X溶液、Z溶液等体积混合,恰好完全反应,则X溶液、Z溶液的浓度之比为______ 。
(4)若X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为________ ;
②请画出向含0.01mol X和0.01mol Y的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像___ 。
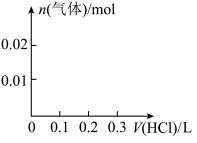
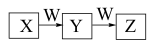
(1)若W是O2,则X不可能是
a.NH3 b.Mg c.H2S d.Al
(2)若Z为淡黄色粉末,常用作呼吸面具中的供氧剂
①Z与CO2反应的化学方程式为
②78g Z与水发生反应时转移电子的物质的量为
(3)若X、Y、Z三种物质都含有一种金属元素,且Y为两性物质
①X溶液一步转化为Z溶液的反应离子方程式为
②将X溶液、Z溶液等体积混合,恰好完全反应,则X溶液、Z溶液的浓度之比为
(4)若X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为
②请画出向含0.01mol X和0.01mol Y的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。其中B是地壳中含量最多的金属。它们之间能发生一系列反应(图中有些反应的产物和反应的条件没有全部标出)。
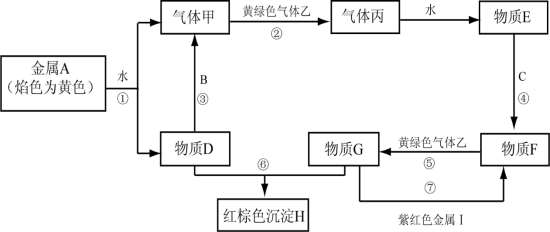
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:C_______ H_______
(2)写出反应③的离子方程式:_______ 写出反应④的离子方程式:_______
(3)实验室检验物质G中阳离子的常用试剂是:_______
(4)实验室检验物质D中阳离子的方法是_______

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:C
(2)写出反应③的离子方程式:
(3)实验室检验物质G中阳离子的常用试剂是:
(4)实验室检验物质D中阳离子的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F、G为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,G为红褐色沉淀。常温下甲、乙、丙为气态非金属单质,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如下图所示(有的反应部分产物已经略去)。请根据以上信息回答下列问题:

(1)写出A的电子式_______ ;
(2)F转化为G的过程中出现的现象是_______ ;
(3)写出②中反应的离子方程式:_______ ;
(4)①~⑥转化中不含有氧化还原反应的是_______ (填序号)。

(1)写出A的电子式
(2)F转化为G的过程中出现的现象是
(3)写出②中反应的离子方程式:
(4)①~⑥转化中不含有氧化还原反应的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A是一种常见金属,C是强碱,各物质有以下物质相互转化。试回答:
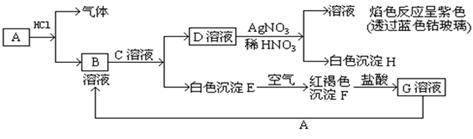
(1)写出A的化学式______ ,C的化学式______ 。
(2)写出由D转变成H的化学方程式______ 。
(3)写出向G溶液加入A的离子反应方程式______ 。

(1)写出A的化学式
(2)写出由D转变成H的化学方程式
(3)写出向G溶液加入A的离子反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示物质相互转换关系:
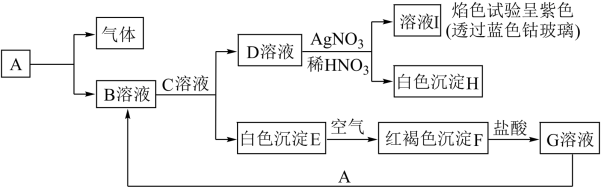
试回答:
(1)写出B的化学式____________ 、C溶液是______________ 。
(2)写出由E转变成F发生反应的化学方程式_______________ 。
(3)鉴别G溶液中阳离子的操作方法及实验现象:__________________ 。
(4)向G溶液中加入A的离子方程式____________________ 。
(5)写出D溶液中加入AgNO3得到白色沉淀的离子方程式__________________ 。

试回答:
(1)写出B的化学式
(2)写出由E转变成F发生反应的化学方程式
(3)鉴别G溶液中阳离子的操作方法及实验现象:
(4)向G溶液中加入A的离子方程式
(5)写出D溶液中加入AgNO3得到白色沉淀的离子方程式
您最近一年使用:0次
【推荐1】锗是重要的半导体材料,应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:
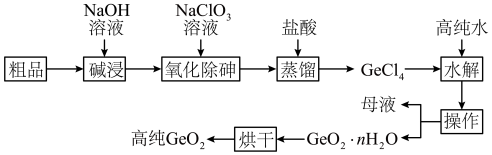
已知:①“碱浸”过程中的反应为GeO2+2NaOH=Na2GeO3+H2O As2O3+2NaOH=2NaAsO2+H2O
②“蒸馏”过程中的反应为Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔点为-49. 5 ℃,AsCl3与GeCl4的沸点分别为130.2 ℃、84 ℃。
(1)锗的原子序数为32,锗在元素周期表中的位置为第___________ 周期___________ 族。
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应的化学方程式为___________ 。
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是___________ 。
(4)“水解”操作时发生的化学反应方程式为___________ ,“水解”操作时保持较低温度有利于提高产率,其可能的原因是___________ (答一条即可)。
(5)若1 t二氧化锗粗品(含杂质30%)经提纯得0.745 t的高纯二氧化锗产品,则杂质脱除率为___________ 。

已知:①“碱浸”过程中的反应为GeO2+2NaOH=Na2GeO3+H2O As2O3+2NaOH=2NaAsO2+H2O
②“蒸馏”过程中的反应为Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔点为-49. 5 ℃,AsCl3与GeCl4的沸点分别为130.2 ℃、84 ℃。
(1)锗的原子序数为32,锗在元素周期表中的位置为第
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应的化学方程式为
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是
(4)“水解”操作时发生的化学反应方程式为
(5)若1 t二氧化锗粗品(含杂质30%)经提纯得0.745 t的高纯二氧化锗产品,则杂质脱除率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以铬矿石(主要成分为Cr2O3,还有Al2O3、SiO2等杂质)为原料制取红矾钠(Na2Cr2O7·2H2O)的流程如图所示。

已知:I.Cr2O3在碱性条件下易被氧化;
Ⅱ.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3+Na2CO3=2NaAlO2+CO2↑;
Ⅲ.
(1)“煅烧”时,Cr2O3参加反应的化学方程式为______ 。若“煅烧”操作最适宜的温度是800~900℃,则在实验室中进行此项操作时,应选择______ 坩埚(填字母)。
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有______ (填化学式)。
(3)“过滤Ⅱ”所得沉淀主要有______ (填化学式)。
(4)电解时阳极的主要反应式______ 。

已知:I.Cr2O3在碱性条件下易被氧化;
Ⅱ.高温条件下,Al2O3与Na2CO3发生的反应为:Al2O3+Na2CO3=2NaAlO2+CO2↑;
Ⅲ.

(1)“煅烧”时,Cr2O3参加反应的化学方程式为
a.陶瓷 b.玻璃 c.石英 d.铁
(2)流程中可循环利用的物质除CO2外还有
(3)“过滤Ⅱ”所得沉淀主要有
(4)电解时阳极的主要反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组以废铁屑(含有碳、Fe2O3杂质)为原料制备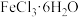 晶体。具体的流程如下:
晶体。具体的流程如下:

试回答下列问题:
(1)提高“酸溶”的速率的方法是:_______ 。
(2)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是_______ 。
(3)过滤时,需要用到的玻璃仪器是:烧杯、_______ 、_______ ,过滤后所得滤渣的主要成分是:_______ 。
(4)“氧化”过程中发生反应的离子方程式为_______ ,该反应中氧化剂是_______ 。
(5)“氧化”过程结束后,如何证明溶液中有 存在?请写出实验方案:
存在?请写出实验方案:_______ 。
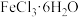 晶体。具体的流程如下:
晶体。具体的流程如下:
试回答下列问题:
(1)提高“酸溶”的速率的方法是:
(2)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是
(3)过滤时,需要用到的玻璃仪器是:烧杯、
(4)“氧化”过程中发生反应的离子方程式为
(5)“氧化”过程结束后,如何证明溶液中有
 存在?请写出实验方案:
存在?请写出实验方案:
您最近一年使用:0次



