下列说法正确的是
| A.加入铝粉能产生H2的溶液中,一定存在大量的Na+、Ba2+、AlO2-、NO3- |
| B.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| C.室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 |
D.已知I3- I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
更新时间:2017/12/21 17:43:44
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列各项关系中正确的是
A.已知NaHSO3溶液显酸性,则溶液中c( )<c(H2SO3) )<c(H2SO3) |
| B.0.2mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合后溶液中存在:c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH) |
| C.常温下pH=2的稀硫酸与pH=12的氨水等体积混合后溶液呈碱性 |
| D.等浓度的溶液①NH4Cl,②(NH4)2SO4,③NH4HSO4中c(NH4+)大小关系为②>①>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 为阿伏加德罗常数的值。工业上制备硫酸涉及
为阿伏加德罗常数的值。工业上制备硫酸涉及 、
、 、
、 、
、 等物质。下列说法正确的是
等物质。下列说法正确的是
 为阿伏加德罗常数的值。工业上制备硫酸涉及
为阿伏加德罗常数的值。工业上制备硫酸涉及 、
、 、
、 、
、 等物质。下列说法正确的是
等物质。下列说法正确的是A. 分子中含有的质子数为 分子中含有的质子数为 |
B. 和 和 充分反应后分子总数为 充分反应后分子总数为 |
C.标准状况下, 中分子的数目为 中分子的数目为 |
D. 的 的 溶液中 溶液中 数目为 数目为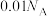 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,水的电离达到平衡:H2O H++OH-,下列叙述正确的是( )
H++OH-,下列叙述正确的是( )
 H++OH-,下列叙述正确的是( )
H++OH-,下列叙述正确的是( )| A.将纯水加热到95℃时,Kw变大,pH不变,水仍呈中性 |
| B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 |
| C.向纯水中加入少量Na2CO3固体,c(OH-)增大,Kw不变,影响水的电离平衡 |
| D.向纯水中加入盐酸,可抑制水的电离;加入醋酸,可促进水的电离 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
【推荐2】已知液氨的性质与水相似。T ℃时,NH3+NH3
 +
+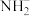 ,
, 的平衡浓度为1×10-15 mol·L-1。下列说法
的平衡浓度为1×10-15 mol·L-1。下列说法错误 的是

 +
+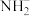 ,
, 的平衡浓度为1×10-15 mol·L-1。下列说法
的平衡浓度为1×10-15 mol·L-1。下列说法| A.在此温度下液氨的离子积为1×10-30 |
| B.在液氨中加入金属钠,可生成NaNH2 |
| C.恒温下,在液氨中加入NH4Cl,可使液氨的电离平衡逆向移动 |
D.降低温度,可使液氨的电离平衡逆向移动,且c( )<c( )<c(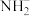 ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列各组离子在指定溶液中能大量共存的是
A.碱性溶液中: 、 、 、 、 、 、 |
B.加入铝粉生成 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.无色溶液中: 、 、 、 、 、 、 |
D.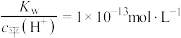 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温下, 的纯碱溶液中,由水电离产生的 的纯碱溶液中,由水电离产生的 数目为 数目为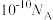 |
B.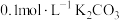 溶液中 溶液中 数目小于 数目小于 |
C.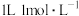 氯化铵水溶液中 氯化铵水溶液中 与 与 数目之和大于 数目之和大于 |
D. 的NaOH水溶液中含有的氧原子数目为 的NaOH水溶液中含有的氧原子数目为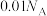 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25℃时,向20.0mL0.100mol/LHR溶液中滴加0.100mol/LMOH溶液,混合溶液的pH与加入MOH溶液体积的变化关系如图所示。设NA为阿伏加德罗常数的值。下列说法错误的是
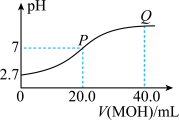

A. 的电离常数的数量级为 的电离常数的数量级为 |
B.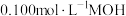 溶液的电离度大于 溶液的电离度大于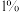 |
C.P点溶液中水电离出的H+数目为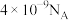 |
D.Q点溶液中存在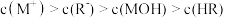 |
您最近一年使用:0次
【推荐1】下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取 溶液和 溶液和 溶液充分反应后,再加 溶液充分反应后,再加 振荡、静置后取上层清液滴加少量KSCN溶液 振荡、静置后取上层清液滴加少量KSCN溶液 | 溶液变为红色 |  与 与 的化学反应存在限度 的化学反应存在限度 |
| B | 向某钾盐中滴加浓盐酸 | 产生的气体可以使品红溶液褪色 | 该钾盐一定为 或 或 或二者的混合物 或二者的混合物 |
| C | 相同温度下,用pH试纸分别测定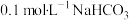 和NaClO溶液的pH 和NaClO溶液的pH | 后者比前者大 |  的酸性强于HClO 的酸性强于HClO |
| D | 向无水乙醇中加入浓硫酸,加热,将产生的气体通入酸性 | 酸性 溶液褪色 溶液褪色 | 产生的气体中一定含有乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如下图所示,若锥形瓶内是水,分液漏斗内的液体是盐酸,向烧杯内滴加水时,发现U形管内液面左边低于右边,恢复到原温度后液面左边与右边基本相平,则烧杯内的物质是
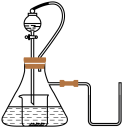

| A.过氧化钠 | B.氧化钠 | C.钠 | D.碳酸氢钠 |
您最近一年使用:0次



 :①=②=③=④
:①=②=③=④ 的量:①最大
的量:①最大 ,则消耗溶液的体积:②=③
,则消耗溶液的体积:②=③ 、Br-
、Br-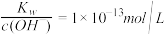 的溶液中:Na+、K+、Cl-、AlO
的溶液中:Na+、K+、Cl-、AlO

 溶液中滴加少量KI溶液,振荡,再滴加几滴淀粉溶液,溶液变蓝
溶液中滴加少量KI溶液,振荡,再滴加几滴淀粉溶液,溶液变蓝 的氧化性比
的氧化性比 的强
的强
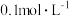 的
的 与
与 溶液的
溶液的 ,
, 的能力:
的能力: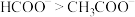
 溶液,紫红色褪去
溶液,紫红色褪去

