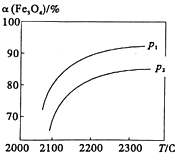
科学家研究以太阳能为热源分解Fe3O4,最终循环分解水制H2,其中一步重要反应为:2Fe3O4(s) 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
 6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
6FeO(s)+O2(g) △H=a kJ/mol。在一定压强下, Fe3O4的平衡转化率随温度变化的a(Fe3O4)―T曲线如图所示。下列有关说法不正确的是
| A.a>0 |
| B.压强p1>p2 |
| C.升高温度,该反应的平衡常数增大 |
| D.将体系中O2分离出去,能提高Fe3O4的转化率 |
更新时间:2017-12-26 20:23:00
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列化学用语正确的是
A.NaHCO3的水解方程式:HCO3-+H2O H3O++CO32- H3O++CO32- |
B.醋酸铵的电离:CH3COONH4 CH3COO-+NH4+ CH3COO-+NH4+ |
C.氯化银的溶解平衡表达式:AgCl(s)  Ag+(aq)+Cl-(aq) Ag+(aq)+Cl-(aq) |
| D.汽车尾气净化反应2NO+2CO=2CO2+N2能够自发进行,则该反应的△H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化硫是一种应用广泛的化工原料。在接触法制硫酸的工业中,二氧化硫制取三氧化硫的反应为2SO2(g)+O2(g) = 2SO3(g) ∆H= -196 kJ•mol-1.实验室用亚硫酸钠固体与70%的硫酸制取少量的二氧化硫。下列有关用二氧化硫制取三氧化硫的说法正确的是
| A.反应的∆S > 0 |
| B.2 mol SO2与足量O2反应,放出的热量为196 kJ |
| C.工业上用通入足量的空气来提高SO2的转化率 |
| D.反应中每消耗1 mol SO2转移的电子数目约等于4×6.02×1023 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:①2H2O(g)===2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1 ②H2S(g)===H2(g)+S(g) ΔH=+20.1 kJ·mol-1下列判断正确的是( )
| A.氢气的燃烧热:ΔH=-241.8 kJ·mol-1 |
| B.相同条件下,充分燃烧1 mol H2(g)与1 mol S(g)的混合物比充分燃烧1 mol H2S(g)放热多20.1 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.②中若生成固态硫,ΔH将增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:
Ⅰ.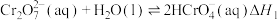
Ⅱ.
关于该溶液的说法不正确 的是(温度变化忽略不计)
 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:Ⅰ.
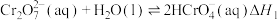
Ⅱ.

关于该溶液的说法
| A.加水稀释,溶液中离子总数增加 |
B.加入少量浓 溶液,Ⅰ和Ⅱ均向正反应方向移动 溶液,Ⅰ和Ⅱ均向正反应方向移动 |
C.加入少量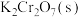 ,溶液颜色不再变化时, ,溶液颜色不再变化时,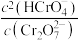 比原溶液中的小 比原溶液中的小 |
D.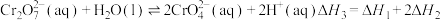 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关说法正确的是
| A.工业上现在大规模采用电解熔融NaCl或AlCl3制取Na或Al |
| B.若电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化 |
| C.某反应的平衡常数K300℃>K350℃,则该反应 △H<0 |
| D.合成氨生产中将NH3液化分离,目的是加快正反应速率,提高H2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将一定量的 SO2(g)和 O2(g)置于一恒容密闭容器中,在不同温度下进行反应(已知该反应为放热反应)。实验记录得到下表中的两组数据:下列有关说法中不正确的是( )
| 实验序号 | 温度(℃) | 平衡常数(L/mol) | 起始量/mol | 平衡量/mol | 达到平衡所需时间(min) | ||
| SO2 | O2 | SO2 | O2 | ||||
| 1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
| A.表中x=1.6;y=0.2 | B.表中t>6 |
| C.表中K1、K2的关系:K2>K1 | D.实验1在前6min的反应速率 υ(SO2)=0.2 mol/(L•min) |
您最近一年使用:0次