实验室模拟工业利用氟磷灰石[Ca5(PO4)3F]生产磷铵[(NH4)3PO4]和白磷。其工艺流程如下图所示:
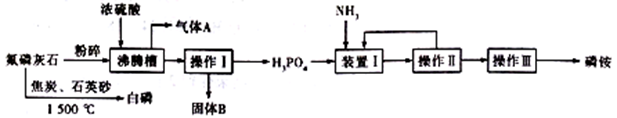
(1)氟磷灰石中磷元素的化合价为________ ,气体A 的电子式为________________ ;固体B 的化学式为____________________________ 。
(2)沸腾槽不能用陶瓷材质的原因是_______________________ (用化学方程式表示)。
(3)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500 ℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为____________________________ 。
(4)在装置I中通入过量氨气的目的是_______________________________ 。
(5)磷铵与草木灰不能混合使用的原因是_____________________ 。
(6)(NH4)3PO4溶液中含磷离子浓度的大小顺序是______________________ 。

(1)氟磷灰石中磷元素的化合价为
(2)沸腾槽不能用陶瓷材质的原因是
(3)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500 ℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为
(4)在装置I中通入过量氨气的目的是
(5)磷铵与草木灰不能混合使用的原因是
(6)(NH4)3PO4溶液中含磷离子浓度的大小顺序是
2018·河南安阳·一模 查看更多[3]
河南省安阳市2018届高三第一次模拟考试理综化学试题(已下线)【中等生百日捷进提升系列-技能方法】专题20 以流程图为基础的化工工艺综合题2020届高三化学选修4二轮专题练——溶液中微粒浓度大小的比较专题【精编25题】
更新时间:2018-01-26 15:29:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系,该元素(用R表示)的单质能与NaOH溶液反应生成盐(Na2RO3)和氢气。
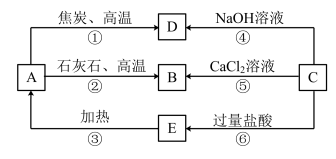
请回答下列问题:
(1)写出各物质的化学式:A________ ;B________ ;C________ ;D________ ;E________ 。
(2)写出反应①的化学方程式:______________________________________ ,该反应中氧化剂与还原剂的物质的量之比为________ 。
(3)写出反应④的离子方程式:______________________________________ 。
(4)写出反应⑤的离子方程式:______________________________________ 。
(5)H2CO3的酸性强于E的,请用离子方程式予以证明:________________________________ 。

请回答下列问题:
(1)写出各物质的化学式:A
(2)写出反应①的化学方程式:
(3)写出反应④的离子方程式:
(4)写出反应⑤的离子方程式:
(5)H2CO3的酸性强于E的,请用离子方程式予以证明:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__ ,还可使用____ 代替硝酸。
(2)沉淀A的主要成分是_____ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为__ 。
(3)加氨水过程中加热的目的是______ 。沉淀B的主要成分为______ 、______ (填化学式)。
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,则高锰酸钾与草酸反应的离子反应方程式为:___ 。

回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
(3)加氨水过程中加热的目的是
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,则高锰酸钾与草酸反应的离子反应方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】由三种元素组成的一种常态为液态的化合物 ,沸点约为
,沸点约为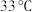 ,有关转化如图:
,有关转化如图:
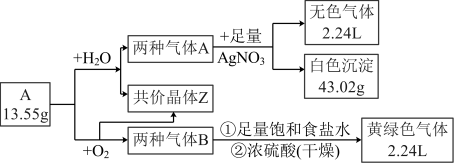
注:①气体体积已折算为标准状况;②上述生成 均为
均为 。
。
试分析推断并回答:
(1) 的化学式
的化学式 _______ ;
(2) 在
在 中燃烧生成的产物通常是
中燃烧生成的产物通常是 和
和 _______ (写分子式);
(3)已知在一定条件下: ,则
,则 ,写出后者完整的化学方程式
,写出后者完整的化学方程式 _______ ;而 与乙烯在一定条件下发生加成反应主要生成
与乙烯在一定条件下发生加成反应主要生成 _______ (写结构简式);
(4) 通常具有
通常具有 _______ 结构;
(5)工业上常用 与一种单质在高温下作用制取另一种单质的粗产品,该反应能否证明组成这二种单质的元素的非金属性强弱?若能,其主要理由是
与一种单质在高温下作用制取另一种单质的粗产品,该反应能否证明组成这二种单质的元素的非金属性强弱?若能,其主要理由是 _______ ;若不能,则请设计另外一个简单实验证明: _______ (写出所用试剂及主要操作和现象、结论)。
 ,沸点约为
,沸点约为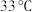 ,有关转化如图:
,有关转化如图:
注:①气体体积已折算为标准状况;②上述生成
 均为
均为 。
。试分析推断并回答:
(1)
 的化学式
的化学式 (2)
 在
在 中燃烧生成的产物通常是
中燃烧生成的产物通常是 和
和 (3)已知在一定条件下:
 ,则
,则 ,写出后者完整的化学方程式
,写出后者完整的化学方程式  与乙烯在一定条件下发生加成反应主要生成
与乙烯在一定条件下发生加成反应主要生成 (4)
 通常具有
通常具有 (5)工业上常用
 与一种单质在高温下作用制取另一种单质的粗产品,该反应能否证明组成这二种单质的元素的非金属性强弱?若能,其主要理由是
与一种单质在高温下作用制取另一种单质的粗产品,该反应能否证明组成这二种单质的元素的非金属性强弱?若能,其主要理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】“高压氢还原法”可直接从溶液中提取金属Cu粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
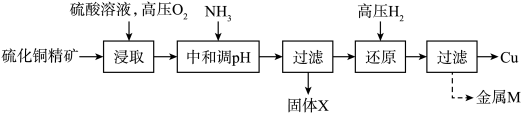
请回答下列问题:
(1)“浸取”时,能够提高浸取率的措施有___________ (任写一条即可)。
(2)“浸取”过程中,1mol CuS参与反应时,转移2NA电子,写出该过程CuS发生的离子反应方程式___________ 。
(3)工业上对硫化铜精矿的预处理有很多方法,相比于高压氢还原法的“浸取”步骤,在空气中“高温焙烧法”最大的缺点是___________ 。
(4)流程图中“中和调pH”一步,氨水调节的pH范围为___________ 。
(5)“过滤”操作用到的玻璃仪器有___________ 。
(6)固体X的主要成分是___________ ,金属M的成分___________ 。

 |  |  | |
| 开始沉淀pH | 1.9 | 4.2 | 6.2 |
| 沉淀完全pH | 3.2 | 6.7 | 8.2 |
(1)“浸取”时,能够提高浸取率的措施有
(2)“浸取”过程中,1mol CuS参与反应时,转移2NA电子,写出该过程CuS发生的离子反应方程式
(3)工业上对硫化铜精矿的预处理有很多方法,相比于高压氢还原法的“浸取”步骤,在空气中“高温焙烧法”最大的缺点是
(4)流程图中“中和调pH”一步,氨水调节的pH范围为
(5)“过滤”操作用到的玻璃仪器有
(6)固体X的主要成分是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】合成氨在工业生产中具有重要意义。
(1)在合成氨工业中I2O5常用于定量测定CO的含量。已知2I2(s)+5O2(g)=2I2O5(s)△H=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g)△H=-566kJ·mol-1。则该测定反应的热化学方程式为____________________________________ 。
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数φ (CO2)随时间t变化曲线如图。

①b点CO的平衡转化率α为____________ ,c点的平衡常数K为________________ 。
②下列措施能提高该反应CO转化率的是________ (填字母)
a.升高温度b.增大压强c.加入催化剂d.移走CO2
(3)若氨水与SO2恰好生成正盐,则此时溶液呈_________ (填“酸性”或“碱性”),向上述溶液中通入___________ (填“NH3”或“SO2”)可使溶液呈中性。(已知常温下NH3·H2O的Kb=1.8×10-5mol·L-1,H2SO3的Ka1=1.5×10-2mol·L-1,Ka2=6.3×10-8mol·L-1)
(1)在合成氨工业中I2O5常用于定量测定CO的含量。已知2I2(s)+5O2(g)=2I2O5(s)△H=-76kJ·mol-1;2CO(g)+O2(g)=2CO2(g)△H=-566kJ·mol-1。则该测定反应的热化学方程式为
(2)不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 mol CO,测得CO2的体积分数φ (CO2)随时间t变化曲线如图。

①b点CO的平衡转化率α为
②下列措施能提高该反应CO转化率的是
a.升高温度b.增大压强c.加入催化剂d.移走CO2
(3)若氨水与SO2恰好生成正盐,则此时溶液呈
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一瓶澄清溶液,可能含有 、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、
、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、 、
、 、
、 中的一种或几种。取该溶液进行以下实验:
中的一种或几种。取该溶液进行以下实验:
①用pH试纸检验,表明溶液呈强酸性;
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色;
③另取部分溶液,向其中逐滴加入NaOH溶液,使溶液从酸性变为碱牲,在滴加过程中先生成白色沉淀后完全溶解;取部分碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
④另取部分③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
根据以上实验事实回答下列问题:
(1)该溶液中肯定存在的离子是___________________ ,肯定不存在的离子是________ ;
(2)步骤③加入NaOH溶液过程中先生成白色沉淀后完全溶解的离子方程式为_______ 。
 、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、
、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、 、
、 、
、 中的一种或几种。取该溶液进行以下实验:
中的一种或几种。取该溶液进行以下实验:①用pH试纸检验,表明溶液呈强酸性;
②取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色;
③另取部分溶液,向其中逐滴加入NaOH溶液,使溶液从酸性变为碱牲,在滴加过程中先生成白色沉淀后完全溶解;取部分碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝。
④另取部分③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
根据以上实验事实回答下列问题:
(1)该溶液中肯定存在的离子是
(2)步骤③加入NaOH溶液过程中先生成白色沉淀后完全溶解的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钛酸锰( )纳米材料是一种多用途催化剂。工业上用红钛锰矿(主要成分为
)纳米材料是一种多用途催化剂。工业上用红钛锰矿(主要成分为 ,还含有少量FeO、
,还含有少量FeO、 、
、 等杂质)来制备
等杂质)来制备 ,其工艺流程如图所示。
,其工艺流程如图所示。
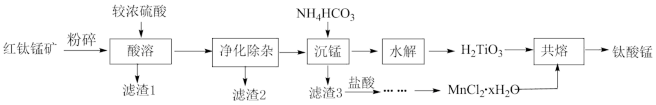
已知:①红钛锰矿“酸溶”后Ti元素主要以 的形式存在;②
的形式存在;② 不溶于无机酸和碱,不溶于水。
不溶于无机酸和碱,不溶于水。
(1)钛酸锰中Ti的化合价为___________ ,“粉碎”的目的是___________ 。
(2)“酸溶”中发生的主要反应的化学方程式为___________ 。
(3)“净化除杂”需先加氧化剂氧化再调溶液的pH,则滤渣2的成分是___________ 。
(4)“沉锰”的条件一般控制在45℃以下的原因是___________ 。
(5)实验室进行“共熔”(高温焙烧)操作时,将固体放置在___________ (填一种硅酸盐仪器名称)中加热。
 )纳米材料是一种多用途催化剂。工业上用红钛锰矿(主要成分为
)纳米材料是一种多用途催化剂。工业上用红钛锰矿(主要成分为 ,还含有少量FeO、
,还含有少量FeO、 、
、 等杂质)来制备
等杂质)来制备 ,其工艺流程如图所示。
,其工艺流程如图所示。
已知:①红钛锰矿“酸溶”后Ti元素主要以
 的形式存在;②
的形式存在;② 不溶于无机酸和碱,不溶于水。
不溶于无机酸和碱,不溶于水。(1)钛酸锰中Ti的化合价为
(2)“酸溶”中发生的主要反应的化学方程式为
(3)“净化除杂”需先加氧化剂氧化再调溶液的pH,则滤渣2的成分是
(4)“沉锰”的条件一般控制在45℃以下的原因是
(5)实验室进行“共熔”(高温焙烧)操作时,将固体放置在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:
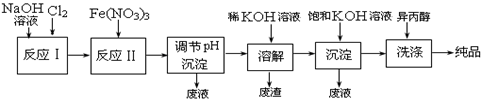
①反应I的化学方程式为___________________ 。
②反应II的离子方程式为_______________________ 。
③加入饱和KOH溶液的目的是__________________________ 。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为_________________ ;___________________ 。(用文字表述)
(3)干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为______________ 。
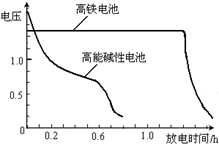
(4)高铁电池是正在研制中的可充电干电池,右图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有______________ ;_____________ 。
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:

|
①反应I的化学方程式为
②反应II的离子方程式为
③加入饱和KOH溶液的目的是
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为
(3)干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为
(4)高铁电池是正在研制中的可充电干电池,右图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铁、铜及其化合物是中学化学中常见化学物质,阅读材料回答问题:
(一)氯化铁是重要的化工原料,FeCl3·6H2O的实验室制备流程图如下:
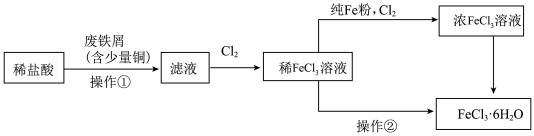
(1)废铁屑表面往往含有油污,去除废铁屑表面的油污的方法是___________ 。操作①要用到的玻璃仪器有玻璃棒、烧杯和___________ 。
(2)加入含有少量铜的废铁屑比加入纯铁屑反应更快,原因为___________ 。操作②涉及的过程为:加热浓缩、___________ 、过滤、洗涤、干燥。
(3)检验FeCl3稀溶液中是否残留Fe2+的试剂可以是___________ 。为增大FeCl3溶液的浓度,向稀FeCl3溶液中加入纯Fe粉后通入Cl2。此过程中发生的主要反应的离子方程式为___________ 、___________ 。
(二)为测定CuSO4溶液的浓度,某同学设计了如下方案:
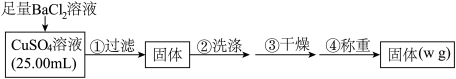
(4)判断 沉淀完全的操作为
沉淀完全的操作为___________ 。
(5)固体质量为w g,则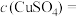
___________ mol/L。若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得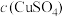
___________ (填“偏高”、“偏低”或“无影响”)。
(一)氯化铁是重要的化工原料,FeCl3·6H2O的实验室制备流程图如下:

(1)废铁屑表面往往含有油污,去除废铁屑表面的油污的方法是
(2)加入含有少量铜的废铁屑比加入纯铁屑反应更快,原因为
(3)检验FeCl3稀溶液中是否残留Fe2+的试剂可以是
(二)为测定CuSO4溶液的浓度,某同学设计了如下方案:

(4)判断
 沉淀完全的操作为
沉淀完全的操作为(5)固体质量为w g,则
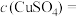
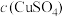
您最近一年使用:0次



