(1)已知:Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑现将9.6g铜完全溶于200mL的硫酸中,试计算
CuSO4+2H2O+SO2↑现将9.6g铜完全溶于200mL的硫酸中,试计算
①标况下产生SO2的体积为_______ 。
②所生成硫酸铜溶液的物质的量浓度(设反应后溶液的体积为200mL)为_______ 。
(2)通常情况下,将1体积98%的浓硫酸(密度ρg/cm3)与5体积的水混合得到一种稀硫酸,该硫酸(密度dg/cm3)物质的量浓度为________________________ 。
(3)一定量的氢气在氯气中燃烧,所得混合物用100ml 3.00mol/L 的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol,原NaOH溶液的质量分数为_________ 。所得溶液中Cl-的物质的量为________ mol。氢气和氯气的物质的量之比n(H2)∶n(Cl2)为____________ 。
 CuSO4+2H2O+SO2↑现将9.6g铜完全溶于200mL的硫酸中,试计算
CuSO4+2H2O+SO2↑现将9.6g铜完全溶于200mL的硫酸中,试计算①标况下产生SO2的体积为
②所生成硫酸铜溶液的物质的量浓度(设反应后溶液的体积为200mL)为
(2)通常情况下,将1体积98%的浓硫酸(密度ρg/cm3)与5体积的水混合得到一种稀硫酸,该硫酸(密度dg/cm3)物质的量浓度为
(3)一定量的氢气在氯气中燃烧,所得混合物用100ml 3.00mol/L 的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol,原NaOH溶液的质量分数为
更新时间:2018-03-17 18:07:54
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)在一定条件下,将NH4HCO3受热分解生成NH3、CO2、H2O(g),得到的混合气体的平均摩尔质量为_______ g/mol(保留小数点后一位)。
(2)在10.0 mL0.1 mol/LNa2CO3溶液中逐滴加入0.1 mol/L的稀盐酸,边加边振荡,若使反应不产生CO2气体,加入的稀盐酸的体积最多不超过_______ mL。
(3)将不纯的NaOH样品1 g (样品含少量Na2CO3和水),放入50 mL 2 mol/L的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1 mol/L的NaOH溶液,蒸发中和后的溶液,最终得到_______  的固体。
的固体。
(2)在10.0 mL0.1 mol/LNa2CO3溶液中逐滴加入0.1 mol/L的稀盐酸,边加边振荡,若使反应不产生CO2气体,加入的稀盐酸的体积最多不超过
(3)将不纯的NaOH样品1 g (样品含少量Na2CO3和水),放入50 mL 2 mol/L的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1 mol/L的NaOH溶液,蒸发中和后的溶液,最终得到
 的固体。
的固体。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2==CH2+Cl2→CH2Cl—CH2Cl ①
CH2Cl—CH2Cl→CH2="=CHCl+HCl "②
已知反应①中二氯乙烷的产率(产率= ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯__________ t,同时得到副产物氯化氢__________ t。(计算结果保留1位小数)
CH2==CH2+Cl2→CH2Cl—CH2Cl ①
CH2Cl—CH2Cl→CH2="=CHCl+HCl "②
已知反应①中二氯乙烷的产率(产率=
 ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8 t乙烯可制得氯乙烯
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】取50.0 mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到8.24 g白色沉淀,用过量稀硝酸处理后沉淀量减少到2.33g,并有气体放出。试计算:
(1)原混合溶液中Na2SO4的物质的量浓度______ ;
(2)原混合溶液中Na+的物质的量浓度__________ ;
(3)产生的气体在标准状况下的体积______________ 。
(1)原混合溶液中Na2SO4的物质的量浓度
(2)原混合溶液中Na+的物质的量浓度
(3)产生的气体在标准状况下的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】化学计量在化学中占有重要地位,请回答下列问题:
(1)0.3 mol NH3分子中所含原子数与______ 个H2O分子中所含原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的 的质量是
的质量是_______ 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的相对分子质量为______ 。
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是_____ 。
(5)某盐混合溶液中含有离子:Na+、Mg2+ 、Cl-、 ,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(
,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c( )=
)=______ 。
(1)0.3 mol NH3分子中所含原子数与
(2)含0.4 mol Al3+的Al2(SO4)3中所含的
 的质量是
的质量是(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的相对分子质量为
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(5)某盐混合溶液中含有离子:Na+、Mg2+ 、Cl-、
 ,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(
,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c( )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】Ⅰ.(1)病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如右图所示。利用标签所提供的信息,计算该注射液中葡萄糖的物质的量浓度为____________ (保留两位有效数字);
(2)检查人的血液中葡萄糖(简称血糖)的含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL)。以“mmol/L”表示时,人的血糖正常值在3.61~6.11 mmol/L 之间。若某人的血糖检查结果为92mg/dL,他的血糖正常吗?_________ (填“正常”或“不正常”)
Ⅱ.现有0.270kg质量分数为10%的CuCl2溶液,计算
(1)溶液中CuCl2的物质的量为___________ ;
(2)要将溶液中的Cl-完全沉淀,需加入1.0 mol/L的AgNO3溶液_______ mL;
(3)要将溶液中的铜完全置换出来,需加入Fe 的质量为__________ 。

(2)检查人的血液中葡萄糖(简称血糖)的含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL)。以“mmol/L”表示时,人的血糖正常值在3.61~6.11 mmol/L 之间。若某人的血糖检查结果为92mg/dL,他的血糖正常吗?
Ⅱ.现有0.270kg质量分数为10%的CuCl2溶液,计算
(1)溶液中CuCl2的物质的量为
(2)要将溶液中的Cl-完全沉淀,需加入1.0 mol/L的AgNO3溶液
(3)要将溶液中的铜完全置换出来,需加入Fe 的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】请计算:
(1)200mL 16mol·L-1的浓硝酸与3.2g Cu反应,反应过程中还原产物只有NO2,则反应结束后:产生气体的体积为_______ (标准状况下),溶液中c(H+):c(NO )=
)=_______ (忽略HNO3的挥发)。
(2)6.4g Cu与过量硝酸(a mol·L-1,30mL)充分反应。硝酸的还原产物只有NO2、NO,反应后溶液中含H+为0.1mol,此时溶液中所含NO 为
为_______ mol。
(1)200mL 16mol·L-1的浓硝酸与3.2g Cu反应,反应过程中还原产物只有NO2,则反应结束后:产生气体的体积为
 )=
)=(2)6.4g Cu与过量硝酸(a mol·L-1,30mL)充分反应。硝酸的还原产物只有NO2、NO,反应后溶液中含H+为0.1mol,此时溶液中所含NO
 为
为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将32.0 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体体积为11.2 L(已换算为标准状况)。请回答:
(1)NO的体积为_______ L
(2)待产生的气体全部释放后,向溶液中加入V mLa mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______ mol·L-1.(不用化简)
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水_______ g。(保留一位小数)
(1)NO的体积为
(2)待产生的气体全部释放后,向溶液中加入V mLa mol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】已知Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。
(1)写出Cl2在70℃的NaOH水溶液中符合上述条件的总反应方程式_________ ;
(2)计算完全反应后生成物NaClO3的物质的量浓度______
(1)写出Cl2在70℃的NaOH水溶液中符合上述条件的总反应方程式
(2)计算完全反应后生成物NaClO3的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知Cl2在70℃的NaOH水溶液中,能发生氧化还原反应后可生成NaClO与NaClO3现有63.9g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后测得溶液中NaClO与NaClO3的物质的量比为4:1,并得到500mL溶液。
(1)写出Cl2在70℃的NaOH水溶液中发生上述反应的化学方程式______ 。
(2)计算完全反应后溶液中NaClO、NaClO3物质的量浓度____ 、______ 。
(1)写出Cl2在70℃的NaOH水溶液中发生上述反应的化学方程式
(2)计算完全反应后溶液中NaClO、NaClO3物质的量浓度
您最近一年使用:0次

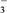 两种离子的物质的量(n)与反应时间(t)的关系曲线如图所示(不考虑氯气和水的反应)。
两种离子的物质的量(n)与反应时间(t)的关系曲线如图所示(不考虑氯气和水的反应)。