下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是________ ,只有负价而无正价的是________ ,氧化性最强的单质是_______ ,还原性最强的单质是________ 。
(2)最高价氧化物的水化物中碱性最强的是________ ,酸性最强的是________ ,呈两性的是________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物中碱性最强的是
17-18高一·全国·课时练习 查看更多[2]
更新时间:2018-03-12 13:43:34
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的前三周期:
请回答下列问题:
(1)A、B两种元素组成相对分子质量最小的化合物,其分子的空间结构为________ 。
(2)C、E两种元素形成的氢化物沸点较高的是___________ ,请简述理由________ 。
(3)B、E、F三种元素的最高价氧化物对应水化物的酸性强弱顺序为______ (用化学式表示)。
(4)用A、C的单质可以制成燃料电池,电池中装有由A、C、D三种元素形成的浓溶液,用多孔的金属惰性电极浸入此浓溶液中,在X极通入C的单质,Y极通入A的单质,则Y极是该电池的_______ 极,X极的电极反应式是______ 。当电池中转移1 mol电子时,消耗A单质的体积为_____ L(标准状况)。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | B | C | ||||||
| 3 | D | E | F |
请回答下列问题:
(1)A、B两种元素组成相对分子质量最小的化合物,其分子的空间结构为
(2)C、E两种元素形成的氢化物沸点较高的是
(3)B、E、F三种元素的最高价氧化物对应水化物的酸性强弱顺序为
(4)用A、C的单质可以制成燃料电池,电池中装有由A、C、D三种元素形成的浓溶液,用多孔的金属惰性电极浸入此浓溶液中,在X极通入C的单质,Y极通入A的单质,则Y极是该电池的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有甲、乙、丙、丁四种短周期元素,甲元素M电子层上的电子数是K电子层上电子数的一半,乙元素的单质在室温下,冷的浓硫酸或空气中表面都能生成致密的氧化膜;丙元素的单质在常温下是黄绿色气体;丁元素的二价阴离子与丙元素的阴离子具有相同的电子层结构。
(1)写出甲、乙、丙、丁四种元素的符号。
甲______ 、乙_______ 、丙_______ 、丁________ 。
(2)甲元素和乙元素最高价氧化物对应的水化物碱性较强的是__________ (填化学式)。
(3)将过量的丙元素的单质通入FeBr2溶液中,发生反应的离子方程式是:_________ ,该反应的氧化剂是:______ (写物质名称)。
(1)写出甲、乙、丙、丁四种元素的符号。
甲
(2)甲元素和乙元素最高价氧化物对应的水化物碱性较强的是
(3)将过量的丙元素的单质通入FeBr2溶液中,发生反应的离子方程式是:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】针对下面10种元素,完成以下各小题。
(1)地壳中含量最多的元素是_______ (填名称)。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)Al的原子结构示意图为_______ 。
(4)C与N相比,原子半径较小的是_______ 。
(5)最高价氧化物对应的水化物碱性最强的是_______ (填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是_______ 。
(7)S和Cl相比,元素非金属性较强的是_______ 。
(8)可用来制造光导纤维的物质是_______ ,晶体硅的主要用途是_______ (写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:_______ 。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是
(2)化学性质最不活泼的元素是
(3)Al的原子结构示意图为
(4)C与N相比,原子半径较小的是
(5)最高价氧化物对应的水化物碱性最强的是
(6)MgO和Al2O3中,属于两性氧化物的是
(7)S和Cl相比,元素非金属性较强的是
(8)可用来制造光导纤维的物质是
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表列出了①~⑥六种元素在周期表中的位置。
请按要求回答下列问题:
(1)写出①的元素符号___________________ 。
(2)⑥的原子结构示意图是_______________ 。
(3)写出③与⑤的单质反应的化学方程式__________________________ 。
(4)③和④中金属性较弱的是_______________ (填化学式)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(1)写出①的元素符号
(2)⑥的原子结构示意图是
(3)写出③与⑤的单质反应的化学方程式
(4)③和④中金属性较弱的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】分子筛是一类具有规整孔道结构的多孔材料,能够选择性吸附空间结构各异和不同尺寸的分子,在化学工业中有着广泛的应用。近年来,我国科学家在分子筛研究领域不断取得新的突破。这些研究中涉及的部分元素在周期表中位置如下:
(1)近期我国科学家制备了一种无缺陷的分子筛膜,可高效分离CH4与CO2两种气体。下列有关分子空间结构的描述正确的是_______
(2)传统的分子筛主要含有O、Na、Al和Si元素,通过调控这 4种元素的比例,可获得不同性能的分子筛产品。这4种元素描述中正确的是_______ 。
(3)通过将分子筛中的元素Na替换为K或Ca,可改变分子筛的孔径大小。这3种元素中说法正确的是_______
(4)N2常用于分子筛的孔结构测试,H、O和N元素可形成多种物质。下列说法正确的是_______
(5)某些分子筛可以选择性吸附Ar。Ar位于元素周期表的_______
| 周期 | 族 | ||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | H | ||||||
| 2 | C | N | O | ||||
| 3 | Na | Al | Si | ||||
| 4 | K | Ca | |||||
| A.CH4是平面结构 | B.CO2是V形结构 |
| C.CH4是正四面体结构 | D.CO2是直线形结构 |
| A.非金属性最强的是O |
| B.核外电子数最少的是 Na |
| C.金属性最强的是Al |
| D.原子半径最大的是Si |
| A.仅Na可与Cl2反应 |
| B.K的单质与水的反应最剧烈 |
| C.Na的氧化物与水的反应均为化合反应 |
| D.Ca的最高价氧化物的水化物碱性最强 |
| A.N2中含有共价三键 |
| B.NO可由NH3催化氧化得到 |
| C.NH3的水溶液呈碱性 |
| D.稀HNO3与Cu反应产生H2 |
| A.第二周期 | B.Ⅷ族 | C.第三周期 | D.0族 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】铁是一种重要的元素,在成人体中的含量达44~5g,铁的配合物在有机合成、催化等领域中发挥重要作用。
Ⅰ.Fe³⁺的配合物在溶液中呈现不同的颜色,如 呈淡紫色(稀溶液时为无色),
呈淡紫色(稀溶液时为无色),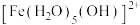 、
、 呈黄色。在黄色
呈黄色。在黄色 溶液中,加入稀
溶液中,加入稀 至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L
至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L NaCl溶液,溶液又变为黄色。
NaCl溶液,溶液又变为黄色。
(1)铁元素位于元素周期表的第___________ 周期第___________ 族。
(2) 中,中心离子为
中,中心离子为___________ ,配位原子是___________ ,配位数为___________ 。
(3)加入NaCl溶液后,溶液又变为黄色的原因:___________ (用离子方程式表示)。
Ⅱ. 不易被人体吸收,维生素C可帮助人体将
不易被人体吸收,维生素C可帮助人体将 转变为易吸收的
转变为易吸收的 。
。
(4)维生素C的分子结构如下图所示,分子中碳原子的杂化方式有___________ ;推测维生素C在水中的溶解性:___________ (填“难溶于水”或“易溶于水”)。
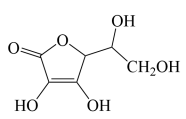
(5)根据维生素C的结构特征,分析预测其可能的化学性质,参考①的示例,完成下表。 (若不需要“可反应的试剂”,可对应填写“没有”)
②___________ 、___________ ;
③___________ 、___________ 、___________ 。
Ⅰ.Fe³⁺的配合物在溶液中呈现不同的颜色,如
 呈淡紫色(稀溶液时为无色),
呈淡紫色(稀溶液时为无色),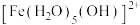 、
、 呈黄色。在黄色
呈黄色。在黄色 溶液中,加入稀
溶液中,加入稀 至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L
至溶液接近无色,再往该无色溶液加入3滴1 mol⋅L NaCl溶液,溶液又变为黄色。
NaCl溶液,溶液又变为黄色。(1)铁元素位于元素周期表的第
(2)
 中,中心离子为
中,中心离子为(3)加入NaCl溶液后,溶液又变为黄色的原因:
Ⅱ.
 不易被人体吸收,维生素C可帮助人体将
不易被人体吸收,维生素C可帮助人体将 转变为易吸收的
转变为易吸收的 。
。(4)维生素C的分子结构如下图所示,分子中碳原子的杂化方式有

(5)根据维生素C的结构特征,分析预测其可能的化学性质,参考①的示例,完成下表。 (若不需要“可反应的试剂”,可对应填写“没有”)
| 序号 | 结构特征 | 可反应的试剂 | 反应类型 |
| ① | 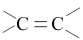 |  | 加成反应 |
| ② | 氧化反应 | ||
| ③ |
③
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】黑火药是中国四大发明之一,其爆炸反应的化学方程式是:2KNO3 + 3C + S→A + N2↑ + 3CO2↑,完成下列填空:
(1)化学方程式中的第二周期元素非金属性由强到弱的顺序依次为_____________________ 。
(2)N2的电子式为_____________ 。
(3)生成物A的化学式为________ ;其晶体类型为_________ ;构成晶体A的微粒半径大小关系为________ (用微粒符号表示)。
(4)说明氮元素的非金属性比碳元素强的事实是___________ 。
(1)化学方程式中的第二周期元素非金属性由强到弱的顺序依次为
(2)N2的电子式为
(3)生成物A的化学式为
(4)说明氮元素的非金属性比碳元素强的事实是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,根据表中给出10种元素按要求作答。
(1)镁元素位于元素周期表中第____________ 周期____________ 族;
(2)空气组成中体积分数最大的气体是____________ ;
(3)O与S相比,原子半径较小的是____________ ;
(4)金刚石的组成元素是____________ ;
(5)单质的化学性质最不活泼的元素是____________ ;
(6)Na与Mg元素相比,金属性较强的是____________ ;
(7)NH3与PH3相比,热稳定性较弱的是____________ ;
(8)H2SO4与H3PO4相比,酸性较强的是____________ ;
(9)Mg(OH)2与Al(OH)3,其中属于两性氢氧化物的是____________ ;
(10)单质呈黄绿色的气体组成元素是____________ ,其单质的水溶液呈____________ (填“酸性”或“碱性”)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | P | S | Cl |
(1)镁元素位于元素周期表中第
(2)空气组成中体积分数最大的气体是
(3)O与S相比,原子半径较小的是
(4)金刚石的组成元素是
(5)单质的化学性质最不活泼的元素是
(6)Na与Mg元素相比,金属性较强的是
(7)NH3与PH3相比,热稳定性较弱的是
(8)H2SO4与H3PO4相比,酸性较强的是
(9)Mg(OH)2与Al(OH)3,其中属于两性氢氧化物的是
(10)单质呈黄绿色的气体组成元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)从元素原子得失电子的角度看,元素⑤具有___________ (填“氧化性”或“还原性”)。
(2)元素②形成的单质气体含有___________ (填“极性”或“非极性”)共价键。
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为___________ 。
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),最高价氧化物对应的水化物具有两性的物质是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是___________ (填离子符号)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)从元素原子得失电子的角度看,元素⑤具有
(2)元素②形成的单质气体含有
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是
您最近一年使用:0次



