黑火药是中国四大发明之一,其爆炸反应的化学方程式是:2KNO3 + 3C + S→A + N2↑ + 3CO2↑,完成下列填空:
(1)化学方程式中的第二周期元素非金属性由强到弱的顺序依次为_____________________ 。
(2)N2的电子式为_____________ 。
(3)生成物A的化学式为________ ;其晶体类型为_________ ;构成晶体A的微粒半径大小关系为________ (用微粒符号表示)。
(4)说明氮元素的非金属性比碳元素强的事实是___________ 。
(1)化学方程式中的第二周期元素非金属性由强到弱的顺序依次为
(2)N2的电子式为
(3)生成物A的化学式为
(4)说明氮元素的非金属性比碳元素强的事实是
13-14高二·上海金山·阶段练习 查看更多[1]
(已下线)上海市金山区2013-2014学年水平模拟卷高二化学试题
更新时间:2020-03-23 13:23:32
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】如表为元素周期表中的一部分,请回答下列问题:
(1)写出⑤元素的名称_______ 。
(2)写出③元素的离子结构示意图_______ 。
(3)④单质与水发生反应的离子方程式_______ 。
(4)写出⑥元素在周期表中的位置_______ 。
(5)比较单质氧化性的强弱⑤_______ ⑦(填”>”、”<”或”=”)。
| 项目 | I A | II A | III A | IV A | V A | VI A | VII A |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | |||||
| 四 | ⑥ | ⑦ |
(1)写出⑤元素的名称
(2)写出③元素的离子结构示意图
(3)④单质与水发生反应的离子方程式
(4)写出⑥元素在周期表中的位置
(5)比较单质氧化性的强弱⑤
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】比较下列各组元素中金属性或非金属性的强弱。
(1)Na、K_______ ;
(2)P、Cl_______ ;
(3)S、Cl_______ ;
(4)O、S_______ ;
(1)Na、K
(2)P、Cl
(3)S、Cl
(4)O、S
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】含氯化合物具有广泛的应用,回答下列问题。
(1)1mol 含有的中子数为
含有的中子数为_______  。
。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是_______ (填微粒符号,下同),Ⅱ是_______ ,Ⅲ是_______ 。
(3) 是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是
是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是_______ (填字母)。
a.原子得电子能力 b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性 d.单质的沸点
(4)由Cu、C、 溶液组成的原电池如图所示:
溶液组成的原电池如图所示:

该电池中负极为_______ (填化学式),电子移动方向为_______ (填“Cu→C”或“C→Cu”),正极上发生的电极反应式为_______ 。
(1)1mol
 含有的中子数为
含有的中子数为 。
。(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)
 是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是
是高效、广谱、绿色的消毒剂。下列能判断Cl、O两种元素非金属性强弱的是a.原子得电子能力 b.与金属钠反应得电子的数目
c.最简单气态氢化物的稳定性 d.单质的沸点
(4)由Cu、C、
 溶液组成的原电池如图所示:
溶液组成的原电池如图所示:
该电池中负极为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】X、Y、Z、W、M、R、T七种短周期元素,周期表中位置如图:
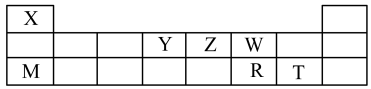
试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是______ (用元素符号表示)。
(2)W的简单氢化物的电子式为_______ 。
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为______ 。
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是______ (用化学式表示)。
(5)M和R最高价氧化物对应水化物反应的离子方程式为______ 。

试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是
(2)W的简单氢化物的电子式为
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是
(5)M和R最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】元素周期表的一部分,按要求完成各小题。
(1)金属性最强的单质与水反应的离子方程式为____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是____ 。
(3)①③⑤三种元素的原子半径由大到小的顺序为____ 。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是____ 。向该元素和⑧号元素组成的化合物溶液中,缓缓滴加NaOH至过量,现象为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是
(3)①③⑤三种元素的原子半径由大到小的顺序为
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:_________ (填元素符号)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子式是:_________ ,碱性最强的化合物的电子式是:_________ 。
(3)元素⑤的单质与元素③的最高价氧化物对应的水化物反应的离子方程式为_________ 。
(4)元素②的简单氢化物是由_________ (填“极性”或“非极性”)键形成的,在常温下该化合物与元素⑥的单质反应的离子方程式为__________________ 。
(5)元素②、③、⑥、⑧四种元素形成的离子,离子半径由大到小的顺序是_________ (用离子符号表示)。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 第二周期 | ① | ② | ||||||
| 第三周期 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 第四周期 | ⑧ | ⑨ |
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子式是:
(3)元素⑤的单质与元素③的最高价氧化物对应的水化物反应的离子方程式为
(4)元素②的简单氢化物是由
(5)元素②、③、⑥、⑧四种元素形成的离子,离子半径由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Q、R、X、Y、Z的电子层数均不大于3,且核电核数依次增大;Q+离子中只有质子,Z+离子的最内层电子数是最外层的 ;R、X、Y三种元素的原子核外电子层数相同,R某种单质的熔点很高;Y原子的最外层电子数是电子层数的3倍。
;R、X、Y三种元素的原子核外电子层数相同,R某种单质的熔点很高;Y原子的最外层电子数是电子层数的3倍。
(1)X的元素符号为_______ ,Z+离子的结构示意图为_____ 。
(2)Q与R、X、Y形成的化合物中,属于非极性分子的是______ (填分子式),其分子的空间形状为_______ 。
(3)Q2Y的稳定性比H2S_______ (填“大”“小”),说明理由_______ 。
 ;R、X、Y三种元素的原子核外电子层数相同,R某种单质的熔点很高;Y原子的最外层电子数是电子层数的3倍。
;R、X、Y三种元素的原子核外电子层数相同,R某种单质的熔点很高;Y原子的最外层电子数是电子层数的3倍。(1)X的元素符号为
(2)Q与R、X、Y形成的化合物中,属于非极性分子的是
(3)Q2Y的稳定性比H2S
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】X、Y、Z、M、R、Q是短周期主族元素,部分信息如表所示:
①表中与X位于同族的元素是_______ (填元素符号),该元素对应离子的结构示意图为_______ 。
②Y与R相比,非金属性较强的是___ (用元素符号表示),下列事实能证明这一结论的是____ (填母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性: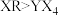
c.最高价氧化物对应水化物的酸性: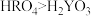
③根据表中数据推测,Y的原子半径的范围是_______ 。
④Z、Q的最高价氧化物对应的水化物在水中反应生成盐的化学式是_______ 。
| X | Y | Z | M | R | Q | |
原子半径/nm | 0. 186 | 0.074 | 0.099 | 0. 143 | ||
主要化合价 | -4, +4 | -2 | -1,+ 7 | +3 | ||
其他 | 简单阳离子核外无电子 | 无机非金属材料的“主角” | 焰色反应呈黄色 |
①表中与X位于同族的元素是
②Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性:
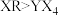
c.最高价氧化物对应水化物的酸性:
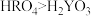
③根据表中数据推测,Y的原子半径的范围是
④Z、Q的最高价氧化物对应的水化物在水中反应生成盐的化学式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】现有下列晶体,请按要求回答相应问题。(前六个小题用编号填空)
A.干冰 B.晶体硅 C.氩 D.二氧化硅 E.氯化铵
(1)通过非极性键形成的晶体是______ 。
(2)属于非电解质且熔化时只需破坏分子间作用力的是______ 。
(3)属于分子晶体,且分子为直线型结构的是_______ 。
(4)不含任何化学键的晶体是___ 。
(5)固态时不导电,熔融状态下能导电的是_______ 。
(6)含有离子键、共价键、配位键的化合物是_____ 。
(7)已知石墨在一定条件下可将D还原成B,反应方程式为SiO2+2C Si+2CO,若石墨中C—C的键能为a,SiO2中Si—O的键能为b,晶体硅中Si—Si的键能为c,CO的键能为d,请用a、b、c、d表示生成晶体硅时的反应热△H=
Si+2CO,若石墨中C—C的键能为a,SiO2中Si—O的键能为b,晶体硅中Si—Si的键能为c,CO的键能为d,请用a、b、c、d表示生成晶体硅时的反应热△H=___________________ 。
A.干冰 B.晶体硅 C.氩 D.二氧化硅 E.氯化铵
(1)通过非极性键形成的晶体是
(2)属于非电解质且熔化时只需破坏分子间作用力的是
(3)属于分子晶体,且分子为直线型结构的是
(4)不含任何化学键的晶体是
(5)固态时不导电,熔融状态下能导电的是
(6)含有离子键、共价键、配位键的化合物是
(7)已知石墨在一定条件下可将D还原成B,反应方程式为SiO2+2C
 Si+2CO,若石墨中C—C的键能为a,SiO2中Si—O的键能为b,晶体硅中Si—Si的键能为c,CO的键能为d,请用a、b、c、d表示生成晶体硅时的反应热△H=
Si+2CO,若石墨中C—C的键能为a,SiO2中Si—O的键能为b,晶体硅中Si—Si的键能为c,CO的键能为d,请用a、b、c、d表示生成晶体硅时的反应热△H=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)氯酸钾熔化,粒子间克服了___________ 的作用力;二氧化硅熔化粒子间克服了___________ 的作用力;碘升华,粒子间克服了___________ 作用力。三种晶体的熔点由高到低的顺序是___________ 。
(2)A、B、C、D为四种晶体,性质如下:A固态时能导电,能溶于盐酸;B能溶于CS2,不溶于水;C固态时不导电,液态时能导电,可溶于水;D固态、液态时均不导电,熔点为3500℃。试推断它们的晶体类型:A.___________ ;B.___________ ;C.___________ ;D.___________ 。
(3)图中A~D是中学化学教材中常见的几种晶体结构模型,请填写相应物质的名称:A.___________ ;B.___________ ;C.___________ ;D.___________

(2)A、B、C、D为四种晶体,性质如下:A固态时能导电,能溶于盐酸;B能溶于CS2,不溶于水;C固态时不导电,液态时能导电,可溶于水;D固态、液态时均不导电,熔点为3500℃。试推断它们的晶体类型:A.
(3)图中A~D是中学化学教材中常见的几种晶体结构模型,请填写相应物质的名称:A.

您最近一年使用:0次



