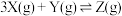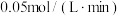在一定温度下,向a L密闭容器中加入1molX气体和2 molY气体,发生如下反应:X(g) + 2Y(g) 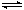 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
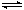 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是| A.容器内压强不随时间变化 |
| B.容器内各物质的浓度完全相同 |
| C.容器内X、Y、Z的浓度之比为1∶2∶2 |
| D.单位时间消耗0.1molX同时生成0.2molZ |
10-11高二下·浙江杭州·期中 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】工业上常用煤和水作原料经过多步反应制得氢气,恒容的条件下,其中一步反应原理为CO(g)+H2O(g)  CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是
CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是
 CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是
CO2(g)+H2(g),下面选项的条件中可判断该反应达到平衡状态的是| A.单位时间内消耗1 mol的H2O同时生成1 mol的H2 |
| B.两个H—O键断裂的同时有一个H—H键断裂 |
| C.反应容器内的密度不再发生变化 |
| D.混合气体的相对分子质量不发生变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】把5.0g铝片投入到500mL0.5mol∙L-1稀硫酸中,反应产生氢气的速率随时间t的变化如图所示,下列推论错误的是
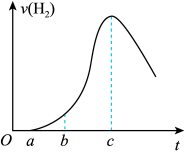

| A.0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液 |
| B.b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
| C.t=c时反应处平衡状态 |
| D.t>c产生氢气的速率降低主要是因为溶液中c(H+)降低 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】一定条件下,将1 molN2与3 molH2置于容积为2 L的恒容密闭容器中,发生反应:N2(g)+3H2(g) 2NH3(g),经过20 min,该反应达到平衡,此时容器中含有0.4 molNH3.下列说法正确的是
2NH3(g),经过20 min,该反应达到平衡,此时容器中含有0.4 molNH3.下列说法正确的是
 2NH3(g),经过20 min,该反应达到平衡,此时容器中含有0.4 molNH3.下列说法正确的是
2NH3(g),经过20 min,该反应达到平衡,此时容器中含有0.4 molNH3.下列说法正确的是| A.20 min时,正、逆反应速率均为0 |
| B.N2与H2浓度比不变,说明该反应已达平衡状态 |
| C.20 min内,该反应平均速率v(H2)=0.03 mol/(L·min) |
| D.20 min后,保持条件不变,NH3的浓度不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在某密闭容器中发生反应: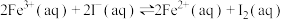 。下列情况不能说明反应达到平衡状态的是
。下列情况不能说明反应达到平衡状态的是
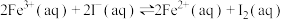 。下列情况不能说明反应达到平衡状态的是
。下列情况不能说明反应达到平衡状态的是| A.溶液颜色不再变化 | B.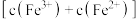 不再变化 不再变化 |
C.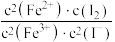 不再变化 不再变化 | D.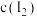 不再变化 不再变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】一定温度下在容积不变的密闭容器中进行如下可逆反应:
SiF4(g)+2H2O(g)⇌SiO2(s)+4HF(g),下列能表明该反应已达到化学平衡状态的是
①v正(SiF4)=4v逆(HF)②HF的体积分数不再变化③容器内气体压强不再变化
④混合气体的密度保持不变⑤4molO—H键断裂的同时,有2molH—F键断裂
SiF4(g)+2H2O(g)⇌SiO2(s)+4HF(g),下列能表明该反应已达到化学平衡状态的是
①v正(SiF4)=4v逆(HF)②HF的体积分数不再变化③容器内气体压强不再变化
④混合气体的密度保持不变⑤4molO—H键断裂的同时,有2molH—F键断裂
| A.①②③④ | B.②③④ | C.②⑤ | D.③④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】以Cl2、SO2和PCl3为原料,制备POCl3和氯化亚砜(SOCl2)的原理为PCl3(g)+Cl2(g)+SO2(g) POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
 POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是
POCl3(s)+SOCl2(g);ΔH<0,下列说法正确的是| A.使用催化剂可以同时降低正反应和逆反应的活化能 |
| B.1molCl-Cl键断裂的同时有2molS-Cl键形成,说明反应到达该条件下的平衡状态 |
C.反应平衡常数K= |
| D.上述反应中消耗3.36LCl2,转移电子数为0.3×6.02×1023 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】合成氨反应的化学方程式为:N2(g) + 3H2 (g)⇌2NH3(g)。一定条件下,下列说法能充分说明该反应已经达到化学平衡状态的是
| A.每消耗 1 mol N2的同时,有 2 mol NH3 生成 |
| B.正、逆反应速率相等且都等于零 |
| C. H2、N2、NH3的浓度均不再变化 |
| D.H2、NH3、N2在容器中共存 |
您最近一年使用:0次

 和3mol H2,在一定条件下使其发生反应生成
和3mol H2,在一定条件下使其发生反应生成 。达到平衡时,下列说法中正确的是
。达到平衡时,下列说法中正确的是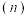 随着时间
随着时间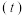 变化的曲线如图所示.下列说法正确的是
变化的曲线如图所示.下列说法正确的是