由铜、锌和稀硫酸组成的原电池中,正极是_______ ,发生_______ ,电极反应是_______ ;负极是_______ ,发生_______ ,电极反应是_______ ,电子的流动方向是从_______ 极到_______ 极;电流方向是从_______ 极到_______ 极。
10-11高一下·吉林延边·期中 查看更多[2]
更新时间:2016-12-08 17:45:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】如图是一个电化学过程的示意图,请按要求回答下列问题
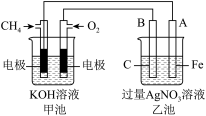
(1)甲池是_______ 装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入CH4的电极_______ 。
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增_______ g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是____
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
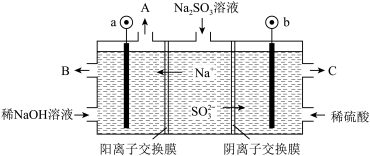
①图中a极要连接电源的_______ (填“正”或“负”)极,C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。

(1)甲池是
(2)写出电极反应式:通入CH4的电极
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。

①图中a极要连接电源的
②
 放电的电极反应式为
放电的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(12分)全矾液流电池是一种新型电能储存和高效转化装置,其电解质溶液为VOSO4溶液,该电解质溶液可通过下列方法制取:将18.2gV2O5和30mL浓H2SO4加入到40mL水中,并在充分搅拌下在水浴上加热20min。向溶液中加水稀释至375mL,通SO2至悬浮液变成深蓝色溶液。将此溶液蒸发浓缩至原体积的五分之一,通入足量的CO2。再将溶液煮沸后,用稀释至1000mL,全矾液流电池的工作原理为:
(1)通入SO2发生反应的化学方程式为______________________ 。
(2)通入CO2的目的是_________________________ 。
(3)全矾液流电池充电时,阳极的电极反应式为____________________ 。
(4)某溶液中含有VO2+、Cr2O32—,现向此溶液中滴入29.00mL0.1mol/L的FeSO4溶液,恰好使VO2+→VO2+,Cr2O32—→ Cr3+。再滴入2.00mL,0.020mol/LKMnO2溶液,又恰好使VO2+→VO2+,而Cr3+不变,试求溶液中Cr的质量(mg) .

(1)通入SO2发生反应的化学方程式为
(2)通入CO2的目的是
(3)全矾液流电池充电时,阳极的电极反应式为
(4)某溶液中含有VO2+、Cr2O32—,现向此溶液中滴入29.00mL0.1mol/L的FeSO4溶液,恰好使VO2+→VO2+,Cr2O32—→ Cr3+。再滴入2.00mL,0.020mol/LKMnO2溶液,又恰好使VO2+→VO2+,而Cr3+不变,试求溶液中Cr的质量(mg) .
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氢气是未来非常理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
(1)分解海水时,________ 能转变为________ 能。生成的氢气用于燃料电池时,________ 能转变为________ 能。
(2)某种氢氧燃料电池是用NaOH溶液作电解质,正极的电极反应式为________ ;若把燃料改为甲烷,负极的电极反应式为________ 。
(3)氢气可用于合成氨。一定温度下,向2L 的密闭容器中加入1 molN2和 3molH2发生反应 N2(g)+3H2(g) 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的 。则前2min用NH3表示的化学反应速率为
。则前2min用NH3表示的化学反应速率为________ ;平衡时,N2的转化率为________ ,混合气体的平均相对分子质量为________ 。
 2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:(1)分解海水时,
(2)某种氢氧燃料电池是用NaOH溶液作电解质,正极的电极反应式为
(3)氢气可用于合成氨。一定温度下,向2L 的密闭容器中加入1 molN2和 3molH2发生反应 N2(g)+3H2(g)
 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的 。则前2min用NH3表示的化学反应速率为
。则前2min用NH3表示的化学反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
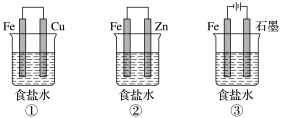
为防止金属Fe被腐蚀,可以采用上述________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为_________________ 。
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_______________________ 。
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
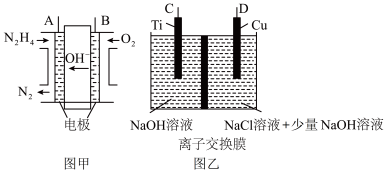
(1)上述装置中D电极应连接肼燃料电池的________ 极(填“A”或“B”),该电解池中离子交换膜为________ 离子交换膜(填“阴”或“阳”)。
(2)该电解池的阳极反应式为____________________ 。
(3)当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为
Ⅱ.纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。

(1)上述装置中D电极应连接肼燃料电池的
(2)该电解池的阳极反应式为
(3)当反应生成14.4 g Cu2O时,至少需要肼
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】原电池是直接把化学能转化为电能的装置。
(1)如图所示:
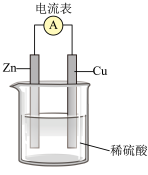
①在Cu-Zn原电池中,Zn片上发生___________ 反应(填“氧化”或“还原”)。 Cu片上发生的电极反应式为___________ 。
②外电路中电子流向___________ 极(填 “正”或“负”,下同); 内电路溶液中SO 移向
移向___________ 极。
(2)某原电池的总反应为Zn + Cu2+ = Cu + Zn2+,该原电池组成正确的是___________。
(3)某锂-空气电池的总反应为4Li + O2 + 2H2O = 4LiOH,其工作原理如图所示:
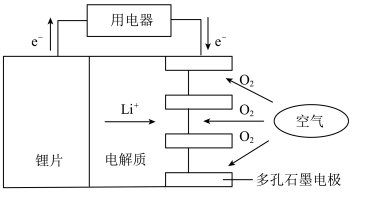
下列说法正确的是___________ 。
a.锂片作负极
b.O2发生氧化反应
c.正极的反应式为 O2 + 4e-+ 2H2O = 4OH-
(1)如图所示:

①在Cu-Zn原电池中,Zn片上发生
②外电路中电子流向
 移向
移向(2)某原电池的总反应为Zn + Cu2+ = Cu + Zn2+,该原电池组成正确的是___________。
A.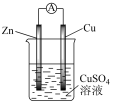 | B.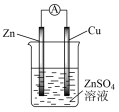 |
C. | D.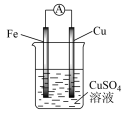 |

下列说法正确的是
a.锂片作负极
b.O2发生氧化反应
c.正极的反应式为 O2 + 4e-+ 2H2O = 4OH-
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。

(1)①氢气在燃烧时,放出大量热量,说明该反应是___ 热反应,这是由于反应物的总能量__ 生成物的总能量(填“大于”、“小于”或“等于”,下同);从化学反应的本质角度来看,由于断裂反应物中的化学键吸收的总能量__ 形成产物的化学键放出的总能量。
②通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,甲图就是能够实现该转化的装置,被称为氢氧燃料电池。该电池的正极是___ (填“a电极”或“b电极”),在负极发生的电极反应是__ 。
(2)①把锌粒投入盛有稀硫酸的敞口容器中,产生氢气的速率变化如图乙所示。时间a→b时段,产生氢气的速率增大的主要原因是___ 。
②按图丙所示装置进行实验,电子从__ (填“锌片”或“铜片”)流出,该电极上发生的电极反应式为:__ 。原电池工作一段时间后,溶液pH___ 。(填“增大”或“减小”)。
(3)能源是当今社会发展的三大支柱之一。有专家指出:如果对燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为___ (填序号)。
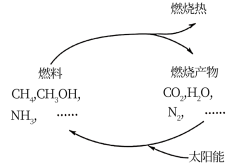
A.热能 B.电能 C.化学能 D.生物质能

(1)①氢气在燃烧时,放出大量热量,说明该反应是
②通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,甲图就是能够实现该转化的装置,被称为氢氧燃料电池。该电池的正极是
(2)①把锌粒投入盛有稀硫酸的敞口容器中,产生氢气的速率变化如图乙所示。时间a→b时段,产生氢气的速率增大的主要原因是
②按图丙所示装置进行实验,电子从
(3)能源是当今社会发展的三大支柱之一。有专家指出:如果对燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为

A.热能 B.电能 C.化学能 D.生物质能
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】美国阿波罗宇宙飞船上使用了一种新型发电装置——氢氧燃料电池,其构造如图所示,其中A、B两个电极均由多孔的碳块组成。
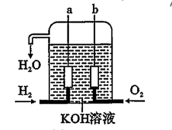
(1)①该电池的正极通入的气体是______ ,一段时间后正极区域溶液的pH值将________ ,负极的电极反应方程式为__________ 。
②若该电池工作时溶液中增加了1 mol H2O,则理论上电路中通过电子的物质的量为____ 。
(2)若将反应:Cu+2FeCl3=CuCl2+2FeCl2,设计成原电池。请写出负极材料_________ ,正极的电极反应方程式为__________ 。
(3)锌锰电池以锌皮、石墨棒为电极材料,电池工作时电流从____ 流向____ (填“锌皮”或“石墨棒”)

(1)①该电池的正极通入的气体是
②若该电池工作时溶液中增加了1 mol H2O,则理论上电路中通过电子的物质的量为
(2)若将反应:Cu+2FeCl3=CuCl2+2FeCl2,设计成原电池。请写出负极材料
(3)锌锰电池以锌皮、石墨棒为电极材料,电池工作时电流从
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】能源是现代文明的原动力,化学电池在生产生活中有着广泛的应用。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是_______ (填标号)。
A.C(s)+H2O(g)=CO(g)+H2(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2CO(g)+O2(g)=2CO2(g)
(2)为了探究化学反应中的能量变化,某同学设计了如图所示两个实验。有关实验现象,下列说法正确的是___________(填标号)。
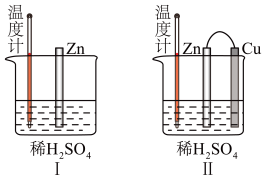
(3)图Ⅱ中外电路中的电子是从_______ (填“Zn”或“Cu”)电极经导线流向_______ 电极。若反应过程中有0.2 mol电子发生转移,则生成的氢气在标准状况下的体积为___________ 。若电池的总反应为2Fe3++Cu=2Fe2++Cu2+,则负极材料是______ (填化学式),正极反应式为_______________
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为CH4燃料电池示意图,工作时电子流向如图所示。

写出电极A的电极反应式_______ ,电极A附近pH如何变化?_______ (填“变大”或“变小”)。
(1)根据构成原电池的本质判断,下列反应可以设计成原电池的是
A.C(s)+H2O(g)=CO(g)+H2(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2CO(g)+O2(g)=2CO2(g)
(2)为了探究化学反应中的能量变化,某同学设计了如图所示两个实验。有关实验现象,下列说法正确的是___________(填标号)。

| A.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| B.图Ⅱ中产生气体的速率比图Ⅰ快 |
| C.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| D.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
(4)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计如图为CH4燃料电池示意图,工作时电子流向如图所示。

写出电极A的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现代社会应用最广泛的能源之一。
(1)某原电池装置如图所示:
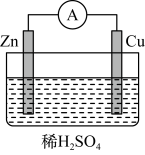
①负极反应是___________ 。
②电子由___________ 片通过导线流向___________ 片。(填化学式)
③一段时间后,溶液的pH___________ 。(填“增大”或“减小”)
④溶液中的H+向___________ 片移动。(填化学式)
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:

请回答下列问题:
①电极X的材料是___________ (填化学式) ;正极上发生的电极反应式为___________ ;
②当导线中通过了0.1mol电子时,银棒增重___________ g
(1)某原电池装置如图所示:

①负极反应是
②电子由
③一段时间后,溶液的pH
④溶液中的H+向
(2)依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示:

请回答下列问题:
①电极X的材料是
②当导线中通过了0.1mol电子时,银棒增重
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如下图设计的串联电池装置,R为变阻器,以调节电路电流。
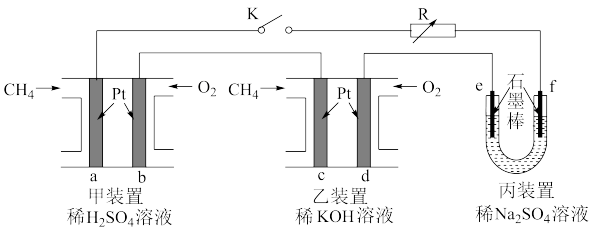
(1)写出b、c电极的电极反应式:b______________ ,c_______________ ;
(2)写出f电极的电极反应式____________________ ,向此电极区域滴入酚酞的现象为:_____________ ;该电极区域水的电离平衡被____________ (填“促进”、“抑制”或“无影响”)。
(3)闭合K一段时间后,丙装置的电解质溶液pH__________ (填“变大”、“变小”或“不变”),原因是______________ 。
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入______ g H2O就可以将析出的沉淀溶解并恢复到原有浓度。

(1)写出b、c电极的电极反应式:b
(2)写出f电极的电极反应式
(3)闭合K一段时间后,丙装置的电解质溶液pH
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某化学兴趣小组为探究 元素不同化合价的物质的转化,设计了如图装置,回答下列问题:
元素不同化合价的物质的转化,设计了如图装置,回答下列问题:
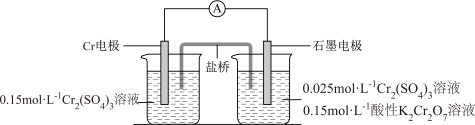
(1)该装置工作时,电子由___________ (填“Cr””或“石墨”,下同)电极经导线转移到___________ 电极。
(2)部分离子在溶液中的迁移速率如表:
①盐桥的作用是___________ 。
②根据上表数据分析盐桥中最好选择 作为电解质的原因:
作为电解质的原因:___________ ;该装置工作时,盐桥中向负极移动的离子为___________ (填离子符号)。
(3)设烧杯内液体体积均为 ,反应
,反应 时,
时, 电极质量减少
电极质量减少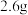 ,石墨电极一侧
,石墨电极一侧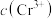 变为
变为 。假设
。假设 不迁移。
不迁移。
①石墨电极上发生的电极反应为___________ 。
②该装置的电子的有效利用率为___________  。
。
 元素不同化合价的物质的转化,设计了如图装置,回答下列问题:
元素不同化合价的物质的转化,设计了如图装置,回答下列问题:
(1)该装置工作时,电子由
(2)部分离子在溶液中的迁移速率如表:
| 阳离子 | 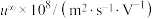 | 阴离子 | 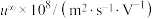 |
 | 4.07 |  | 4.61 |
 | 5.19 |  | 7.4 |
 | 6.59 |  | 7.91 |
 | 7.62 |  | 8.27 |
②根据上表数据分析盐桥中最好选择
 作为电解质的原因:
作为电解质的原因:(3)设烧杯内液体体积均为
 ,反应
,反应 时,
时, 电极质量减少
电极质量减少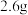 ,石墨电极一侧
,石墨电极一侧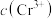 变为
变为 。假设
。假设 不迁移。
不迁移。①石墨电极上发生的电极反应为
②该装置的电子的有效利用率为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
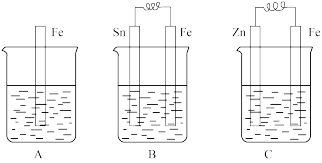
(1)A中反应的离子方程式为_________________________________ 。
(2)B中Fe极为_______ 极,电极反应式为_______________________ 。C中Fe极为_______ 极,电极反应式为__________________________ ,电子从_______ 极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________ 。

(1)A中反应的离子方程式为
(2)B中Fe极为
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
您最近一年使用:0次



