A、B、C、D、E、F、G、H八种元素都是前4周期元素,且原子序数依次增大。已知:元素A的原子中没有成对电子。元素B、C、D同周期,元素B、G同主族,且B、D、G三原子P轨道上均有2个未成对电子元素E、F、G在同一周期,且E原子中没有未成对电子。元素H的基态原子核外有6个未成对电子。
请回答下列问题:
(1)B、C、D三元素的电负性由大到小排列顺序为_______ (用元素符号表示);E、F、G三元素的原子的第一电离能由大到小排列顺序为_______ (用元素符号表示)。
(2)元素D与G所形成的晶体和元素D与B所形成的晶体熔沸点由高到低的顺序为___ (填化学式),其原因是_________ 。
(3)元素B与C的气态氢化物在A B中溶解性由大到小的顺序为
B中溶解性由大到小的顺序为___ (填化学式),其原因是________ 。
(4)B、D两元素形成的阴离子BD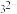 中的B的杂化类型为
中的B的杂化类型为______ ,空间结构为______ ,与BD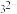 互为等电子体且含C、D两元素的微粒的化学式为
互为等电子体且含C、D两元素的微粒的化学式为______ 。
(5)A、B、C三元素各一个原子形成的分子中 键与
键与 键的个数比为
键的个数比为______ ,该分子的VSERR模型______ 。
(6)元素H的基态原子的核外电子排布为_______ ,在周期表中处于_____ 区。
请回答下列问题:
(1)B、C、D三元素的电负性由大到小排列顺序为
(2)元素D与G所形成的晶体和元素D与B所形成的晶体熔沸点由高到低的顺序为
(3)元素B与C的气态氢化物在A
 B中溶解性由大到小的顺序为
B中溶解性由大到小的顺序为(4)B、D两元素形成的阴离子BD
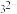 中的B的杂化类型为
中的B的杂化类型为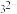 互为等电子体且含C、D两元素的微粒的化学式为
互为等电子体且含C、D两元素的微粒的化学式为(5)A、B、C三元素各一个原子形成的分子中
 键与
键与 键的个数比为
键的个数比为(6)元素H的基态原子的核外电子排布为
2011·陕西西安·三模 查看更多[1]
(已下线)2011届陕西省西安市高三第三次质检(理综)化学部分
更新时间:2016-12-09 01:48:55
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A原子核内只有1个质子;B原子半径是其所在主族中最小的,B的最高价氧化物对应的水化物的化学式为HBO3;C原子最外层的电子数比次外层的多4;C的简单阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C;C、E同主族。回答下列问题:
(1)B在元素周期表中的位置为______________________ 。
(2)E的氧化物对应的水化物有______________________ (写化学式)。
(3)B、C、D、E形成的简单离子半径由大到小的关系是______________________ (用离子符号表示)。
(4)化合物D2C的形成过程为______________________ (用电子式表示)。
(5)由A、B、C三种元素形成的常见的离子化合物的化学式为___________ ,该化合物的水溶液与强碱溶液共热发生反应的离子方程式为______________________ 。
(6)化合物D2EC3在一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为______________________ 。
(1)B在元素周期表中的位置为
(2)E的氧化物对应的水化物有
(3)B、C、D、E形成的简单离子半径由大到小的关系是
(4)化合物D2C的形成过程为
(5)由A、B、C三种元素形成的常见的离子化合物的化学式为
(6)化合物D2EC3在一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】Q、W、X、Y、Z为五种原子序数依次增大的短周期元素。已知:
①Q原子的核外电子数等于电子层数,且与W组成的一种化合物是沼气的主要成分;
②元素X的最高价氧化物的水化物和其气态氢化物能够反应,生成离子化合物甲;
③W与Y组成的化合物乙,是机动车排出的大气污染物之一,也是造成“雾霾”天气的物质之一;
④Y与Z能形成电子总数为30和38的两种离子化合物,分别为丙和丁。
(1)丁的电子式是__________ 。
(2)WY2与Z2Y2反应的化学方程式是_________________________________________ 。
(3)甲在水溶液中的水解方程式为______________________________________ 。
(4)写出一种实验室制取XQ3的方法__________________________________ 。(用化学方程式表示)
(5)标准状况下22.4L X的气态氢化物,与0.5L 1mol/L的X最高价氧化物的水化物反应,所得溶液中离子浓度由大到小的顺序是________________________________________ (用化学式表示)。
①Q原子的核外电子数等于电子层数,且与W组成的一种化合物是沼气的主要成分;
②元素X的最高价氧化物的水化物和其气态氢化物能够反应,生成离子化合物甲;
③W与Y组成的化合物乙,是机动车排出的大气污染物之一,也是造成“雾霾”天气的物质之一;
④Y与Z能形成电子总数为30和38的两种离子化合物,分别为丙和丁。
(1)丁的电子式是
(2)WY2与Z2Y2反应的化学方程式是
(3)甲在水溶液中的水解方程式为
(4)写出一种实验室制取XQ3的方法
(5)标准状况下22.4L X的气态氢化物,与0.5L 1mol/L的X最高价氧化物的水化物反应,所得溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。上述物质有如图转化关系如图所示。
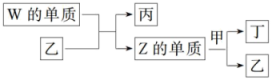
(1)Y、Z元素分别为_______ 、_______ (填元素符号)
(2)丙的水溶液刻蚀玻璃的化学反应方程式是_______
(3)X与Y还可以结合形成Y2X4分子,Y2X4的电子式为_______ ,Y的化合价为_______ 。实验室可用次氯酸钠溶液与甲反应制备Y2X4,反应的化学方程式为_______ 。
(4)下列关于元素及其化合物性质的判断中,正确的是_______ (填序号)
A.元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
B.金属元素A、B能分别形成+2、+3价离子,所以氧化性:A2+<B3+
C.因为 ,所以金属性:Pb>Fe
,所以金属性:Pb>Fe
D.因为 ,所以非金属性:Cl>S
,所以非金属性:Cl>S
E.因为水溶液的酸性:HmA>HnB,所以非金属性:A>B
F.HCl是一元酸,而H2SO4是二元酸,所以酸性:H2SO4>HCl
(5)某同学查阅资料知:甲的分解温度在850℃以上,甲烷(CH4)的分解温度是655℃,据此得出结论:Y元素的非金属性强于碳元素。该同学通过实验间接证明了自己的结论。你认为该同学的实验方案是(请结合离子方程式简要说明):_______ 。

(1)Y、Z元素分别为
(2)丙的水溶液刻蚀玻璃的化学反应方程式是
(3)X与Y还可以结合形成Y2X4分子,Y2X4的电子式为
(4)下列关于元素及其化合物性质的判断中,正确的是
A.元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
B.金属元素A、B能分别形成+2、+3价离子,所以氧化性:A2+<B3+
C.因为
 ,所以金属性:Pb>Fe
,所以金属性:Pb>FeD.因为
 ,所以非金属性:Cl>S
,所以非金属性:Cl>SE.因为水溶液的酸性:HmA>HnB,所以非金属性:A>B
F.HCl是一元酸,而H2SO4是二元酸,所以酸性:H2SO4>HCl
(5)某同学查阅资料知:甲的分解温度在850℃以上,甲烷(CH4)的分解温度是655℃,据此得出结论:Y元素的非金属性强于碳元素。该同学通过实验间接证明了自己的结论。你认为该同学的实验方案是(请结合离子方程式简要说明):
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】(1)含碳物质不完全燃烧会产生CO。血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒,写出铁离子(Fe3+)的核外电子排布式为_____________ ,CO有多种等电子体,其中常见的一种分子是__________ 。利用CO可以合成化工原料COCl2、配合物Fe(CO)5等,已知一个COCl2分子中每个原子最外层都形成8电子的稳定结构,则一个COCl2分子内含有_____ 个δ键,C原子的杂化方式为__________ 。Fe(CO)5等在一定条件下分解生成CO和铁,反应过程中断裂的化学键是__________ ,形成的化学键是___________ 。
(2)A、B均为短周期金属元素。依据下表数据,回答问题:
写出A原子的电子排布图_______________ ,Al原子的第一电离能_____ (填:“大于”、“小于”或“等于”)738 kJ·mol-1,原因是_________________ 。
(2)A、B均为短周期金属元素。依据下表数据,回答问题:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。
请回答下列问题:
(1)Ti的基态原子价电子排布式为_______ 。
(2)纳米TiO2常用作下述反应的催化剂。
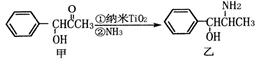
化合物甲的分子中采取sp2方式杂化的碳原子有_______ 个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为_______ 。
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2·H2O,其配离子中含有的化学键类型是_______ ,1 mol该配合物中含有的 键数目是
键数目是_______ 。
(4)通过X—射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据如下:
KCl、MgO、CaO、TiN四种离子晶体熔点由高到低的顺序为_______ 。
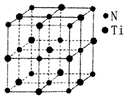
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有_______ 个:Ti原子的配位数为_______ ;此配位原子构成的空间构型为_______ ;该晶胞中N、Ti原子之间的最近距离为a nm。则该氮化钛晶体的密度为_______ g·cm-3、NA为阿伏伽德罗常数的值,只列计算式)。
请回答下列问题:
(1)Ti的基态原子价电子排布式为
(2)纳米TiO2常用作下述反应的催化剂。

化合物甲的分子中采取sp2方式杂化的碳原子有
(3)含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2·H2O,其配离子中含有的化学键类型是
 键数目是
键数目是(4)通过X—射线探知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(5)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】中科院大连化物所化学研究团队在化学链合成NH3研究方面取得新进展,该研究中涉及的物质有Ni-BaH2/Al2O3、Fe-K2O-Al2O3、Cs-Ru/MgO等,相关研究成果发表于《自然》上。请回答下列问题:
(1)Fe的基态原子共有_______ 种不同能级的电子,其最高能级的电子云形状是_______ 。
(2)氮原子的电子排布图表示的状态中,能量最低的是_______(填字母)。
(3)一种含Cu、S元素的有机物的结构简式如图所示,N原子的杂化方式为_______ 。
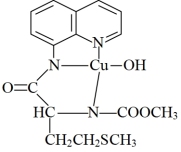
(4)元素的第一电离能:Mg_______ (填“>”或“<”)Al;N、O的电负性由大到小的顺序为_______ (用元素符号表示)。
(5)某镍白铜合金的立方晶胞结构如图所示:
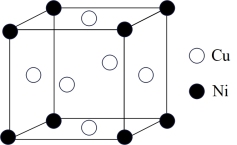
①该合金的化学式为_______ 。
②若该合金的晶胞边长为anm,则该合金的密度为_______ g·cm-3(设NA为阿伏加德罗常数的值)。
(1)Fe的基态原子共有
(2)氮原子的电子排布图表示的状态中,能量最低的是_______(填字母)。
A.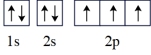 | B.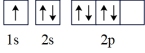 |
C.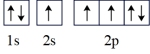 | D.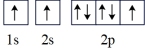 |

(4)元素的第一电离能:Mg
(5)某镍白铜合金的立方晶胞结构如图所示:

①该合金的化学式为
②若该合金的晶胞边长为anm,则该合金的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为_____________ 。元素Mn与O中,第一电离能较大的是_________ ,基态原子核外未成对电子数较多的是_________________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为__________ 和__________ 。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_________________ ,原因是______________________________ 。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在________ 。
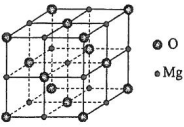
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为________ nm。MnO也属于NaCl型结构,晶胞参数为a' =0.448 nm,则r(Mn2+)为________ nm。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420 nm,则r(O2-)为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。
(1)以 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_______ 。
②实际生产中采用铁的氧化物 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
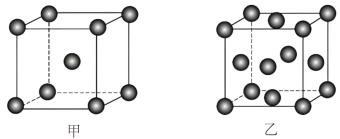
ⅰ.晶胞甲、乙所含铁原子个数比为_______ 。
ⅱ.晶胞甲的棱长为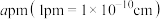 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞的密度
,则该晶胞的密度
_______  。
。
③我国科学家开发出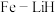 等双中心催化剂,在合成
等双中心催化剂,在合成 中显示出高催化活性。第一电离能(
中显示出高催化活性。第一电离能( ):
):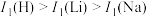 ,原因是
,原因是_______ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱: 。
。
①1体积水可溶解1体积 ,1体积水可溶解约700体积
,1体积水可溶解约700体积 。
。 极易溶于水的原因是“相似相溶”和
极易溶于水的原因是“相似相溶”和_______ 。
②反应时,向饱和NaCl溶液中先通入_______ (填化学式)。
③ 分解得
分解得 。
。 空间结构为
空间结构为_______ 。
(3) 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
① 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为_______ 。
② 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是_______ (填元素符号)。
③原子半径B_______ N(填“>”或“<”)。
 具有易液化、含氢密度高、应用广泛等优点,
具有易液化、含氢密度高、应用广泛等优点, 的合成及应用一直是科学研究的重要课题。
的合成及应用一直是科学研究的重要课题。(1)以
 、
、 合成
合成 ,Fe是常用的催化剂。
,Fe是常用的催化剂。①基态Fe原子的电子排布式为
②实际生产中采用铁的氧化物
 、FeO,使用前用
、FeO,使用前用 和
和 的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
ⅰ.晶胞甲、乙所含铁原子个数比为
ⅱ.晶胞甲的棱长为
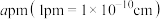 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞的密度
,则该晶胞的密度
 。
。③我国科学家开发出
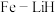 等双中心催化剂,在合成
等双中心催化剂,在合成 中显示出高催化活性。第一电离能(
中显示出高催化活性。第一电离能( ):
):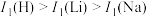 ,原因是
,原因是(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱:
 。
。①1体积水可溶解1体积
 ,1体积水可溶解约700体积
,1体积水可溶解约700体积 。
。 极易溶于水的原因是“相似相溶”和
极易溶于水的原因是“相似相溶”和②反应时,向饱和NaCl溶液中先通入
③
 分解得
分解得 。
。 空间结构为
空间结构为(3)
 、
、 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
 的中心原子的杂化轨道类型为
的中心原子的杂化轨道类型为②
 存在配位键,提供空轨道的是
存在配位键,提供空轨道的是③原子半径B
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钙铜合金可用作电解法制备金属钙的阴极电极材料。回答下列问题:
(1)铜在元素周期表中位于_______ (填“s”、“p”、“d”或“ds”)区。
(2)基态Ca原子的价电子排布式为_______ 。Co与Ca位于同一周期,且最外层电子数相同,但金属Co的熔点、沸点均比金属Ca的高,原因是_______ 。
(3)硫酸铜稀溶液呈蓝色,则硫酸铜稀溶液中不存在的作用力有_______ (填标号),其中硫酸根的空间构型为_______ 。
A.配位键 B.金属键 C.共价键 D.氢键 E.范德华力
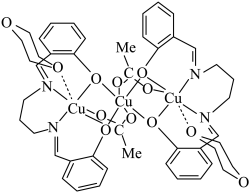
(4)Cu的一种配位化合物(Me为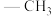 )的结构如图所示,其中Cu的配位数为
)的结构如图所示,其中Cu的配位数为_______ ,碳原子的杂化类型为_______ ,C、N、O的第一电离能从小到大的顺序是_______ (填元素符号)。
(5)一种钙铜合金的结构如图(III可看作是由I、II两种原子层交替堆积排列而形成的,其晶胞结构为IV)。
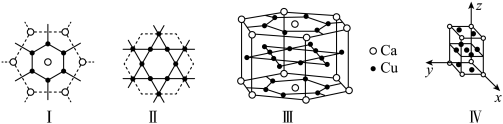
该钙铜合金中铜原子与钙原子的个数比为_______ ;晶体的坐标系称为晶轴系,晶轴系以晶胞参数为晶轴的单位向量如上图(IV),在图中画出上图(IV)中Cu原子沿z轴方向向x—y平面投影的位置_______ (用“ ”表示铜原子)。
”表示铜原子)。
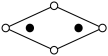
(1)铜在元素周期表中位于
(2)基态Ca原子的价电子排布式为
(3)硫酸铜稀溶液呈蓝色,则硫酸铜稀溶液中不存在的作用力有
A.配位键 B.金属键 C.共价键 D.氢键 E.范德华力
(4)Cu的一种配位化合物(Me为
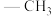 )的结构如图所示,其中Cu的配位数为
)的结构如图所示,其中Cu的配位数为
(5)一种钙铜合金的结构如图(III可看作是由I、II两种原子层交替堆积排列而形成的,其晶胞结构为IV)。

该钙铜合金中铜原子与钙原子的个数比为
 ”表示铜原子)。
”表示铜原子)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硅材料和铝材料在生产生活中应用广泛。回答下列问题:
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.([Ne]3s23p2)、b.([Ne]3s23p1)、c.([Ne]3s23p14s1),半径由大到小的顺序为_______ (填标号);第三周期元素中,第一电离能介于Al和P之间的元素有_______ 种。
(2)N(SiH3)3是一种高介电常数材料。已知:N(SiH3)3中Si-N-Si键角120°,N(CH3)3中C-N-C键角111°。共价键的极性Si-N_______ C-N(填“>”、“=”或“<”)。下列划线原子与N(SiH3)3中N原子杂化类型相同的是_______ (填标号)。
A.Al(OCH3)3 B.NH3BH3 C.N(CH3)3 D.NH4NO3
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是_______ 。
(4)已知合金Na2AlAu3的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入Au3Al四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
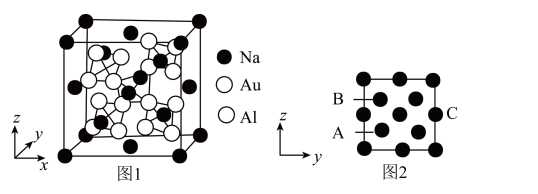
每个Na周围距离其最近的Na有_______ 个;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点的分数坐标为( ,
, ,
, ),则B点的分数坐标为
),则B点的分数坐标为_______ ;设NA为阿伏加德罗常数的值,Na2AlAu3的摩尔质量为Mg•mol-1,晶体的密度为ρg•cm-3,则A、C两原子间的距离为_______ pm(列出计算表达式)。
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.([Ne]3s23p2)、b.([Ne]3s23p1)、c.([Ne]3s23p14s1),半径由大到小的顺序为
(2)N(SiH3)3是一种高介电常数材料。已知:N(SiH3)3中Si-N-Si键角120°,N(CH3)3中C-N-C键角111°。共价键的极性Si-N
A.Al(OCH3)3 B.NH3BH3 C.N(CH3)3 D.NH4NO3
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是
(4)已知合金Na2AlAu3的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入Au3Al四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。

每个Na周围距离其最近的Na有
 ,
, ,
, ),则B点的分数坐标为
),则B点的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】镓与ⅤA族元素形成的化合物是重要的半导体材料,应用最广泛的是砷化镓(GaAs),回答下列问题:
(1)基态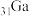 原子的核外电子排布式为
原子的核外电子排布式为___________ ,基态As原子核外有___________ 个未成对电子。
(2)镓失去电子的逐级电离能(单位: )的数值依次为577、1984.5、2961.8、6192由此可推知镓的主要化合价为
)的数值依次为577、1984.5、2961.8、6192由此可推知镓的主要化合价为___________ 和+3。砷的电负性比镓___________ (填“大”或“小”)。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:___________ 。
 的熔点超过1000℃,可能的原因
的熔点超过1000℃,可能的原因___________ 。
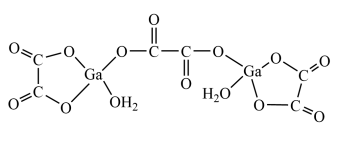
(4)二水合草-酸镓的结构如图所示,其中镓原子的配位数为___________ ,草酸根中碳原子的杂化方式为___________ 。
(5)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
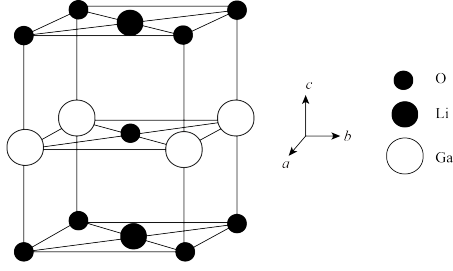
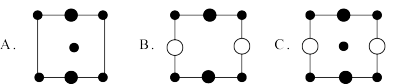
其化学式为___________ ,上述晶胞沿着a轴的投影图为___________ (填选项字母)。
(1)基态
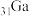 原子的核外电子排布式为
原子的核外电子排布式为(2)镓失去电子的逐级电离能(单位:
 )的数值依次为577、1984.5、2961.8、6192由此可推知镓的主要化合价为
)的数值依次为577、1984.5、2961.8、6192由此可推知镓的主要化合价为(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:
| 镓的卤化物 |  | 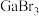 |  |
| 熔点/℃ | 77.75 | 122.3 | 211.5 |
| 沸点/℃ | 201.2 | 279 | 346 |
 的熔点超过1000℃,可能的原因
的熔点超过1000℃,可能的原因(4)二水合草-酸镓的结构如图所示,其中镓原子的配位数为

(5)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:

其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Ⅰ、氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。
(1)NF3,NBr3、NCl3这三种分子的空间构型是_______ 。
(2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子_______________ 。
(3)NaN3与KN3离子键强弱相比,NaN3_____ KN3(填“>”、“=”或“<” )。
(4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。

①写出氮化碳的化学式____________________ ;
②指出氮化碳的晶体类型___________________ 。
Ⅱ、分析表中四种物质的相关数据,请回答:
(1)CH4和SiH4比较,沸点高低的原因是________________________ ;
(2)NH3和PH3比较,分解温度高低的原因是____________________ ;
(3)结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时___________ 先液化。
(1)NF3,NBr3、NCl3这三种分子的空间构型是
(2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子
(3)NaN3与KN3离子键强弱相比,NaN3
(4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。

①写出氮化碳的化学式
②指出氮化碳的晶体类型
Ⅱ、分析表中四种物质的相关数据,请回答:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点/K | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度/K | 873 | 773 | 1073 | 713.2 |
(1)CH4和SiH4比较,沸点高低的原因是
(2)NH3和PH3比较,分解温度高低的原因是
(3)结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时
您最近一年使用:0次



