已知下列数据:
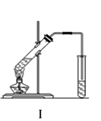
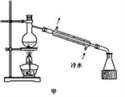

实验室制取乙酸乙酯的主要装置如上图I所示,主要步骤为:①在30mL的大试管中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到盛有10mL饱和Na2CO3溶液的(加入2滴酚酞试液)试管中;③小火加热试管中的混合液;④待小试管中收集约2mL产物时停止加热,撤出小试管并用力振荡,然后静置;⑤分离出纯净的乙酸乙酯。请回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是_____________________________ ;
(2)写出该实验制取乙酸乙酯的化学方程式_________________________________ ,浓H2SO4的作用是 _______________________ ;
(3)步骤③中,用小火加热试管中的混合液,其原因_________________________ ;
(4)步骤④所观察到的现象是___________________________________________________
(5)步骤⑤中,分离出乙酸乙酯的方法是_________________________________ ;
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取圆底烧瓶中产物)。你认为哪种装置更合理,为什么?_____ 。
| 物 质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 |
| 乙 醇 | -114 | 78.4 | 0.79 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.900 |
| 浓H2SO4 | 338 | 1.84 |



实验室制取乙酸乙酯的主要装置如上图I所示,主要步骤为:①在30mL的大试管中按体积比2:3:2的比例配制浓硫酸、乙醇和乙酸的混合液;②按照图I连接装置,使产生的蒸气经导管通到盛有10mL饱和Na2CO3溶液的(加入2滴酚酞试液)试管中;③小火加热试管中的混合液;④待小试管中收集约2mL产物时停止加热,撤出小试管并用力振荡,然后静置;⑤分离出纯净的乙酸乙酯。请回答下列问题:
(1)步骤①中,配制这一比例的混合液的操作是
(2)写出该实验制取乙酸乙酯的化学方程式
(3)步骤③中,用小火加热试管中的混合液,其原因
(4)步骤④所观察到的现象是
(5)步骤⑤中,分离出乙酸乙酯的方法是
(6)为提高乙酸乙酯的产率,甲、乙两位同学分别设计了如上图甲、乙的装置(乙同学待反应完毕冷却后再用饱和Na2CO3溶液提取圆底烧瓶中产物)。你认为哪种装置更合理,为什么?
更新时间:2018-06-03 10:19:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。完成下列填空:

(1)实验时,通常加入过量的乙醇,原因是__________ 。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是_______ ;浓硫酸用量又不能过多,原因是_______ 。
(2)饱和Na2CO3溶液的作用是_______________ 。
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,______ 、_______ ,然后分液。
(4)若用b装置制备乙酸乙酯,其缺点有__________ 、__________ 。由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________ ,分离乙酸乙酯与该杂质的方法是_______________ 。

(1)实验时,通常加入过量的乙醇,原因是
(2)饱和Na2CO3溶液的作用是
(3)反应结束后,将试管中收集到的产品倒入分液漏斗中,
(4)若用b装置制备乙酸乙酯,其缺点有
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】某人设计淀粉利用方案如下图1所示:
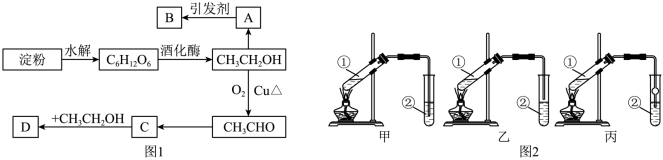
其中:A是乙烯能催熟水果,B是高分子化合物,D为乙酸乙酯.请回答以下问题:
(1)“C6H12O6”的名称是______ ,C中含有官能团名称 ______ ;
(2)A→CH3CH2OH反应类型______ ;C→D反应类型 ______ 。
检验CH3CHO的试剂可以是______ ,现象为 ________________________ 。
(3)写出下列转化的化学方程式
①A→CH3CH2OH:___________________________ ;
②CH3CH2OH→CH3CHO:___________________________ 。
(4)下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯图2,该反应的化学方程式为___________________________ 。
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置(如图2):
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是______ (填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是 ______ 。在试管②中加入5mL X试剂为 ______ (化学式)。

其中:A是乙烯能催熟水果,B是高分子化合物,D为乙酸乙酯.请回答以下问题:
(1)“C6H12O6”的名称是
(2)A→CH3CH2OH反应类型
检验CH3CHO的试剂可以是
(3)写出下列转化的化学方程式
①A→CH3CH2OH:
②CH3CH2OH→CH3CHO:
(4)下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【实验原理】甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯图2,该反应的化学方程式为
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置(如图2):
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】乙酸乙酯是一种用途广泛的精细化工产品。某课外小组设计实验室制取乙酸乙酯的方案如下:
已知:①无水氯化钙可与乙醇形成CaCl2·6C2H5OH。
②有关有机物的沸点:
③2CH3CH2OH CH3CH2OCH2CH3+H2O。
CH3CH2OCH2CH3+H2O。
制备过程:
装置如图所示,A中盛有浓硫酸,B中盛有9.5 mL无水乙醇和6 mL冰醋酸,D中盛有饱和碳酸钠溶液。

(1)写出乙酸与乙醇发生酯化反应的化学方程式:_______ 。
(2)实验过程中滴加大约3 mL浓硫酸,B的容积最合适的是_______(填字母)。
(3)球形干燥管的主要作用是_______ 。
(4)预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是_______ 。
已知:①无水氯化钙可与乙醇形成CaCl2·6C2H5OH。
②有关有机物的沸点:
| 有机物 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.5 | 79 | 118 | 77.1 |
 CH3CH2OCH2CH3+H2O。
CH3CH2OCH2CH3+H2O。制备过程:
装置如图所示,A中盛有浓硫酸,B中盛有9.5 mL无水乙醇和6 mL冰醋酸,D中盛有饱和碳酸钠溶液。

(1)写出乙酸与乙醇发生酯化反应的化学方程式:
(2)实验过程中滴加大约3 mL浓硫酸,B的容积最合适的是_______(填字母)。
| A.25 mL | B.50 mL | C.250 mL | D.500 mL |
(4)预先向饱和Na2CO3溶液中滴加几滴酚酞试液,目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】如下图是乙酸乙酯的合成路线图,已知B的水溶液可以溶解 ,E可作果实催熟剂。
,E可作果实催熟剂。
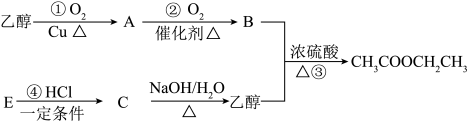
请完成下列问题:
(1)B中所含官能团的名称是___________ ,E的结构简式为:___________ ;反应④的反应类型是___________ 。
(2)实验室我们可以用如图所示的装置制取乙酸乙酯。回答下列问题。
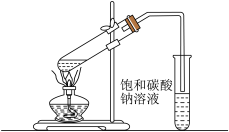
①写出制取乙酸乙酯的化学反应方程式:___________ ;
②试剂B、乙醇和浓硫酸的添加顺序为:___________ :
③装置中导管要在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是___________ ;
④如果用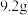 的乙醇和
的乙醇和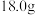 的B反应制得乙酸乙酯
的B反应制得乙酸乙酯 ,则本实验的产率是
,则本实验的产率是___________ ;(产率指的是某种生成物的实际产量与理论产量的比值)。
 ,E可作果实催熟剂。
,E可作果实催熟剂。
请完成下列问题:
(1)B中所含官能团的名称是
(2)实验室我们可以用如图所示的装置制取乙酸乙酯。回答下列问题。

①写出制取乙酸乙酯的化学反应方程式:
②试剂B、乙醇和浓硫酸的添加顺序为:
③装置中导管要在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
④如果用
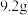 的乙醇和
的乙醇和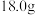 的B反应制得乙酸乙酯
的B反应制得乙酸乙酯 ,则本实验的产率是
,则本实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】“酒是陈的香”,就因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室中我们也可以用图所示的装置制取乙酸乙酯。请回答下列问题:

(1)该反应方程式是___________
(2)浓硫酸的作用是①___________ ,②___________
(3)试管a中需要加入浓硫酸、乙酸各2mL,乙醇3mL,正确的加入顺序为___________
A.浓硫酸、乙醇、乙酸 B.浓硫酸、乙酸、乙醇
C.乙醇、浓硫酸、乙酸 D.乙酸、浓硫酸、乙醇
(4)为了防止试管a中的液体在实验时发生暴沸,在试管加热前应采取的措施是___________
(5)试管b中加有饱和的碳酸钠溶液,其作用是___________
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是___________

(1)该反应方程式是
(2)浓硫酸的作用是①
(3)试管a中需要加入浓硫酸、乙酸各2mL,乙醇3mL,正确的加入顺序为
A.浓硫酸、乙醇、乙酸 B.浓硫酸、乙酸、乙醇
C.乙醇、浓硫酸、乙酸 D.乙酸、浓硫酸、乙醇
(4)为了防止试管a中的液体在实验时发生暴沸,在试管加热前应采取的措施是
(5)试管b中加有饱和的碳酸钠溶液,其作用是
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】乙酸苯甲酯是一种难溶于水,密度大于水的无色油状液体,具有茉莉花气味,可用做调香剂。
(一)以乙烯,甲苯为原料,合成乙苯甲酯的路线如图所示。
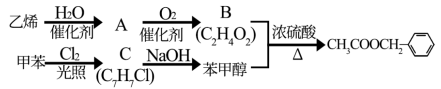
(1)写出由乙烯制备A的化学方程式_______________________________________________________ 。
(二)制备乙酸苯甲酯的流程如图:
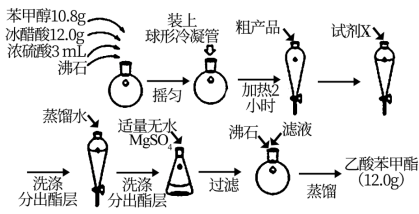
(2)球形冷凝管的作用为_______________________ .
(3)试剂X可为_______
A.氢氧化钠溶液 B.碳酸钠溶液 C.乙醇 D.氯化钠溶液
(4)分出酯层时应收集______ 层液体(填“上”或“下”)
(5)无水MgSO4的作用为__________________________ 。
(6)本实验所得乙酸苯甲酯的产率为__________ 。(已知:相对分子量:苯甲醇-108; 乙酸-60; 乙酸苯甲酯-150)
(一)以乙烯,甲苯为原料,合成乙苯甲酯的路线如图所示。

(1)写出由乙烯制备A的化学方程式
(二)制备乙酸苯甲酯的流程如图:

(2)球形冷凝管的作用为
(3)试剂X可为
A.氢氧化钠溶液 B.碳酸钠溶液 C.乙醇 D.氯化钠溶液
(4)分出酯层时应收集
(5)无水MgSO4的作用为
(6)本实验所得乙酸苯甲酯的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醛在医药、染料、香料等行业中都有着广泛的应用。实验室通过如图所示的流程由甲苯氧化制备苯甲醛,试回答下列问题。

(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是___ 。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的是___ 。
(3)实验过程中,可循环使用的物质有___ 。
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是___ 。

(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的是
(3)实验过程中,可循环使用的物质有
(4)实验中分离甲苯和苯甲醛采用的操作Ⅰ是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】以淀粉为主要原料合成一种具有果香味有机物C和高分子化合物E的合成路线如下图所示。

请回答下列问题:
(1)写出E的结构简式_______________ ,D分子内含有的官能团是______ (填名称)。
(2)写出下列反应的反应类型:②_________________ ,④_________________ 。
(3)写出下列反应的化学方程式:
①____________________________________________________________________ ;
③____________________________________________________________________ 。
(4)某同学欲用入图装置制备物质C,试管B中装有足量的饱和碳酸钠溶液的目的是:_________________________________________ ;插入试管B的导管接有一个球状物,其作用为___________________ ;如需将试管B中的物质C分离出来,用到的主要玻璃仪器有:烧杯、__________________ 。


请回答下列问题:
(1)写出E的结构简式
(2)写出下列反应的反应类型:②
(3)写出下列反应的化学方程式:
①
③
(4)某同学欲用入图装置制备物质C,试管B中装有足量的饱和碳酸钠溶液的目的是:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某校兴趣小组采用类似制乙酸乙酯的装置(如图),由环己醇制备环己烯,其反应原理为 。环己醇和环己烯的部分性质见下表:
。环己醇和环己烯的部分性质见下表:
| 有机物 | 密度/(g·cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环已烯 | 0.81 | -103 | 83 | 难溶于水 |
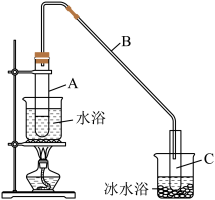
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后加入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品(含有环己醇和少量酸性杂质)。
①导管B的作用是
②加入碎瓷片的目的是
(2)制备精品
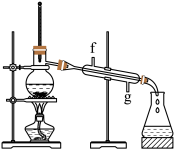
②将所得的环己烯按如图装置蒸馏,蒸馏时要加入生石灰,其目的是
③收集产品时,应控制温度在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时部分环己醇随产品一起蒸出
④区分环己烯精品和粗品的试剂是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:

已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有____ (任写一种)。
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:____ 。
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为____ ,若加 A 后溶液的 pH调为5,则溶液中 Fe3+的浓度为____ mol/L。
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:____ 。
(5)“赶氨”时,最适宜的操作方法是____ 。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是____ (写化学式)。
(7)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是____ 。

已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的化学方程式:
(3)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为
(4)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:
(5)“赶氨”时,最适宜的操作方法是
(6)滤液Ⅱ经蒸发结晶得到的盐主要是
(7)过滤Ⅱ得到的沉淀经过洗涤、干燥可以得到碱式碳酸铜,判断沉淀是否洗净的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】结合所学相关知识,完成以下实验题。已知铁屑和氯气在500~600 ℃下可制取无水FeCl3,如图是制取氯化铁粉末所需的装置,已知氯化铁粉末容易吸水生成结晶化合物:FeCl3+6H2O=FeCl3·6H2O。请回答下列问题。
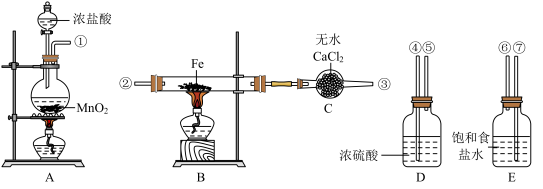
(1)按照气体流向从左到右的顺序连接仪器(填仪器接口):_____ ,①接___,___接___,___接②。
(2)A装置的烧瓶中发生反应的离子方程式为______ ,B装置中发生反应的化学方程式为______ 。
(3)D装置的作用是_________ ;E装置的作用是___________ 。
(4)实验开始时,应先点燃_______ (填“A”或“B”)处的酒精灯。
(5)这套实验装置是否完整?______ (填“是”或“否”)。若不完整,还须补充_____ (若第一空填“是”,则此空不需要作答)装置。
(6)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为___________ ,已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓)= CaCl2+2Cl2↑+2H2O。用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是___________ (填序号)。
①CO2 ②HCl ③H2O ④H2

(1)按照气体流向从左到右的顺序连接仪器(填仪器接口):
(2)A装置的烧瓶中发生反应的离子方程式为
(3)D装置的作用是
(4)实验开始时,应先点燃
(5)这套实验装置是否完整?
(6)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学方程式为
①CO2 ②HCl ③H2O ④H2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼钢的阳极泥(主要含有TeO2、少量Ag、 Au)为原料制备单质碲的一种工艺流程如下:
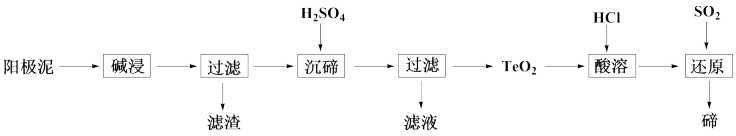
已知Te02微溶于水,易溶于较浓的强酸和强碱。
(1)“碱浸”时所用的试剂是___ (填化学式)。
(2)碱浸后的“滤渣”可用于____ 。
(3)“沉碲”时,缓慢加入H2SO4,并不断搅拌。为生成TeO2沉淀需控制溶液的pH为4.5—5.0,其原因是____ 。
(4)“酸溶”后,将SO2通入TeC14酸性溶液中进行“还原”得到碲,该反应的化学方程式是____ 。
(5) 25℃时,亚碲酸(H2Te03)的Kal=lxl0-3,Ka2=2×l0-8
①0.lmol/L的NaHTe03的溶液中c(TeO32-) - c(H2TeO3)=____ (填离子浓度表达式)。
②0.lmol.L-1的NaHTe03溶液呈__________ 填“酸性”,“碱性”,“中性”)理由是____ (写出利用平衡常数计算及推理过程).

已知Te02微溶于水,易溶于较浓的强酸和强碱。
(1)“碱浸”时所用的试剂是
(2)碱浸后的“滤渣”可用于
(3)“沉碲”时,缓慢加入H2SO4,并不断搅拌。为生成TeO2沉淀需控制溶液的pH为4.5—5.0,其原因是
(4)“酸溶”后,将SO2通入TeC14酸性溶液中进行“还原”得到碲,该反应的化学方程式是
(5) 25℃时,亚碲酸(H2Te03)的Kal=lxl0-3,Ka2=2×l0-8
①0.lmol/L的NaHTe03的溶液中c(TeO32-) - c(H2TeO3)=
②0.lmol.L-1的NaHTe03溶液呈
您最近一年使用:0次



