在通常条件下,下列各组物质的性质排列正确的是
| A.熔点:SiO2>CCl4>S |
| B.晶格能由大到小:MgC12>MgO>NaCl |
| C.沸点:NaCl>乙酸>硝酸 |
| D.热稳定性:HF<H2O<NH3 |
更新时间:2018/07/04 12:48:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 的分子结构如图所示,下列有关说法错误的是
的分子结构如图所示,下列有关说法错误的是
 的分子结构如图所示,下列有关说法错误的是
的分子结构如图所示,下列有关说法错误的是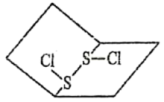
A. 是极性分子 是极性分子 |
B. 分子中,S为+1价,Cl为-1价 分子中,S为+1价,Cl为-1价 |
C. 的相对分子质量比 的相对分子质量比 大,熔、沸点高 大,熔、沸点高 |
D. 分子中既含有极性键又含有非极性键 分子中既含有极性键又含有非极性键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
A. 分子中 分子中 键与 键与 键个数比为1∶1 键个数比为1∶1 |
B. 的稳定性高,是因为水分子间存在氢键 的稳定性高,是因为水分子间存在氢键 |
| C.键长等于成键两原子的半径之和 |
| D.分子之间可能存在化学键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于晶体的说法中,不正确的是( )
①晶胞是晶体结构的基本单元
②含有离子的晶体一定是离子晶体
③共价键的强弱决定分子晶体熔沸点的高低
④分子晶体的熔点一定比金属晶体低
⑤MgO远比NaCl的晶格能大
⑥含有共价键的晶体一定是原子晶体
①晶胞是晶体结构的基本单元
②含有离子的晶体一定是离子晶体
③共价键的强弱决定分子晶体熔沸点的高低
④分子晶体的熔点一定比金属晶体低
⑤MgO远比NaCl的晶格能大
⑥含有共价键的晶体一定是原子晶体
| A.①③④⑤ | B.②③④⑥ | C.②③⑤⑥ | D.③④⑤⑥ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】“类推”是一种重要的学习方法,但有时会产生错误结论,下列类推结论中正确的是
| A.碱金属氟化物的晶格能顺序是LiF>NaF>KF>RbF>CsF;则钠的卤化物的晶格能顺序是NaF>NaCl>NaBr>NaI |
| B.ⅣA族元素氢化物沸点顺序是GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序是AsH3>PH3>NH3 |
| C.晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 |
| D.若盐酸的浓度是醋酸浓度的2倍;则盐酸中H+浓度也是醋酸中H+浓度的2倍 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在通常条件下,下列各组物质的性质排列正确的是
| A.熔点: KCl>SiO2> SO2 | B.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl |
| C.沸点:正戊烷>异戊烷>新戊烷 | D.水溶性:HCl>H2S> SO2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法错误的是
| A.构成共价晶体的原子,其原子半径越小晶体的硬度越大 |
| B.通常情况下固体不导电、熔化时导电的晶体为离子晶体 |
| C.H2O和PH3化学键类型和晶体类型均相同 |
| D.金属晶体和离子晶体中都存在微粒间强烈的相互作用,都有延展性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】利用反应CCl4+4Na C(金刚石)+4NaCl可实现人工合成金刚石。下列说法错误的是
C(金刚石)+4NaCl可实现人工合成金刚石。下列说法错误的是
 C(金刚石)+4NaCl可实现人工合成金刚石。下列说法错误的是
C(金刚石)+4NaCl可实现人工合成金刚石。下列说法错误的是| A.熔化金刚石时,破坏共价键 |
| B.金刚石的网状结构中,最小的环为六元环 |
| C.NaCl晶体中每个Cl-周围有12个Na+ |
| D.CCl4和C(金刚石)中C的杂化方式相同 |
您最近半年使用:0次

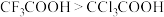
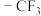 的极性大于
的极性大于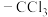 的极性,导致
的极性,导致 的羧基中的羟基的极性更大,更易电离出
的羧基中的羟基的极性更大,更易电离出


