有可逆反应Fe(s)+CO2(g) FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
 FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是
FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2。则下列说法不正确的是| A.该反应的平衡常数表达式为K=c(CO)/c(CO2) |
| B.该反应的逆反应是放热反应 |
| C.v正(CO2)=v逆(CO)时该反应达到平衡状态 |
| D.c(CO2):c(CO)=1:1时该反应达到平衡状态 |
更新时间:2018-07-18 16:03:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】对可逆反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),下列叙述正确的是
| A.达到化学平衡时,4v正(NH3)=5v逆(H2O) |
| B.若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率减小 |
| D.达到平衡时,若减小容器体积,则NH3的转化率会增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,在恒容密闭容器中发生反应: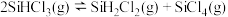 。
。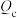 表示某时刻的浓度商,K为该温度下的平衡常数。下列情况能说明该反应一定达到化学平衡状态的是
表示某时刻的浓度商,K为该温度下的平衡常数。下列情况能说明该反应一定达到化学平衡状态的是
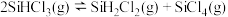 。
。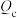 表示某时刻的浓度商,K为该温度下的平衡常数。下列情况能说明该反应一定达到化学平衡状态的是
表示某时刻的浓度商,K为该温度下的平衡常数。下列情况能说明该反应一定达到化学平衡状态的是A. |
| B.体系内物质的总质量保持不变 |
C. 、 、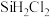 、 、 同时在容器中存在 同时在容器中存在 |
D.单位时间内消耗  ,同时生成 ,同时生成 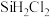 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】“碳达峰·碳中和”是我国社会发展的重大战略之一,CH4还原CO2是实现“双碳”经济的有效途径之一,相关主要反应有:
Ⅰ:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1
2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1
Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=+41kJ/mol,K2
CO(g)+H2O(g) ΔH2=+41kJ/mol,K2
下列说法正确的是
Ⅰ:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1
2CO(g)+2H2(g) ΔH1=+247kJ/mol,K1Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=+41kJ/mol,K2
CO(g)+H2O(g) ΔH2=+41kJ/mol,K2下列说法正确的是
A.反应Ⅰ的平衡常数K1=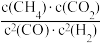 |
| B.反应Ⅱ的ΔS<0 |
| C.有利于提高CO2平衡转化率的条件是高温低压 |
| D.该工艺每转化0.2mol CO2可获得0.4molCO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一定温度下,将X和Y各0.16mol加入10L恒容密闭容器中,发生下列反应: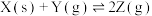
 。一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是
。一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是
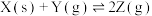
 。一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是
。一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.2min末的反应速率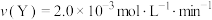 |
| B.7min时该反应恰好达到化学平衡状态 |
C.此反应的平衡常数表达式为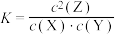 |
| D.其他条件不变,再充入0.1mol X、0.1mol Y、0.2mol Z,此时v(逆)>v(正) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列说法正确的是
| A.增大压强或升高温度,—定能使化学反应速率加快 |
| B.合成氨工业中,将氨气液化分离来可以提高正反应速率和产率 |
C.500°C、30 MPa下,0.5 mol N2(g)和1.5mol H2(g)反应生成NH3(g)放热QkJ,其热化学方程式为N2(g)+3 H2(g) 2 NH3(g)△H=-2QkJ/mol 2 NH3(g)△H=-2QkJ/mol |
D.已知两个平衡体系:2NiO(s) 2Ni(s)+O2(g)2CO(g)+O2(g) 2Ni(s)+O2(g)2CO(g)+O2(g) 2CO2(g)是平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g) 2CO2(g)是平衡常数分别为K1和K2,可推知平衡NiO(s)+CO(g) Ni(s)+CO2(g)的平衡常数为 Ni(s)+CO2(g)的平衡常数为 |
您最近一年使用:0次

 NO+SO3,达到平衡时,下列叙述正确的是
NO+SO3,达到平衡时,下列叙述正确的是

