CO2是重要的化工原料,也是应用广发的化工产品。CO2与过氧化钠或超氧化钾反应可产生氧气。
完成下列计算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。2.00 mol NH4HCO3完全分解,分解产物经干燥后的体积为_______ L(标准状况)。
(2)某H2中含有2.40 molCO2,该混合气体通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为_______ 。
(3)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2,4KO2+4CO2+2H2O→4KHCO3+3O2,若9 mol CO2在密封舱内和KO2反应后生成9 mol O2,则反应前密封舱内H2O的量应该是多少_______ ?列式计算。
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:CH4+H2O CO+3H2,已知:CO+2H2
CO+3H2,已知:CO+2H2 CH3OH,CO2+3H2
CH3OH,CO2+3H2 CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率
CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率_______ 。
完成下列计算:
(1)CO2通入氨水生成NH4HCO3,NH4HCO3很容易分解。2.00 mol NH4HCO3完全分解,分解产物经干燥后的体积为
(2)某H2中含有2.40 molCO2,该混合气体通入2.00 L NaOH溶液中,CO2被完全吸收。如果NaOH完全反应,该NaOH溶液的浓度为
(3)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2,4KO2+4CO2+2H2O→4KHCO3+3O2,若9 mol CO2在密封舱内和KO2反应后生成9 mol O2,则反应前密封舱内H2O的量应该是多少
(4)甲烷和水蒸气反应的产物是合成甲醇的原料:CH4+H2O
 CO+3H2,已知:CO+2H2
CO+3H2,已知:CO+2H2 CH3OH,CO2+3H2
CH3OH,CO2+3H2 CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率
CH3OH+H2O。300 mol CH4完全反应后的产物中,加入100 mol CO2后合成甲醇。若获得甲醇350 mol,残留氢气120 mol,计算CO2的转化率
2016·上海·高考真题 查看更多[6]
2016年全国普通高等学校招生统一考试化学(上海卷精编版)人教版2017届高三单元精练检测一化学试题(已下线)2019年高考化学一轮复习讲练测1.2 物质的量浓度 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【教学案】(已下线)2019高考备考二轮复习精品资料-专题2 化学常用计量(教学案)2016年全国普通高等学校招生统一考试化学(上海卷参考版)
更新时间:2016-12-09 15:45:42
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】有硫酸,硫酸亚铁、硫酸铁的混合溶液 ,已知溶液中各阳离子的物质的量浓度相等,
,已知溶液中各阳离子的物质的量浓度相等, 的物质的量浓度为
的物质的量浓度为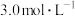 。
。
请计算:
(1)硫酸的物质的量浓度为________  。
。
(2)理论上此溶液最多可溶解铁粉的质量为________ g。
 ,已知溶液中各阳离子的物质的量浓度相等,
,已知溶液中各阳离子的物质的量浓度相等, 的物质的量浓度为
的物质的量浓度为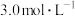 。
。请计算:
(1)硫酸的物质的量浓度为
 。
。(2)理论上此溶液最多可溶解铁粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)在标准状况下,0.5mol N2和1mol O2 的混合气体的体积约是_____ .
(2)标准状况下,气体的摩尔体积是______ ,0.5mol CO2 的质量是____ ,在标准状况下的体积是_____ .
(3)①标准状况下,2mol NH3与_______ g CO2的体积相等.
②等质量的O2和O3所含的原子个数之比是______ .
③用金属Na、Mg、Al与足量的稀盐酸反应,欲制取相同条件下等体积的H2,则需要金属Na、Mg、Al的质量比为_____ (最简整数比).
④已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的相对分子质量为__ .
(2)标准状况下,气体的摩尔体积是
(3)①标准状况下,2mol NH3与
②等质量的O2和O3所含的原子个数之比是
③用金属Na、Mg、Al与足量的稀盐酸反应,欲制取相同条件下等体积的H2,则需要金属Na、Mg、Al的质量比为
④已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的相对分子质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室常用的浓盐酸密度为1.08 g·mL-1,质量分数为36.5 %。
(1)此浓盐酸的物质的量浓度为__________________ 。
(2)取此浓盐酸50 mL,用蒸馏水稀释为200 mL,稀释后盐酸的物质的量浓度为_____ 。
(3)将13 g 锌投入足量的上述实验所得的稀盐酸中,充分反应后,求:(写出计算过程)
①放出的H2在标准状况下的体积____________ 。
②将生成的H2 通过足量的灼热CuO,求生成铜的质量_________ (假设氢气在反应中没有损失)。
(1)此浓盐酸的物质的量浓度为
(2)取此浓盐酸50 mL,用蒸馏水稀释为200 mL,稀释后盐酸的物质的量浓度为
(3)将13 g 锌投入足量的上述实验所得的稀盐酸中,充分反应后,求:(写出计算过程)
①放出的H2在标准状况下的体积
②将生成的H2 通过足量的灼热CuO,求生成铜的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】在一个容积为500mL的密闭容器中,充入5mol H2和2 mol CO。在一定温度和一定压强下,发生如下反应在:2H2(g) +CO(g) CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的
CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的 ,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
 CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的
CH3OH(g),经过5min后达到平衡状态。若此时测得容器内压强是起始时的 ,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
,求:(1)以H2的浓度变化表示的该反应的速率(2)达平衡时CO的转化率(3)该温度下的平衡常数K
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,向容积为10L的密闭容器内通入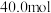
 和
和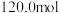
 ,经2s后达到平衡状态,平衡时
,经2s后达到平衡状态,平衡时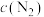 为
为 。
。
(1)达到平衡时氨气的物质的量浓度为:________ 。
(2)用 的浓度变化表示2s内的平均速率
的浓度变化表示2s内的平均速率
________ 。
(3)达到平衡时氮气的转化率是________ 。
(4)平衡时混合气体中氨的体积分数(和物质的量分数相同)是________ 。
(5)平衡时氮气、氢气、氨气的分子数之比为________ 。
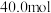
 和
和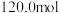
 ,经2s后达到平衡状态,平衡时
,经2s后达到平衡状态,平衡时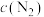 为
为 。
。(1)达到平衡时氨气的物质的量浓度为:
(2)用
 的浓度变化表示2s内的平均速率
的浓度变化表示2s内的平均速率
(3)达到平衡时氮气的转化率是
(4)平衡时混合气体中氨的体积分数(和物质的量分数相同)是
(5)平衡时氮气、氢气、氨气的分子数之比为
您最近一年使用:0次
【推荐3】把6 molA气体和5 molB气体混合放入4L恒容密闭容器中。在一定条件下发生反应:3A(g)+B(g)  2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC.又知在此时D的平均速率为0.15mol•L-1•min-1.(要求写出计算过程)
2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC.又知在此时D的平均速率为0.15mol•L-1•min-1.(要求写出计算过程)
求:
(1)平衡时A的物质的量浓度____ ;
(2)B的转化率____ ;
(3)x的值____ ;
(4)平衡时D的物质的量分数____ ;
(5)反应前后压强比(分数表示)____
(6)平衡常数K____
 2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC.又知在此时D的平均速率为0.15mol•L-1•min-1.(要求写出计算过程)
2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC.又知在此时D的平均速率为0.15mol•L-1•min-1.(要求写出计算过程)求:
(1)平衡时A的物质的量浓度
(2)B的转化率
(3)x的值
(4)平衡时D的物质的量分数
(5)反应前后压强比(分数表示)
(6)平衡常数K
您最近一年使用:0次



