(1)在标准状况下,0.5mol N2和1mol O2 的混合气体的体积约是_____ .
(2)标准状况下,气体的摩尔体积是______ ,0.5mol CO2 的质量是____ ,在标准状况下的体积是_____ .
(3)①标准状况下,2mol NH3与_______ g CO2的体积相等.
②等质量的O2和O3所含的原子个数之比是______ .
③用金属Na、Mg、Al与足量的稀盐酸反应,欲制取相同条件下等体积的H2,则需要金属Na、Mg、Al的质量比为_____ (最简整数比).
④已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的相对分子质量为__ .
(2)标准状况下,气体的摩尔体积是
(3)①标准状况下,2mol NH3与
②等质量的O2和O3所含的原子个数之比是
③用金属Na、Mg、Al与足量的稀盐酸反应,欲制取相同条件下等体积的H2,则需要金属Na、Mg、Al的质量比为
④已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的相对分子质量为
更新时间:2019-10-11 19:23:01
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】按要求填空;
(1)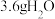 物质的量为
物质的量为_______ mol,约含有_______ 个原子;
(2)已知 个X气体的质量是
个X气体的质量是 ,则X气体的摩尔质量是
,则X气体的摩尔质量是_______ ;
(3)同温同压下,同体积的甲烷 和
和 质量之比为
质量之比为_______ ,质子数之比_______ ;
(4)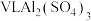 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为_______ ,取出V/2L再加入水稀释到4VL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是_______ 。
(5)某化合物由NaCl、 、
、 三种物质组成,已知钠、镁、铝三元素质量比为
三种物质组成,已知钠、镁、铝三元素质量比为 ,则NaCl、
,则NaCl、 、
、 三种物质的物质的量之比为
三种物质的物质的量之比为_______ ,当 的物质的量为1mol时,混合物的质量是
的物质的量为1mol时,混合物的质量是_______ g。
(6)用质量分数为36.5%的浓盐酸(密度为1.16 )配制成
)配制成 的稀盐酸250ml,浓盐酸的物质的量浓度是:
的稀盐酸250ml,浓盐酸的物质的量浓度是:_______ ;需要浓盐酸体积为:_______ mL(精确到小数点后1位)
(1)
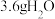 物质的量为
物质的量为(2)已知
 个X气体的质量是
个X气体的质量是 ,则X气体的摩尔质量是
,则X气体的摩尔质量是(3)同温同压下,同体积的甲烷
 和
和 质量之比为
质量之比为(4)
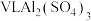 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为 的物质的量浓度是
的物质的量浓度是(5)某化合物由NaCl、
 、
、 三种物质组成,已知钠、镁、铝三元素质量比为
三种物质组成,已知钠、镁、铝三元素质量比为 ,则NaCl、
,则NaCl、 、
、 三种物质的物质的量之比为
三种物质的物质的量之比为 的物质的量为1mol时,混合物的质量是
的物质的量为1mol时,混合物的质量是(6)用质量分数为36.5%的浓盐酸(密度为1.16
 )配制成
)配制成 的稀盐酸250ml,浓盐酸的物质的量浓度是:
的稀盐酸250ml,浓盐酸的物质的量浓度是:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)3.6克H2O的物质的量是_________ ,含有____________ 个H2O。
(2)物质的量浓度为18.4 mol·L-1,密度为1.84 g·mL-1的硫酸的质量分数为____ ,配制1000 mL浓度为1.84 mol·L-1 的硫酸,需要物质的量浓度为18.4 mol·L-1的硫酸______ L。
(3)将190 g MgCl2溶于水配制成1 L溶液。溶液中MgCl2的物质的量浓度为________ 。从中取出50 mL溶液,含有Cl-的物质的量为________ 。
(2)物质的量浓度为18.4 mol·L-1,密度为1.84 g·mL-1的硫酸的质量分数为
(3)将190 g MgCl2溶于水配制成1 L溶液。溶液中MgCl2的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为___ ,原子个数比为___ ,分子的物质的量之比为___ 。
(2)等温等压下,等体积的O2和O3所含分子个数比为____ ,原子个数比为____ ,质量比为___ 。
(3)在标准状况下15gCO与CO2的混合气体,体积为11.2L混合气体的平均摩尔质量是___ ;CO2与CO的体积之比是___ 。
(1)等质量的O2和O3所含分子个数比为
(2)等温等压下,等体积的O2和O3所含分子个数比为
(3)在标准状况下15gCO与CO2的混合气体,体积为11.2L混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)1 mol HNO3的质量是_______ ,1 mol HNO3约含有_______ 个氧原子。
(2)标准状况下11.2 L HCl气体中含有_______ 个原子。
(3)2 mol OH-约含有_______ 个电子。
(4)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量为_______ ,ACl2的化学式为_______ 。
(2)标准状况下11.2 L HCl气体中含有
(3)2 mol OH-约含有
(4)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)某金属氯化物MCl2 28.5 g,含有0.6 mol Cl-,则该氯化物的摩尔质量为____________ ,金属M的名称为____________ 。
(2)11.1 g CaCl2所含氯离子数与标准状况下约__________ L O3所含氧原子数相等。(计算结果保留一位小数点)
(3)若a g SO2含b个原子,则阿伏加 德罗常数为__________ (用含a、b的公式表示)。
(4)某气体在标准状况下的密度为1.25 g/L,则 28 g该气体所含有的分子数为____________ 。
(5)与3.6 g水含有相同氧原子数目的硫酸的质量为____________ 。
(2)11.1 g CaCl2所含氯离子数与标准状况下约
(3)若a g SO2含b个原子,则阿伏加 德罗常数为
(4)某气体在标准状况下的密度为1.25 g/L,则 28 g该气体所含有的分子数为
(5)与3.6 g水含有相同氧原子数目的硫酸的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】Ⅰ.回答下列问题:
(1)在无土栽培中,配制1L内含0.5molNH4Cl、0.16molKCl、0.24molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为________ 、_______ 、______ 。
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为________ 。
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H22.24L(标准状况),则此铁块中一定含有的金属杂质是_______ 。
Ⅱ.实验室常用加热氯酸钾的方法制取少量氧气。
(4)请写出反应的化学方程式_______ 。
(5)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?_______ 、________ 。
(1)在无土栽培中,配制1L内含0.5molNH4Cl、0.16molKCl、0.24molK2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H22.24L(标准状况),则此铁块中一定含有的金属杂质是
Ⅱ.实验室常用加热氯酸钾的方法制取少量氧气。
(4)请写出反应的化学方程式
(5)现欲制取1.12L(标准状况)氧气,理论上需要消耗氯酸钾多少克?生成氯化钾物质的量多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组为测定某工厂生产的 的纯度(即质量分数),称取10.0g该
的纯度(即质量分数),称取10.0g该 样品放于烧杯中,加水使之完全溶解,再向烧杯中加入60.0g溶质质量分数为16%的NaOH溶液,充分反应后,过滤,将沉淀洗涤、常温干燥,称得固体质量为5.8g。(已知:该
样品放于烧杯中,加水使之完全溶解,再向烧杯中加入60.0g溶质质量分数为16%的NaOH溶液,充分反应后,过滤,将沉淀洗涤、常温干燥,称得固体质量为5.8g。(已知:该 产品中含有少量
产品中含有少量 等杂质,杂质均能溶于水,且不与NaOH反应)
等杂质,杂质均能溶于水,且不与NaOH反应)
请计算:
(1)假设60.0g溶质质量分数为16%的NaOH溶液完全反应,需要 的质量是
的质量是_______ (不写计算过程)。由此可以判断,烧杯内10.0g样品中的
_______ (填“全部”或“部分”)与NaOH溶液发生了反应。
(2)该样品中 的质量分数是多少?(写出计算过程)
的质量分数是多少?(写出计算过程) _______
 的纯度(即质量分数),称取10.0g该
的纯度(即质量分数),称取10.0g该 样品放于烧杯中,加水使之完全溶解,再向烧杯中加入60.0g溶质质量分数为16%的NaOH溶液,充分反应后,过滤,将沉淀洗涤、常温干燥,称得固体质量为5.8g。(已知:该
样品放于烧杯中,加水使之完全溶解,再向烧杯中加入60.0g溶质质量分数为16%的NaOH溶液,充分反应后,过滤,将沉淀洗涤、常温干燥,称得固体质量为5.8g。(已知:该 产品中含有少量
产品中含有少量 等杂质,杂质均能溶于水,且不与NaOH反应)
等杂质,杂质均能溶于水,且不与NaOH反应)请计算:
(1)假设60.0g溶质质量分数为16%的NaOH溶液完全反应,需要
 的质量是
的质量是
(2)该样品中
 的质量分数是多少?(写出计算过程)
的质量分数是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】一定量的铁与稀盐酸反应,生成了4.48LH2(标准状况下)
(1)参加反应的铁的质量多少克______________ ?
(2)若所用盐酸的浓度为0.5mol/L,则至少需要盐酸的体积为多少毫升______ ?
(1)参加反应的铁的质量多少克
(2)若所用盐酸的浓度为0.5mol/L,则至少需要盐酸的体积为多少毫升
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体(标准状况,下同)体积为b L,样品中铝的质量是______________ g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:_______________________ ,氧化铁与铝的质量比是_____________ 。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c:b__________ 。
(4)用铝热法还原下列物质,制得金属各1mol,消耗铝最少的是____________
A.MnO2 B.Fe3O4 C.Cr2O3 D. V2O5
(1)若取a g样品,向其中加入足量的氢氧化钠溶液,测得生成的气体(标准状况,下同)体积为b L,样品中铝的质量是
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c:b
(4)用铝热法还原下列物质,制得金属各1mol,消耗铝最少的是
A.MnO2 B.Fe3O4 C.Cr2O3 D. V2O5
您最近一年使用:0次



