有一瓶澄清的溶液,其中可能含有 H+、NH4+、Na+、Al3+、Fe3+、I-、NO3- 、CO32-、SO42- 、AlO2-。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③该溶液的焰色反应没有黄色;
④当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。
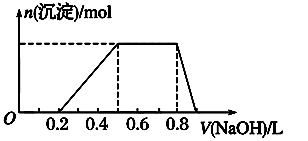
(1)该溶液中肯定含有的离子是_________________________ ,已确定阳离子的物质的量之比为_______________________ 。
(2)肯定不含的离子是_________________________________ 。
(3)不能确定的离子是_________ ,如何证明该离子是否存在?__________ 。
(4)请写出沉淀溶解过程的离子方程式____________________________ 。
①用pH试纸检验,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③该溶液的焰色反应没有黄色;
④当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。

(1)该溶液中肯定含有的离子是
(2)肯定不含的离子是
(3)不能确定的离子是
(4)请写出沉淀溶解过程的离子方程式
更新时间:2018-10-02 06:08:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某溶液的溶质可能由下列离子组成:Cl-、SO 、CO
、CO 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:
Ⅰ. 向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ. 向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ. 将Ⅰ中的沉淀加入足量稀盐酸中,沉淀部分消失,有气体产生。
(1)依据以上实验可以推断,原溶液中一定含有___________ ;一定没有___________ ;检验可能存在的离子的试剂为___________ 。测定该溶液中的阳离子可以通过___________ 方法确定。
(2)Ⅱ中发生的离子反应___________ ;Ⅲ中发生的离子反应___________
 、CO
、CO 、H+、Ba2+、Na+,某同学进行了如下实验:
、H+、Ba2+、Na+,某同学进行了如下实验:Ⅰ. 向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
Ⅱ. 向Ⅰ中滤液中加入AgNO3溶液,有白色沉淀产生;
Ⅲ. 将Ⅰ中的沉淀加入足量稀盐酸中,沉淀部分消失,有气体产生。
(1)依据以上实验可以推断,原溶液中一定含有
(2)Ⅱ中发生的离子反应
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D为四种可溶性盐,它们的阳离子分别是 、
、 、
、 、
、 中的一种,阴离子分别是
中的一种,阴离子分别是 、
、 、
、 、
、 中的一种(离子在物质中不能重复出现)。
中的一种(离子在物质中不能重复出现)。
现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色。
②向①的四支试管中分别加入盐酸,B的溶液中有沉淀生成,D的溶液中有无色无味的气体逸出。
根据①②实验现象回答下列问题:
(1)写出A、C的化学式:A________ ,C________ 。
(2)写出盐酸与D反应产生气体的离子方程式:________ 。
(3)写出C与 溶液反应的离子方程式:
溶液反应的离子方程式:________ 。
(4)将含相同数目A、B、C的溶液混合后,写出溶液中存在的离子________ ;在此溶液中加入锌粒,写出发生反应的离子方程式________ 。
 、
、 、
、 、
、 中的一种,阴离子分别是
中的一种,阴离子分别是 、
、 、
、 、
、 中的一种(离子在物质中不能重复出现)。
中的一种(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈蓝色。
②向①的四支试管中分别加入盐酸,B的溶液中有沉淀生成,D的溶液中有无色无味的气体逸出。
根据①②实验现象回答下列问题:
(1)写出A、C的化学式:A
(2)写出盐酸与D反应产生气体的离子方程式:
(3)写出C与
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)将含相同数目A、B、C的溶液混合后,写出溶液中存在的离子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】今有一混合物的溶液,只可能含有以下离子中的若干种:K+、 、Cl-、Ca2+、Ba2+、
、Cl-、Ca2+、Ba2+、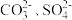 现取三份各100mL溶液进行如下实验:
现取三份各100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-?________ (填“是”或“否”),理由是______________________________ 。
(2)由第二份进行的实验可知混合物中应含有________ 离子,其物质的量浓度为________ 。
(3)由第三份进行的实验可知12.54g 沉淀的成分为____________________ 。请计算形成该沉淀的原混合物中各离子的物质的量________________________ 。
(4)综合上述实验, 能否确定有K+存在?(填“能”或“否”)(以下二选一填)________ ;
若能,请计算K+的浓度范围______________________________;
若不能,请描述检验是否存在K+的实验操作__________________________。
 、Cl-、Ca2+、Ba2+、
、Cl-、Ca2+、Ba2+、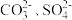 现取三份各100mL溶液进行如下实验:
现取三份各100mL溶液进行如下实验:第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-?
(2)由第二份进行的实验可知混合物中应含有
(3)由第三份进行的实验可知12.54g 沉淀的成分为
(4)综合上述实验, 能否确定有K+存在?(填“能”或“否”)(以下二选一填)
若能,请计算K+的浓度范围______________________________;
若不能,请描述检验是否存在K+的实验操作__________________________。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、M、N、Q的原子序数依次增大,其中X的一种原子无中子,Y、N同主族,Y的最外层电子数是周期数的3倍,Z与Y的核电荷数之差为3,M是地壳中含量最多的金属。回答下列问题:
(1)N在元素周期表中的位置是___________ ,Y的离子结构示意图为___________ 。
(2)Y、M、N三种元素所形成的简单离子,半径由大到小的顺序是___________ (填化学式,下同)。N、Q的简单氢化物热稳定性较差的是___________ 。
(3)X、Y、Z形成的化合物中化学键类型为___________ 。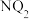 的电子式为
的电子式为___________ 。
(4)实验室检验Z简单离子的方法是___________ 。
(5) M最高价氧化物对应的水化物分别与Z、Q最高价氧化物对应的水化物反应的离子方程式为___________ 、___________ 。
(1)N在元素周期表中的位置是
(2)Y、M、N三种元素所形成的简单离子,半径由大到小的顺序是
(3)X、Y、Z形成的化合物中化学键类型为
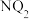 的电子式为
的电子式为(4)实验室检验Z简单离子的方法是
(5) M最高价氧化物对应的水化物分别与Z、Q最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知有以下物质相互转化
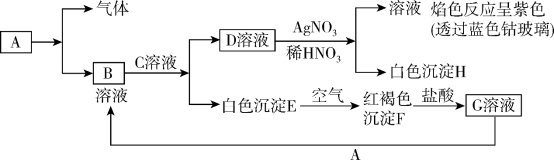
试回答:
(1)写出B的化学式_______ ,H的化学式_______
(2)写出由E→F反应的化学方程式:_______ 。
(3)把KSCN溶液加到G溶液中的现象是_______ ;向G溶液加入A的有关离子反应方程式:_______ 。

试回答:
(1)写出B的化学式
(2)写出由E→F反应的化学方程式:
(3)把KSCN溶液加到G溶液中的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
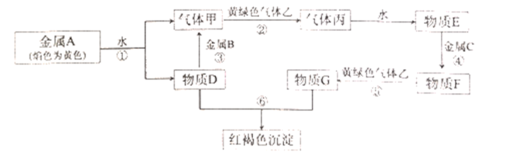
请根据以上信息回答下列问题:
(1)气体丙的电子式是___________ 。
(2)金属B元素在周期表中的位置___________ 。
(3)金属C元素所在周期共有___________ 种元素。
(4)物质D所含的化学键类型有离子键和___________ (填“极性共价键”或“非极性共价键”)。
(5)写出反应⑤的离子方程式___________ 。
(6)工业冶炼单质A的化学方程式___________ 。
(7)金属C可以通过铝热反应冶炼所得,写出该反应的化学方程式___________ 。

请根据以上信息回答下列问题:
(1)气体丙的电子式是
(2)金属B元素在周期表中的位置
(3)金属C元素所在周期共有
(4)物质D所含的化学键类型有离子键和
(5)写出反应⑤的离子方程式
(6)工业冶炼单质A的化学方程式
(7)金属C可以通过铝热反应冶炼所得,写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铵明矾[NH4Al(SO4)2·12H2O]是分析化学常用基准试剂,其制备过程如图。
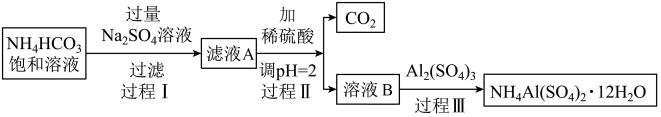
已知:过程Ⅰ的反应原理为:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
(1)写出过程Ⅱ中,往滤液A中加入稀H2SO4产生CO2的离子方程式_____ 。
(2)过程Ⅲ中,往滤液B中,加入适量蒸馏水,加热并不断搅拌,加入适量Al2(SO4)3,_____ 、_____ 、过滤、洗涤、晾干,得到铵明矾(填具体的实验操作步骤,铵明矾的溶解度曲线如图1所示)。
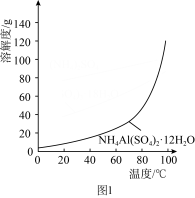
(3)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化关系如图2所示。
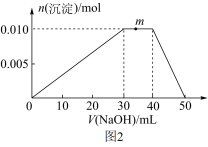
①写出m点反应的离子方程式_____ 。
②若在NH4Al(SO4)2溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_____ mol。

已知:过程Ⅰ的反应原理为:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
(1)写出过程Ⅱ中,往滤液A中加入稀H2SO4产生CO2的离子方程式
(2)过程Ⅲ中,往滤液B中,加入适量蒸馏水,加热并不断搅拌,加入适量Al2(SO4)3,

(3)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化关系如图2所示。

①写出m点反应的离子方程式
②若在NH4Al(SO4)2溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3 (约10%)和MgO(约5%)。其同学设计了如下方案,分离样品中各种金属元素。
已知: Fe(OH)3的Ksp=4.0×10-38。请回答下列问题。
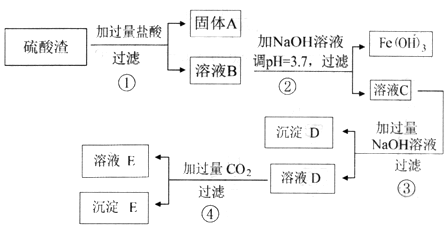
(1) 固体A的一种工业应用________ ;沉淀D的电子式___________ 。
(2) 溶液B中所含的金属阳离子有___________ 。(写离子符号)
(3) 若步骤②中调pH 为3.0,则溶液C中的Fe3+ 是否沉淀完全,通过计算说明______ 。
(4) 写出步骤④中全部反应的离子方程式_______________ 。
(5) 为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①判断到达滴定终点的现象是__________ 。
②某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL 溶液,移取25.00mL 试样溶液,用0.0050 mol/L KMnO4标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是_________________ 。
已知: Fe(OH)3的Ksp=4.0×10-38。请回答下列问题。

(1) 固体A的一种工业应用
(2) 溶液B中所含的金属阳离子有
(3) 若步骤②中调pH 为3.0,则溶液C中的Fe3+ 是否沉淀完全,通过计算说明
(4) 写出步骤④中全部反应的离子方程式
(5) 为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。
①判断到达滴定终点的现象是
②某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL 溶液,移取25.00mL 试样溶液,用0.0050 mol/L KMnO4标准溶液滴定,达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】 (四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为
(四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为 ,含少量
,含少量 、
、 和
和 等)为原料制备四氢铝钠的流程如下。
等)为原料制备四氢铝钠的流程如下。 是酸性氧化物;
是酸性氧化物;
② 。
。
回答下列问题:
(1)浸渣的主要成分是___________ (填化学式)。
(2)“除杂”时铝元素转化的离子方程式为___________ 。
(3)将“沉铝”后的滤液蒸干、灼烧得到的固体是___________ (填化学式)。实验室进行“蒸干、灼烧”时不需要使用的仪器有___________ (填字母)。
A.酒精灯 B.烧杯 C.坩埚 D.蒸发皿
(4)实验室用氢气和钠共热制备 ,
, 的电子式为
的电子式为___________ 。
(5)写出 和
和 反应制备
反应制备 的化学方程式:
的化学方程式:___________ 。
(6)在化学上,含氢还原剂的还原能力用“有效氢”表示。“有效氢”的定义是单位质量含氢还原剂的还原能力相当于多少克氢气。一般地,含氢还原剂中氢元素被氧化成 ,还原能力用失去电子数多少表示。
,还原能力用失去电子数多少表示。 、
、 的“有效氢”之比为
的“有效氢”之比为___________ 。
 (四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为
(四氢铝钠)是一种强还原剂和供氢剂,在有机合成中广泛应用。以铝土矿(主要成分为 ,含少量
,含少量 、
、 和
和 等)为原料制备四氢铝钠的流程如下。
等)为原料制备四氢铝钠的流程如下。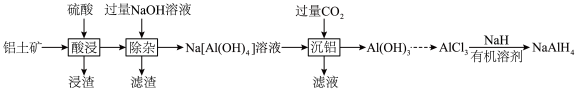
 是酸性氧化物;
是酸性氧化物;②
 。
。回答下列问题:
(1)浸渣的主要成分是
(2)“除杂”时铝元素转化的离子方程式为
(3)将“沉铝”后的滤液蒸干、灼烧得到的固体是
A.酒精灯 B.烧杯 C.坩埚 D.蒸发皿
(4)实验室用氢气和钠共热制备
 ,
, 的电子式为
的电子式为(5)写出
 和
和 反应制备
反应制备 的化学方程式:
的化学方程式:(6)在化学上,含氢还原剂的还原能力用“有效氢”表示。“有效氢”的定义是单位质量含氢还原剂的还原能力相当于多少克氢气。一般地,含氢还原剂中氢元素被氧化成
 ,还原能力用失去电子数多少表示。
,还原能力用失去电子数多少表示。 、
、 的“有效氢”之比为
的“有效氢”之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH 、Cl-、Ca2+、Ba2+、CO
、Cl-、Ca2+、Ba2+、CO 、SO
、SO ,现取三份各100mL该溶液进行如下实验:
,现取三份各100mL该溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.12mol;
③第三份加足BaCl2溶液后,得干燥沉淀10.57g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,回答下列问题:
(1)由第三份进行的实验可知10.57g沉淀的成分是(写沉淀化学式)___________ ,其物质的量分别为___________ (与前面填的对应起来)
(2)由第二份进行的实验得知混合物中应含有___________ (填离子符号),其物质的量浓度为___________ mol/L。
(3)溶液中一定含有的离子是___________ ,可能含有的离子是___________ 。
 、Cl-、Ca2+、Ba2+、CO
、Cl-、Ca2+、Ba2+、CO 、SO
、SO ,现取三份各100mL该溶液进行如下实验:
,现取三份各100mL该溶液进行如下实验:①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.12mol;
③第三份加足BaCl2溶液后,得干燥沉淀10.57g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,回答下列问题:
(1)由第三份进行的实验可知10.57g沉淀的成分是(写沉淀化学式)
(2)由第二份进行的实验得知混合物中应含有
(3)溶液中一定含有的离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】有一包白色粉末,其中可能含有NaCI、Ba(NO3)2、CuSO4、Na2CO3,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
②向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中一定含有的物质是_______ ,可能含有的物质是__________ (以上物质均写化学式),第②步反应中离子方程式为______________________________________
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
②向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中一定含有的物质是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有一无色透明酸性溶液120mL,欲确定是否含有下列离子:K+、Mg2+、Al3+、Cu2+、Ba2+、 、Fe3+、Cl-、I-、
、Fe3+、Cl-、I-、 、
、 、
、 ,将溶液均分成三等份,分别进行如下实验:
,将溶液均分成三等份,分别进行如下实验:
第一份:i.加入少量氯水后,再加入CCl4溶液,有机层为紫红色;
ii.再向水层加AgNO3溶液有稳定的白色沉淀生成,且不溶于稀硝酸。
第二份:加入足量BaCl2溶液,有白色沉淀生成;
第三份:i.加入过量NaOH溶液并加热,生成白色沉淀、并有刺激性气味的气体和溶液A生成;
ii.向溶液A中通入过量CO2,加热、过滤、洗涤、灼烧,得到白色固体(1.02g)。
回答下列问题:
(1)不做任何实验便可确定不存在的离子有___________ ,通过以上实验可判断溶液中肯定存在的阴离子是___________ ,可能存在的阴离子是___________ 。
(2)为进一步确定其它阳离子的存在,应该补充的实验的名称为(不必写详细操作步骤)_____ 。
(3)第三份中步骤ⅱ加热的目的是___________ 。
(4)原溶液中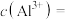
___________  。
。
 、Fe3+、Cl-、I-、
、Fe3+、Cl-、I-、 、
、 、
、 ,将溶液均分成三等份,分别进行如下实验:
,将溶液均分成三等份,分别进行如下实验:第一份:i.加入少量氯水后,再加入CCl4溶液,有机层为紫红色;
ii.再向水层加AgNO3溶液有稳定的白色沉淀生成,且不溶于稀硝酸。
第二份:加入足量BaCl2溶液,有白色沉淀生成;
第三份:i.加入过量NaOH溶液并加热,生成白色沉淀、并有刺激性气味的气体和溶液A生成;
ii.向溶液A中通入过量CO2,加热、过滤、洗涤、灼烧,得到白色固体(1.02g)。
回答下列问题:
(1)不做任何实验便可确定不存在的离子有
(2)为进一步确定其它阳离子的存在,应该补充的实验的名称为(不必写详细操作步骤)
(3)第三份中步骤ⅱ加热的目的是
(4)原溶液中
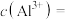
 。
。
您最近一年使用:0次



