选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取、分液 B.渗析 C.蒸发 D.分液 E.蒸馏 F.过滤
(1)分离粗盐溶液中混有的泥沙________ 。
(2)分离碘和水的混合物________ 。
(3)分离淀粉和氯化钠的混合液________ 。
(4)分离酒精和水的混合物________ 。
A.萃取、分液 B.渗析 C.蒸发 D.分液 E.蒸馏 F.过滤
(1)分离粗盐溶液中混有的泥沙
(2)分离碘和水的混合物
(3)分离淀粉和氯化钠的混合液
(4)分离酒精和水的混合物
更新时间:2018-11-05 08:09:03
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】三盐基硫酸铅(3PbO·PbSO4·H2O,其相对分子质量为990)简称“三盐”,不溶于水及有机溶剂。主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示,已知:Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13。
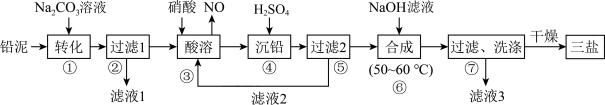
根据下图溶解度曲线,由滤液1得到Na2SO4固体的操作为:将“滤液1”_______ 、_______ 、用乙醇洗涤后干燥
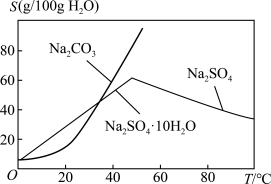

根据下图溶解度曲线,由滤液1得到Na2SO4固体的操作为:将“滤液1”

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氯化硫(SCl2)是一种重要的化工原料, 被广泛用作有机合成的氯化剂和润滑油的处理剂。工业上的合成方法之一是:
①2S(s) + Cl2(g) S2Cl2(l);
S2Cl2(l);
②S2Cl2(l)+ Cl2(g) = 2SCl2(l)。
已知相关物质的性质如下表所示:
某小组在实验室模拟工业制备二氯化硫时设计了如下实验装置(部分夹持装置已略去) 。
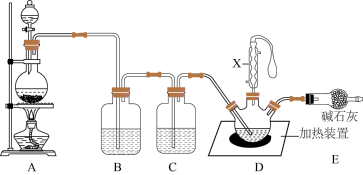
第②步反应后得到SCl2粗品,从混合物中分离出产品的操作方法是___________ 。
①2S(s) + Cl2(g)
 S2Cl2(l);
S2Cl2(l);②S2Cl2(l)+ Cl2(g) = 2SCl2(l)。
已知相关物质的性质如下表所示:
| 物质 | 外观 | 熔点/℃ | 沸点/℃ | 水溶性 |
| S | 淡黄色粉末 | 118 | 445 | 不溶 |
| S2Cl2 | 黄红色液体 | -80 | 138 (分解) | 剧烈反应 |
| SCl2 | 红棕色液体 | -78 | 60 | 剧烈反应 |

第②步反应后得到SCl2粗品,从混合物中分离出产品的操作方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】用于分离或提纯物质的已学方法有:
A 萃取 B 分液 C 过滤 D 蒸发 E 蒸馏
下列各组混合物的分离或提纯应选用上述哪种方法最合适?
( ) (1)除去Ca(OH)2溶液悬浮的Ca(OH)2 颗粒
( ) (2)把饱和食盐水中的食盐提取出来
( ) (3)除去酒精中溶解的微量食盐
( ) (4)把溴水中的溴提取出来
( ) (5)分离柴油和水的混合物
A 萃取 B 分液 C 过滤 D 蒸发 E 蒸馏
下列各组混合物的分离或提纯应选用上述哪种方法最合适?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国科学家屠呦呦因青蒿素研究获得诺贝尔奖,某实验小组拟提取青蒿素
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。实验室用乙醚提取青蒿素的工艺流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是_______ 。
(2)操作II的名称是___________ 。
(3)操作III进行的是重结晶,其操作步骤为加热溶解→____ →____ →过滤、洗涤、干燥。
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。实验室用乙醚提取青蒿素的工艺流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是
(2)操作II的名称是
(3)操作III进行的是重结晶,其操作步骤为加热溶解→
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列几种物质:
①Al ②乙醇 ③ ④熔融CaO ⑤
④熔融CaO ⑤ 溶液 ⑥
溶液 ⑥ ⑦
⑦ 固体
固体
(1)上述物质属于电解质的有___________ (填序号,下同),属于非电解质的有___________ 。
(2)Na加入到 溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:
溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:___________ 。
(3)Al加入到足量NaOH溶液的离子方程式:___________ 。
(4)乙醇中混有水可以先加入CaO再___________ 而得到比较纯净的乙醇。
(5)向 溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。

①Al ②乙醇 ③
 ④熔融CaO ⑤
④熔融CaO ⑤ 溶液 ⑥
溶液 ⑥ ⑦
⑦ 固体
固体(1)上述物质属于电解质的有
(2)Na加入到
 溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:
溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:(3)Al加入到足量NaOH溶液的离子方程式:
(4)乙醇中混有水可以先加入CaO再
(5)向
 溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
| A.HCl | B. | C. | D. |
您最近一年使用:0次
【推荐1】 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

过程①制取1mol Na2FeO4,理论上需要Na2O2的物质的量为__________ 。步骤②中反应能够发生的原因是__________ 。分离出K2FeO4固体的操作中使用的玻璃仪器有__________ 。

过程①制取1mol Na2FeO4,理论上需要Na2O2的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】电解质在溶液中的反应实质上是离子之间的反应离子。请回答以下问题:
I.有四种物质:①氧化铁②盐酸③碳酸氢钠④氢氧化钠
(1)写出其中盐的电离方程式_______ 。
(2)上述物质中有一种与其它三种物质均能反应,此物质是_______ (填序号)。
(3)写出③④两种溶液反应的离子方程式_______ 。
II.某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(已知溶液2为无色溶液)

(4)分离得到沉淀1和溶液1的实验中,使用到的玻璃仪器有_______ 。
(5)沉淀3的化学式:_______ 。
(6)“溶液1+B”生成沉淀2的离子方程式为:_______ 。
I.有四种物质:①氧化铁②盐酸③碳酸氢钠④氢氧化钠
(1)写出其中盐的电离方程式
(2)上述物质中有一种与其它三种物质均能反应,此物质是
(3)写出③④两种溶液反应的离子方程式
II.某溶液中含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(已知溶液2为无色溶液)

(4)分离得到沉淀1和溶液1的实验中,使用到的玻璃仪器有
(5)沉淀3的化学式:
(6)“溶液1+B”生成沉淀2的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁及其化合物在生产、生活中有极其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_______ ,分散剂是_______ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_______ 。
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的化学方程式是_______ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是_______ (填化学专用名词)。
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果。由饱和FeCl3溶液制备Fe(OH)3胶体的化学方程式是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
您最近一年使用:0次

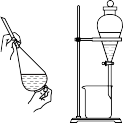

 萃取碘水中的
萃取碘水中的 ,选用
,选用

