(1)在反应 KMnO4+ HCl= MnCl2+ KCl+ Cl2↑+ H2O中,MnCl2为易溶于水的强电解质,回答下列问题:
①氧化剂是___________ ,还原剂是__________ ;
②配平上述方程式并用双线桥法标明电子转移的方向和数目:______________ ;
③写出上述反应的离子方程式:_________________________________________ ;
④若生成71gCl2,被氧化的HCl是_________________ g。
(2)单质铁与稀HNO3可发生多种反应,当8/3n(Fe)<n(HNO3)≤4n(Fe)时,反应方程式可用下列通式表示:aFe+bHNO3(稀)=cNO十dFe(NO3)2+eFe(NO3)3十fH2O。
①假设a=16,且b、c、d、e、f均取正整数时,共有_______ 组系数配比。
②若a、b、c、d、e、f符合上述系数的配比关系,则b与C的关系为:b=____ c。
①氧化剂是
②配平上述方程式并用双线桥法标明电子转移的方向和数目:
③写出上述反应的离子方程式:
④若生成71gCl2,被氧化的HCl是
(2)单质铁与稀HNO3可发生多种反应,当8/3n(Fe)<n(HNO3)≤4n(Fe)时,反应方程式可用下列通式表示:aFe+bHNO3(稀)=cNO十dFe(NO3)2+eFe(NO3)3十fH2O。
①假设a=16,且b、c、d、e、f均取正整数时,共有
②若a、b、c、d、e、f符合上述系数的配比关系,则b与C的关系为:b=
更新时间:2018-11-19 12:13:52
|
相似题推荐
【推荐1】Ⅰ.已知亚硝酸钠能发生如下反应:2NaNO2+ 4HI= 2NO + I2 + 2NaI + 2H2O
(1)用双线桥表示电子转移的方向与数目_______ 。
(2)氧化产物和还原产物的数目比:__________ 。
II.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O该反应中还原产物为__________ 。
(1)用双线桥表示电子转移的方向与数目
(2)氧化产物和还原产物的数目比:
II.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O该反应中还原产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是______ 。
(2)已知0.2molKBrO3在反应中得到1 mol电子生成X,则X的化学式为____ 。
(3)根据上述反应可推知___ 。
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式____ 。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2molKBrO3在反应中得到1 mol电子生成X,则X的化学式为
(3)根据上述反应可推知
A.氧化性:KBrO3>H3AsO4 B.氧化性:H3AsO4>KBrO3
C.还原性:AsH3>X D.还原性:X>AsH3
(4)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式
您最近一年使用:0次
【推荐3】实验室用高锰酸钾和浓盐酸反应制备氯气。2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
(1)用双线桥法标出上述反应方程式中电子转移的方向与数目________ 。
(2)上述反应中,氧化剂是_______ (填化学式,下同),氧化产物_______ ,当有1mol电子发生转移时,理论上生成氯气的体积(标准状况)为_______ L 。
(3)若反应中有0.5mol电子转移,被氧化HCl的的物质的量为_______ mol 。
(1)用双线桥法标出上述反应方程式中电子转移的方向与数目
(2)上述反应中,氧化剂是
(3)若反应中有0.5mol电子转移,被氧化HCl的的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.某反应为:3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O,
(1)用单线桥表示出该反应中电子转移的方向和数目:______________________ 。
(2)该反应中氧化剂的化学式是__________ , 被氧化的元素是________ 。(填元素符号)。
II.有下列三个反应:
a.2FaC13 + 2KI =2FeCl2 + 2KCl + I2
b.2FeCl2+Cl2=2FeCl3
c.2KMnO4+ 16HCl(浓)=2KCl + 2MnCl2+ 5Cl2↑+ 8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为_____________________ ;
(2)在反应c中,若被氧化的HCl为1. 5mol,则转移的电子数是___________________ 个。
(1)用单线桥表示出该反应中电子转移的方向和数目:
(2)该反应中氧化剂的化学式是
II.有下列三个反应:
a.2FaC13 + 2KI =2FeCl2 + 2KCl + I2
b.2FeCl2+Cl2=2FeCl3
c.2KMnO4+ 16HCl(浓)=2KCl + 2MnCl2+ 5Cl2↑+ 8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为
(2)在反应c中,若被氧化的HCl为1. 5mol,则转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业废水中含有的重铬酸根( )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)做处理剂,反应的离子方程式如下:6Fe2++
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)做处理剂,反应的离子方程式如下:6Fe2++ +14H+=6Fe3++2Cr3++7H2O。回答下列问题:
+14H+=6Fe3++2Cr3++7H2O。回答下列问题:
(1)上述反应中,还原剂是___________ (填离子符号);氧化性:
___________ Fe3+(填“>”或“<”)。
(2)用“单线桥”标出电子转移的方向和数目:___________ 。
6Fe2++ +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。
(3)每处理含0.5 mol 的废水,需消耗绿矾
的废水,需消耗绿矾___________ g (已知:FeSO4∙7H2O的摩尔质量为278 g∙mol-1)。
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)做处理剂,反应的离子方程式如下:6Fe2++
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)做处理剂,反应的离子方程式如下:6Fe2++ +14H+=6Fe3++2Cr3++7H2O。回答下列问题:
+14H+=6Fe3++2Cr3++7H2O。回答下列问题:(1)上述反应中,还原剂是

(2)用“单线桥”标出电子转移的方向和数目:
6Fe2++
 +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。(3)每处理含0.5 mol
 的废水,需消耗绿矾
的废水,需消耗绿矾
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】海水中存在大量的氯元素,通过对海水中氯元素的提取,可制取单质氯气,也可制取氯的多种氧化物。回答下列问题:
(1)氯气可溶于水形成氯水,溶液中含氯元素的微粒有_______ 种。氯水中属于弱电解质的是_______ (除水外,写化学式),写出该物质的电离方程式_______ 。
(2)常温时,氯气可与 NaOH 溶液反应制取漂白液(俗称 84 消毒液),漂白液的有效成分是_______ 。84 消毒液可作家庭消毒剂,但不能与洁厕精(主要成分是盐酸)混合使用,原因是_______ (用离子反应方程式表示)。
(3)一定条件下,氯气与 NaOH 溶液充分反应后溶液中的 ClO3-和 ClO-的个数比为 1:2,则溶液中 ClO-和 Cl-的个数比为_______ 。
(4)Cl2O 是一种酸性氧化物,常温时是一种棕黄色气体,有毒。制备原理如下: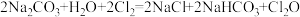 ,请用双线桥表示出该反应中电子转移的方向和数目
,请用双线桥表示出该反应中电子转移的方向和数目_______ 。制备过程中可用NaOH溶液除去剩余Cl2O,写出该反应的化学反应方程式_______ 。
(1)氯气可溶于水形成氯水,溶液中含氯元素的微粒有
(2)常温时,氯气可与 NaOH 溶液反应制取漂白液(俗称 84 消毒液),漂白液的有效成分是
(3)一定条件下,氯气与 NaOH 溶液充分反应后溶液中的 ClO3-和 ClO-的个数比为 1:2,则溶液中 ClO-和 Cl-的个数比为
(4)Cl2O 是一种酸性氧化物,常温时是一种棕黄色气体,有毒。制备原理如下:
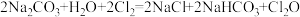 ,请用双线桥表示出该反应中电子转移的方向和数目
,请用双线桥表示出该反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
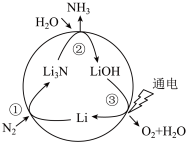
【推荐1】研究氮及其化合物的性质对改善人类的生存环境具有重要意义。回答下列问题:
(1)一种新型人工固氮的原理如图。该转化过程①②③反应中为氧化还原反应的是___________ (填编号)。假设每一步均完全转化,每生成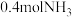 ,同时生成
,同时生成___________ 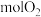 。
。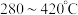 的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出
的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出 消除
消除 的化学反应方程式:
的化学反应方程式:___________ 。
(3)废水中氮的主要存在形态是硝态氮(以 存在)和氨氮(以
存在)和氨氮(以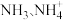 存在),还原法和氧化法是去除废水中氮的重要方法。
存在),还原法和氧化法是去除废水中氮的重要方法。
①还原法:控制其他条件相同,去除 的某含氮废水(废水中总氮
的某含氮废水(废水中总氮 )中的硝态氮,图1为只加过量
)中的硝态氮,图1为只加过量 、图2为同时加过量
、图2为同时加过量 粉与
粉与 时废水中含氮微粒的浓度随时间变化的图像。
时废水中含氮微粒的浓度随时间变化的图像。 的离子方程式为
的离子方程式为___________ ;图2中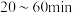 内发生主要反应的离子方程式为
内发生主要反应的离子方程式为___________ 。
②氧化法:利用 将水体中氨氮氧化为
将水体中氨氮氧化为 。已知氧化性:
。已知氧化性: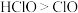 。研究发现,控制其他条件相同,当废水
。研究发现,控制其他条件相同,当废水 为
为 范围内,氨氮去除率随
范围内,氨氮去除率随 降低而升高,分析原因是
降低而升高,分析原因是___________ 。
(1)一种新型人工固氮的原理如图。该转化过程①②③反应中为氧化还原反应的是
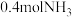 ,同时生成
,同时生成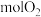 。
。
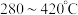 的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出
的烟气中喷入氨可使工厂废气中的氮氧化物转化为无污染的物质。写出 消除
消除 的化学反应方程式:
的化学反应方程式:(3)废水中氮的主要存在形态是硝态氮(以
 存在)和氨氮(以
存在)和氨氮(以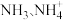 存在),还原法和氧化法是去除废水中氮的重要方法。
存在),还原法和氧化法是去除废水中氮的重要方法。①还原法:控制其他条件相同,去除
 的某含氮废水(废水中总氮
的某含氮废水(废水中总氮 )中的硝态氮,图1为只加过量
)中的硝态氮,图1为只加过量 、图2为同时加过量
、图2为同时加过量 粉与
粉与 时废水中含氮微粒的浓度随时间变化的图像。
时废水中含氮微粒的浓度随时间变化的图像。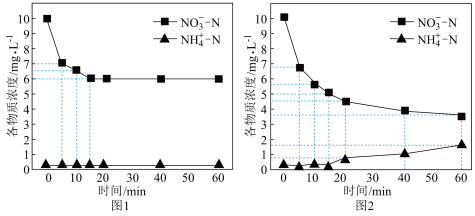
 的离子方程式为
的离子方程式为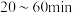 内发生主要反应的离子方程式为
内发生主要反应的离子方程式为②氧化法:利用
 将水体中氨氮氧化为
将水体中氨氮氧化为 。已知氧化性:
。已知氧化性: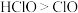 。研究发现,控制其他条件相同,当废水
。研究发现,控制其他条件相同,当废水 为
为 范围内,氨氮去除率随
范围内,氨氮去除率随 降低而升高,分析原因是
降低而升高,分析原因是
您最近一年使用:0次
【推荐2】将质量为12.64gKMnO4固体加热一段时间后,收集到amol O2;向反应后残留的固体中加入足量的浓盐酸,又收集到bmolCl2,此时Mn元素全部以Mn2+的形式存在于溶液中.(KMnO4 的摩尔质量为158g/mol )
(1)请完成并配平下列化学方程式:
_ K2Mn04+__ HCl﹣﹣﹣﹣__ KCl+__ MnCl2+__ Cl2↑+___
该反应中的还原剂是_____ ,当该反应中转移NA个电子时,氧化产物的物质的量为_____ mol,被氧化的还原剂的物质的量为_____ mol.
(2)用酸性高锰酸钾溶液滴定FeSO4溶液写出该反应的离子方程式:_____ .
(3)当KMnO4固体加热生成O2 amol值最大时,向反应后残留的固体中加入足量的浓盐酸并加热,产生Cl2的物质的量b=_____ mol.(此时Mn元素全部以Mn2+的形式存在于溶液中)
(1)请完成并配平下列化学方程式:
该反应中的还原剂是
(2)用酸性高锰酸钾溶液滴定FeSO4溶液写出该反应的离子方程式:
(3)当KMnO4固体加热生成O2 amol值最大时,向反应后残留的固体中加入足量的浓盐酸并加热,产生Cl2的物质的量b=
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40—500C时反应可生成它。CuH不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生反应是2Cu+ = Cu2+ + Cu。根据以上信息,结合自己所掌握的化学知识,回答:
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是______ 。
(2)写出CuH在氯气中燃烧的化学反应方程式______
(3)CuH溶解在稀盐酸中生成的气体是______ ,如果反应中生成了标况下22.4 L的气体,被还原的离子得电子的物质的量是______ 。
(1)在CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是
(2)写出CuH在氯气中燃烧的化学反应方程式
(3)CuH溶解在稀盐酸中生成的气体是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电解质在溶液中发生的反应属于离子反应。结合你的认识完成下列题目。
(1)从稀盐酸、Ba(OH)2溶液、Zn和CuSO4溶液中选出适当的物质,各写出实现下列要求的一个离子方程式。
①实验室制取H2的反应_______ ;
②金属与盐的置换反应_______ ;
③酸与碱的中和反应_______ ;
④生成沉淀的复分解反应_______ 。
(2)经检测,某工业废水显酸性,且废水中含有大量Na+、Cu2+、Cl-、SO 、NO
、NO 。
。
①下列离子中,不可能大量存在于该废水中的是_______ (填字母)。
A.K+ B. Ag+ C. Fe3+ D. CO
②若将该废水调节至碱性,原废水中存在的离子浓度下降的有_______ 。
③除去原废水中的Cu2+和SO ,所需试剂
,所需试剂_______ 。
(3)某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。
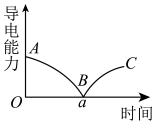
①写出Ba(OH)2溶液与稀硫酸反应的离子方程式_______ 。
②该小组的同学关于图的下列说法中,正确的是_______ (填字母)。
a.AB段溶液的导电能力不断减弱,说明电解质逐渐转变为非电解质
b.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
c.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电
d.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,配平其中一种方法的离子方程式:_______ 。
_______ClO-+_______Fe3++_______OH-=_______FeO +_______Cl-+_______H2O
+_______Cl-+_______H2O
(1)从稀盐酸、Ba(OH)2溶液、Zn和CuSO4溶液中选出适当的物质,各写出实现下列要求的一个离子方程式。
①实验室制取H2的反应
②金属与盐的置换反应
③酸与碱的中和反应
④生成沉淀的复分解反应
(2)经检测,某工业废水显酸性,且废水中含有大量Na+、Cu2+、Cl-、SO
 、NO
、NO 。
。①下列离子中,不可能大量存在于该废水中的是
A.K+ B. Ag+ C. Fe3+ D. CO

②若将该废水调节至碱性,原废水中存在的离子浓度下降的有
③除去原废水中的Cu2+和SO
 ,所需试剂
,所需试剂(3)某兴趣小组的同学向一定体积的Ba(OH)2溶液中逐滴加入稀硫酸,并测得混合溶液的导电能力随时间变化的曲线如图所示。

①写出Ba(OH)2溶液与稀硫酸反应的离子方程式
②该小组的同学关于图的下列说法中,正确的是
a.AB段溶液的导电能力不断减弱,说明电解质逐渐转变为非电解质
b.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
c.BC段溶液的导电能力不断增大,主要是由于过量的Ba(OH)2电离出的离子导电
d.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,配平其中一种方法的离子方程式:
_______ClO-+_______Fe3++_______OH-=_______FeO
 +_______Cl-+_______H2O
+_______Cl-+_______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列9种物质:①CuSO4·5H2O、②铜、③CaCO3、④CO2、⑤NH3、⑥稀硫酸、⑦淀粉溶液,根据要求填空(填序号)
(1)属于电解质的是_______ ;属于非电解质的是_______ 。
(2)在标准状况下,相同体积的④和⑤,其原子个数之比为_______ 。
(3)写出②与浓硝酸反应的化学方程_______ 。
(4)写出⑤的催化氧化的化学方程式_______ 。
(5) 实验室制备氨气的化学方程式_______ 。
(6)铁粉和硫粉混合加热的化学方程_______ 。
(1)属于电解质的是
(2)在标准状况下,相同体积的④和⑤,其原子个数之比为
(3)写出②与浓硝酸反应的化学方程
(4)写出⑤的催化氧化的化学方程式
(5) 实验室制备氨气的化学方程式
(6)铁粉和硫粉混合加热的化学方程
您最近一年使用:0次
【推荐3】软锰矿(主要成分为MnO2)可用于工业上制取高锰酸钾(KMnO4),工艺如下:
I.将软锰矿粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
II.冷却,将固体研细,用稀KOH溶液浸取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
IV.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应。
(1)KMnO4中Mn的化合价为___________ 。
(2)I中,粉碎软锰矿的目的是___________ 。
(3)I中,生成K2MnO4的化学方程式是___________ 。
(4)Ⅱ中,浸取时用稀KOH溶液的原因是___________ 。
(5)Ⅲ中,发生如下反应,配平该离子反应:___________
MnO +CO2+H2O→MnO
+CO2+H2O→MnO +MnO2↓+HCO
+MnO2↓+HCO
氧化产物和还原产物的物质的量之比为___________ 。
I.将软锰矿粉碎后,与KOH固体混合,通入氯气充分焙烧,生成暗绿色熔融态物质。
II.冷却,将固体研细,用稀KOH溶液浸取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
IV.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应。
(1)KMnO4中Mn的化合价为
(2)I中,粉碎软锰矿的目的是
(3)I中,生成K2MnO4的化学方程式是
(4)Ⅱ中,浸取时用稀KOH溶液的原因是
(5)Ⅲ中,发生如下反应,配平该离子反应:
MnO
 +CO2+H2O→MnO
+CO2+H2O→MnO +MnO2↓+HCO
+MnO2↓+HCO
氧化产物和还原产物的物质的量之比为
您最近一年使用:0次



