(1)①根据等电子原理,CO分子的结构式为____________________ 。
②1 molCO2中含有的σ键数目为_________ 。③NO3-的空间构型________ (用文字描述)。
(2)①CO分子内σ键与π键个数之比为____ 。②甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH )。甲醇分子内C原子的杂化方式为________ ,甲醇分子内的O—C—H键角________ (填“大于”、“等于”或“小于”)甲醛分子内的O—C—H键角。
(3)已知CN-与N2结构相似,推算HCN 分子中σ键与π键数目之比为________ 。
②1 molCO2中含有的σ键数目为
(2)①CO分子内σ键与π键个数之比为
(3)已知CN-与N2结构相似,推算HCN 分子中σ键与π键数目之比为
更新时间:2018-12-19 19:18:27
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氮可以形成多种离子,如N3-、NH2-、N3-、NH4+、N2H5+、N2H6+等。已知N2H5+的形成过程类似于NH4+的形成过程,N2H5+在碱性溶液中将生成电中性的分子和水。试写出:
(1)该电中性分子的化学式:_________ ;
(2)N2H5+的电子式:_____________ ;
(3)1 mol N3-共有____ mol 电子;
(4)写出两种非金属氧化物跟N3-电子数相同的物质的化学式_______ 、________ 。
(1)该电中性分子的化学式:
(2)N2H5+的电子式:
(3)1 mol N3-共有
(4)写出两种非金属氧化物跟N3-电子数相同的物质的化学式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是_______ ,其原子核外有_______ 个未成对电子,能量最高的电子所在的轨道呈_______ 形。B为周期表中第29号元素,B的电子排布式为_______ 。
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为: ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为_______ ;此反应中涉及物质中互为等电子体的是_______ ; 的结构式为
的结构式为_______ 。
(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:_______ 。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为:
 ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为 的结构式为
的结构式为(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是地球上极为丰富的元素。
(1)下列氮原子的能量最低的是___________。
(2)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一,有关理论认为N2O与CO2具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为___________ ,其空间构型是___________ 。
(3)肼(N2H4)可作火箭燃料,其分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物,则其分子中氮原子的杂化轨道类型是___________ 。
(4)氮可以形成多种离子,如N3-、NH 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等,已知N2H
等,已知N2H 与N2H
与N2H 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH ,因此有类似于 NH
,因此有类似于 NH 的性质。
的性质。
①写出N2H 的结构式并用“→”标出配位键
的结构式并用“→”标出配位键___________ 。
②N2H 在足量碱性溶液中反应的离子方程式:
在足量碱性溶液中反应的离子方程式:___________ 。
(5)I (可看成II
(可看成II )属于多卤素阳离子,根据VSEPR模型推测I
)属于多卤素阳离子,根据VSEPR模型推测I 的空间构型为
的空间构型为___________ 。
(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形,如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片所带电荷是___________ 。
(1)下列氮原子的能量最低的是___________。
A.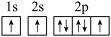 | B.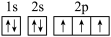 | C.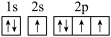 | D.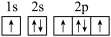 |
(3)肼(N2H4)可作火箭燃料,其分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物,则其分子中氮原子的杂化轨道类型是
(4)氮可以形成多种离子,如N3-、NH
 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等,已知N2H
等,已知N2H 与N2H
与N2H 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH ,因此有类似于 NH
,因此有类似于 NH 的性质。
的性质。①写出N2H
 的结构式并用“→”标出配位键
的结构式并用“→”标出配位键②N2H
 在足量碱性溶液中反应的离子方程式:
在足量碱性溶液中反应的离子方程式:(5)I
 (可看成II
(可看成II )属于多卤素阳离子,根据VSEPR模型推测I
)属于多卤素阳离子,根据VSEPR模型推测I 的空间构型为
的空间构型为(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形,如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片所带电荷是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫及其化合物具有一定的空间结构。
(1)S单质的常见形式为 ,其环状结构如图所示,S原子之间以单键相连,则S原子采取的杂化轨道方式是
,其环状结构如图所示,S原子之间以单键相连,则S原子采取的杂化轨道方式是__________ 。

(2)气态 分子的立体构型为
分子的立体构型为__________ ; 的立体构型为
的立体构型为__________ 。
(1)S单质的常见形式为
 ,其环状结构如图所示,S原子之间以单键相连,则S原子采取的杂化轨道方式是
,其环状结构如图所示,S原子之间以单键相连,则S原子采取的杂化轨道方式是
(2)气态
 分子的立体构型为
分子的立体构型为 的立体构型为
的立体构型为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Pb为第ⅣA族元素,常见的化合价为+2和+4,其单质和化合物都有着广泛的用途。已知Pb2+可以和EDTA[乙二胺四乙酸(HOOCCH2)2NCH2—CH2N(CH2COOH)2]形成无色的1∶1的稳定络合物。请回答下列问题:
(1)在EDTA中,碳原子的杂化方式有___________ 、___________ ,组成EDTA的四种元素中第一电离能最大的是___________
(2)Pb(NO3)2中阴离子的立体构型是___________ ,写出一个与该阴离子立体构型相同的分子的化学式___________
(1)在EDTA中,碳原子的杂化方式有
(2)Pb(NO3)2中阴离子的立体构型是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质,再用CCl4萃取络合物,从而把金属离子从水溶液中完全分离出来。如用双硫腙(H2Dz)~CCl4,分离污水中的Cu2+时,先发生络合反应:Cu2++2H2Dz Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
(1)污水显蓝色是因为四水合铜离子,其空间结构为___________ 。
(2)写出双硫腙和Fe3+络合的离子方程式:___________ 。萃取过程中要控制适宜的酸度。如果溶液的pH过大,其后果是___________ 。
Ⅱ.下图是用双硫腙(H2Dz)~CC14络合萃取某些金属离子的酸度曲线。它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式被萃取分离的百分率。
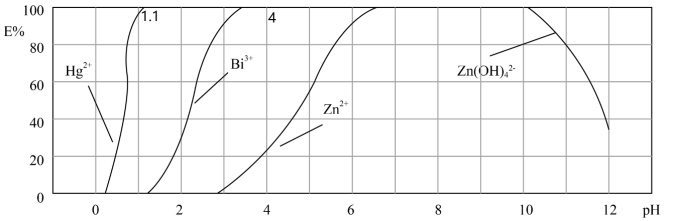
某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)~CC14络合萃取法处理废水。请根据上图回答问题:
(3)欲完全将废水中的Hg2+分离出来,须控制溶液pH为___________ 。
(4)当调节pH=2时,铋(Bi)的存在形式有:___________ ,其物质的量之比为___________ 。
(5)萃取到CCl4中的Zn(HDz)2分液后,加入足量的NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式:___________ 。
 Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。(1)污水显蓝色是因为四水合铜离子,其空间结构为
(2)写出双硫腙和Fe3+络合的离子方程式:
Ⅱ.下图是用双硫腙(H2Dz)~CC14络合萃取某些金属离子的酸度曲线。它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式被萃取分离的百分率。

某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)~CC14络合萃取法处理废水。请根据上图回答问题:
(3)欲完全将废水中的Hg2+分离出来,须控制溶液pH为
(4)当调节pH=2时,铋(Bi)的存在形式有:
(5)萃取到CCl4中的Zn(HDz)2分液后,加入足量的NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式:
您最近半年使用:0次



