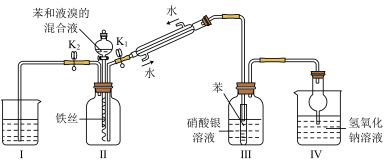
某校学生用下图所示装置进行实验。以探究苯与溴发生反应的原理并分离提纯反应的产物。
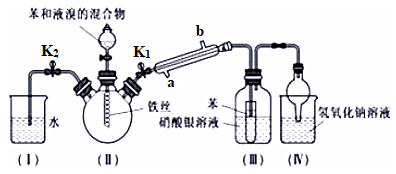
请回答下列问题:
(1)写出装置Ⅱ中发生的主要化学反应方程式____________________________ ,其中冷凝管所起的作用为导气和________ ,Ⅳ中球形干燥管的作用是__________ 。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。Ⅲ中小试管内苯的作用是_________________________ 。
(3)能说明苯与液溴发生了取代反应的现象是______________________ 。
(4)纯净的溴苯是无色油状的液体,这个装置制得的溴苯呈褐色,原因是里面混有溴,将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。①用蒸馏水洗涤,振荡,分液;②用______ 洗涤,振荡,分液;③再用蒸馏水洗涤,振荡,分液;④加入无水氯化钙干燥⑤蒸馏。

请回答下列问题:
(1)写出装置Ⅱ中发生的主要化学反应方程式
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。Ⅲ中小试管内苯的作用是
(3)能说明苯与液溴发生了取代反应的现象是
(4)纯净的溴苯是无色油状的液体,这个装置制得的溴苯呈褐色,原因是里面混有溴,将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。①用蒸馏水洗涤,振荡,分液;②用
更新时间:2018-12-19 20:20:57
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
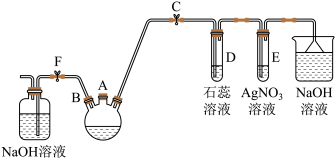
【推荐1】化学兴趣小组学生用如图所示的装置探究苯和液溴的反应并制备溴苯。
请分析后回答下列问题:
(1)关闭F夹,打开C夹,由A口向装有少量苯的三颈烧瓶中加入少量液溴,再加入少量铁屑,塞住A口,则三颈烧瓶中发生反应的化学方程式:______________ 。
(2)D试管内出现的现象为________________________________________ 。
(3)三颈烧瓶右侧导管特别长,除导气外还起的作用是_______________ 。
(4)在三颈烧瓶中仍有气泡冒出时打开F夹,关闭C夹,可以看到的现象是__________ 。
(5)反应结束后分离三颈烧瓶中的溴苯的实验方法是__________________ 。(铁屑已分离)

请分析后回答下列问题:
(1)关闭F夹,打开C夹,由A口向装有少量苯的三颈烧瓶中加入少量液溴,再加入少量铁屑,塞住A口,则三颈烧瓶中发生反应的化学方程式:
(2)D试管内出现的现象为
(3)三颈烧瓶右侧导管特别长,除导气外还起的作用是
(4)在三颈烧瓶中仍有气泡冒出时打开F夹,关闭C夹,可以看到的现象是
(5)反应结束后分离三颈烧瓶中的溴苯的实验方法是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】Ⅰ.根据下面的反应路线及所给信息填空:

(1)A的结构简式是_______ 。
(2)①的反应类型_______ ,②的反应类型_______ 。
(3)反应④的化学方程式_______ 。
Ⅱ.如图中A是制取溴苯的实验装置,B,C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:
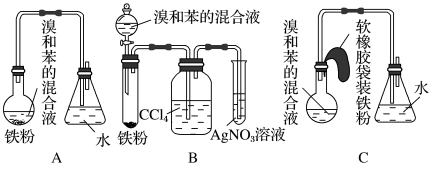
(4)装置A和C均采用了长玻璃导管,其作用是_______ 。
(5)B中采用了洗气瓶吸收装置(里面装有 ),其作用是
),其作用是_______ 。反应后洗气瓶中可能出现的现象是_______ 。
(6)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是_______ 。

(1)A的结构简式是
(2)①的反应类型
(3)反应④的化学方程式
Ⅱ.如图中A是制取溴苯的实验装置,B,C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:

(4)装置A和C均采用了长玻璃导管,其作用是
(5)B中采用了洗气瓶吸收装置(里面装有
 ),其作用是
),其作用是(6)装置B、C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】三苯基甲醇是重要的有机合成中间体。实验室通过用苯甲酸乙酯与苯基溴化镁反应制备三苯基甲醇,其反应原理如下:

已知:① 的生成和使用时必须在无水条件下进行,痕量水就会发生反应:
的生成和使用时必须在无水条件下进行,痕量水就会发生反应: ;
;
②M(溴苯)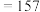 ,M(苯甲酸乙酯)
,M(苯甲酸乙酯) ,M(三苯甲醇)
,M(三苯甲醇)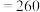 ,M(乙醚)
,M(乙醚) 。
。
实验步骤:
步骤1:按如图组装实验装置后,向三颈烧瓶内放入适量镁屑、一小粒碘和沸石,装上带干燥管的回流冷凝管和盛有过量溴苯和 无水乙醚的恒压滴液漏斗,滴加约三分之一的溴苯乙醚溶液并开动搅拌,慢慢滴入余下的溴苯乙醚溶液,保持反应液呈微沸状态,滴加完毕后,继续回流
无水乙醚的恒压滴液漏斗,滴加约三分之一的溴苯乙醚溶液并开动搅拌,慢慢滴入余下的溴苯乙醚溶液,保持反应液呈微沸状态,滴加完毕后,继续回流 ,使镁屑作用完全。
,使镁屑作用完全。

步骤2:将制备好的过量苯基溴化镁乙醚溶液置于冷水浴中,在搅拌下,滴加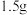 苯甲酸乙酯和
苯甲酸乙酯和 无水乙醚的混合液,控制滴加速度,滴加完毕后,将反应混合物在
无水乙醚的混合液,控制滴加速度,滴加完毕后,将反应混合物在 下继续回流
下继续回流 ,使反应进行完全,冰水浴冷却,搅拌的同时慢慢滴加
,使反应进行完全,冰水浴冷却,搅拌的同时慢慢滴加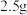 氯化铵配成的饱和水溶液,分解加成产物。
氯化铵配成的饱和水溶液,分解加成产物。
步骤3:分出醚层,蒸去乙醚,剩余物加入 石油醚,搅拌,过滤,收集产品。
石油醚,搅拌,过滤,收集产品。
粗产品用乙醇和水混合溶剂进行重结晶、抽滤、干燥、称量,产物质量为 。
。
回答下列问题:
(1)装置图中c的名称为_______ ,它的作用是_______ ;实验时,冷凝管中的冷却水进口为_______ (填“a”或“b”)。
(2)步骤1中,向三颈烧瓶内放入沸石的目的是_______ 。
(3)步骤2控制滴加速度的原因是_______ 。
(4)步骤3中,分离出醚层的操作名称为_______ 。
(5)三苯基甲醇的产率为_______ (保留三位有效数字)。

已知:①
 的生成和使用时必须在无水条件下进行,痕量水就会发生反应:
的生成和使用时必须在无水条件下进行,痕量水就会发生反应: ;
;②M(溴苯)
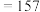 ,M(苯甲酸乙酯)
,M(苯甲酸乙酯) ,M(三苯甲醇)
,M(三苯甲醇)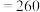 ,M(乙醚)
,M(乙醚) 。
。实验步骤:
步骤1:按如图组装实验装置后,向三颈烧瓶内放入适量镁屑、一小粒碘和沸石,装上带干燥管的回流冷凝管和盛有过量溴苯和
 无水乙醚的恒压滴液漏斗,滴加约三分之一的溴苯乙醚溶液并开动搅拌,慢慢滴入余下的溴苯乙醚溶液,保持反应液呈微沸状态,滴加完毕后,继续回流
无水乙醚的恒压滴液漏斗,滴加约三分之一的溴苯乙醚溶液并开动搅拌,慢慢滴入余下的溴苯乙醚溶液,保持反应液呈微沸状态,滴加完毕后,继续回流 ,使镁屑作用完全。
,使镁屑作用完全。
步骤2:将制备好的过量苯基溴化镁乙醚溶液置于冷水浴中,在搅拌下,滴加
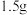 苯甲酸乙酯和
苯甲酸乙酯和 无水乙醚的混合液,控制滴加速度,滴加完毕后,将反应混合物在
无水乙醚的混合液,控制滴加速度,滴加完毕后,将反应混合物在 下继续回流
下继续回流 ,使反应进行完全,冰水浴冷却,搅拌的同时慢慢滴加
,使反应进行完全,冰水浴冷却,搅拌的同时慢慢滴加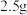 氯化铵配成的饱和水溶液,分解加成产物。
氯化铵配成的饱和水溶液,分解加成产物。步骤3:分出醚层,蒸去乙醚,剩余物加入
 石油醚,搅拌,过滤,收集产品。
石油醚,搅拌,过滤,收集产品。粗产品用乙醇和水混合溶剂进行重结晶、抽滤、干燥、称量,产物质量为
 。
。回答下列问题:
(1)装置图中c的名称为
(2)步骤1中,向三颈烧瓶内放入沸石的目的是
(3)步骤2控制滴加速度的原因是
(4)步骤3中,分离出醚层的操作名称为
(5)三苯基甲醇的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】如图中A是制取溴苯的实验装置,B,C是改进后的装置,请仔细分析对比三个装置,回答以下问题:
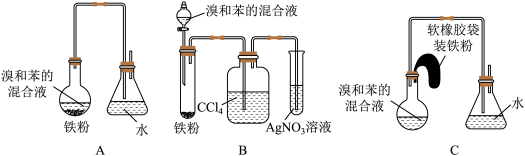
(1)写出三个装置中所共同发生的两个反应的化学方程式:________ 、_____________ 。
(2)写出B装置中盛有AgNO3溶液的试管里所发生反应的离子方程式:__________ 。
(3)装置A和C均采用了长玻璃导管,其作用是________ 。
(4)在按装置B,C装好仪器及药品后要使反应开始,应对装置B进行的操作是_________ ;应对装置C进行的操作是_________ 。
(5)装置B,C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是___________ 。
(6)B中采用了洗气瓶吸收装置,其作用是_________ 。
(7)与装置A和C相比,B装置存在两个明显的缺点,使实验的效果不好或不能正常进行实验。这两个缺点是_________ ;____________ 。

(1)写出三个装置中所共同发生的两个反应的化学方程式:
(2)写出B装置中盛有AgNO3溶液的试管里所发生反应的离子方程式:
(3)装置A和C均采用了长玻璃导管,其作用是
(4)在按装置B,C装好仪器及药品后要使反应开始,应对装置B进行的操作是
(5)装置B,C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是
(6)B中采用了洗气瓶吸收装置,其作用是
(7)与装置A和C相比,B装置存在两个明显的缺点,使实验的效果不好或不能正常进行实验。这两个缺点是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色等。工业上常用辉铋矿(主要成分是 ,还含有少量
,还含有少量 、铁的氧化物等杂质)为原料制备氯氧化铋。
、铁的氧化物等杂质)为原料制备氯氧化铋。 在
在 时开始水解,
时开始水解,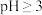 时几乎完全水解为白色的BiOCl沉淀;
时几乎完全水解为白色的BiOCl沉淀;
②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi的价电子排布式为___________ 。
(2)“浸渣”的主要成分是S和___________ ,“浸取”时生成S的离子方程式为___________ 。
(3)“充分搅拌”时加入盐酸羟胺的目的是___________ 。
(4)加入碳酸钠粉末制取BiOCl时,溶液pH值需控制的合理范围为___________ ,发生反应的化学方程式为___________ 。
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入 ,BiOCl被还原为Bi,则阴极的电极反应式是
,BiOCl被还原为Bi,则阴极的电极反应式是___________ 。
(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 ,还含有少量
,还含有少量 、铁的氧化物等杂质)为原料制备氯氧化铋。
、铁的氧化物等杂质)为原料制备氯氧化铋。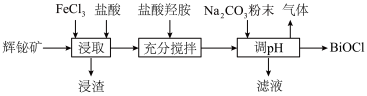
 在
在 时开始水解,
时开始水解,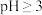 时几乎完全水解为白色的BiOCl沉淀;
时几乎完全水解为白色的BiOCl沉淀;②该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表。
| 金属离子 |  |  |
| 开始沉淀的pH | 1.9 | 7.2 |
| 沉淀完全的pH | 2.9 | 8.2 |
(1)铋与氮同主族,且位于元素周期表的第六周期,基态Bi的价电子排布式为
(2)“浸渣”的主要成分是S和
(3)“充分搅拌”时加入盐酸羟胺的目的是
(4)加入碳酸钠粉末制取BiOCl时,溶液pH值需控制的合理范围为
(5)氯氧化铋(BiOCl)可用作钾离子电池(有机物作离子导体)的负极材料,充电时嵌入
 ,BiOCl被还原为Bi,则阴极的电极反应式是
,BiOCl被还原为Bi,则阴极的电极反应式是(6)铋的一种氧化物的立方晶胞结构如图所示,已知最近的两个铋离子之间的距离为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。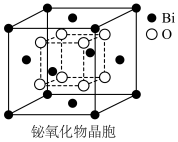
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】金属钛素有“太空金属”、“未来金属”等美誉。工业上,以钛铁矿为原料制备二氧化钛并得到副产品FeSO4·7H2O(绿矾)的工艺流程如下图所示。
酸溶 FeTiO3(s)+2H2SO4(aq)===FeSO4(aq)+TiOSO4(aq)+2H2O(l)
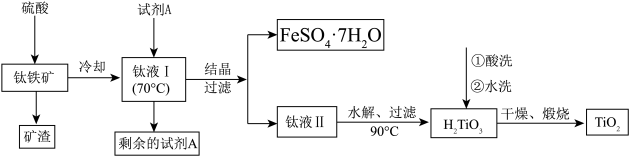
(1)试剂A为____________ 。加入A的目的是 ______________________ (用离子方程式表示)。
(2)钛液Ⅰ需冷却至70 ℃左右,若温度过高会导致产品TiO2回收率降低,原因是_________ 。
(3)请写出钛液Ⅱ水解的化学方程式:_________________ 。取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是_________ (填化学式)。
酸溶 FeTiO3(s)+2H2SO4(aq)===FeSO4(aq)+TiOSO4(aq)+2H2O(l)

(1)试剂A为
(2)钛液Ⅰ需冷却至70 ℃左右,若温度过高会导致产品TiO2回收率降低,原因是
(3)请写出钛液Ⅱ水解的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】甲苯(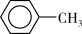 )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛(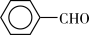 )、苯甲酸(
)、苯甲酸(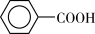 )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
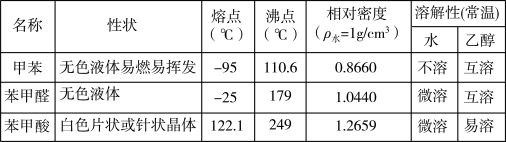
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入2mL甲苯和一定量其它试剂,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。
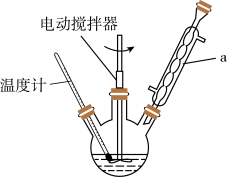
(1)装置a的主要作用是___ 。三颈瓶中发生反应的化学方程式为___ 。
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是___ 。
(3)反应完毕,反应混合液经过自然冷却至室温后,还应经过过滤、___ (填操作名称)等操作,才能得到苯甲醛粗产品。
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,依次进行的操作步骤是___ (按步骤顺序填字母)。
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2
d.与适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸(相对分子质量为122)产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/LKOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为__ (保留一位小数)。
 )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛( )、苯甲酸(
)、苯甲酸( )等产品。下表列出了有关物质的部分物理性质,请回答:
)等产品。下表列出了有关物质的部分物理性质,请回答:
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入2mL甲苯和一定量其它试剂,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的主要作用是
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是
(3)反应完毕,反应混合液经过自然冷却至室温后,还应经过过滤、
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,依次进行的操作步骤是
a.对混合液进行分液
b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2
d.与适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸(相对分子质量为122)产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/LKOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为
您最近一年使用:0次