氯气是一种重要的工业原料。
(1)写出实验室制取氯气反应的化学方程式________________________ 。
(2)资料显示:Ca(ClO)2 +CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
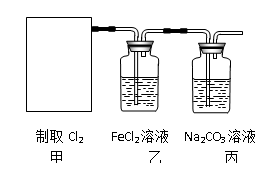
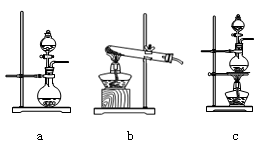
①在该实验中,甲部分的装置是_______ (填字母)。
②乙装置中FeCl2溶液与Cl2反应的离子方程式是________________ 。
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质,这种物质是_______ (化学式)。
④有人认为该实验存在明显的缺陷,如何改进:______________
请你写出Cl2和“④”中“最合适的化学试剂”反应的离子方程式______________ 。
(1)写出实验室制取氯气反应的化学方程式
(2)资料显示:Ca(ClO)2 +CaCl2+2H2SO4
 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
①在该实验中,甲部分的装置是

②乙装置中FeCl2溶液与Cl2反应的离子方程式是
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质,这种物质是
④有人认为该实验存在明显的缺陷,如何改进:
请你写出Cl2和“④”中“最合适的化学试剂”反应的离子方程式
更新时间:2018-12-21 22:14:05
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】利用如所示装置可以验证元素的非金属性的变化规律。
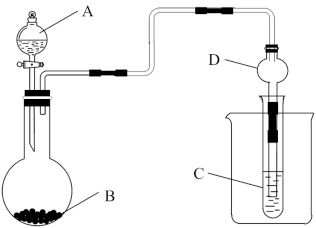
(1)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为_______ 、_______ 、_______ ,装置C中的实验现象为有淡黄色沉淀生成,则反应的离子方程式为_______ 。
(2)若要证明非金属性C>Si,则A中应加入_______ 溶液,B中应加入Na2CO3,装置C中发生的化学反应方程式为_______ 。

(1)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为
(2)若要证明非金属性C>Si,则A中应加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室制取氯气的装置如图所示:
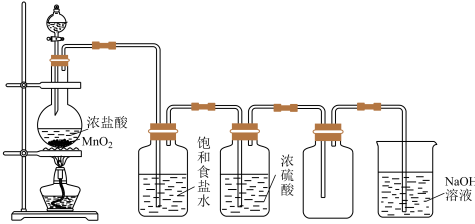
(1)实验原理(制取氯气的反应方程式):___ 。
(2)实验装置:气体制备型化学实验装置的设计,要将化学反应原理、气体净化、收集和尾气处理等结合起来。
实验装置中:①饱和食盐水的作用是除去氯气中的__ ;
②浓硫酸的作用是除去氯气中的__ 。
收集装置中:③该装置中收集氯气使用的是__ 排空气法。
④利用NaOH处理尾气,Cl2与NaOH反应的离子方程式:___ 。
⑤检验氯气是否收集满可用湿润的淀粉KI试纸放在集气瓶口,若试纸__ ,则证明已集满。

(1)实验原理(制取氯气的反应方程式):
(2)实验装置:气体制备型化学实验装置的设计,要将化学反应原理、气体净化、收集和尾气处理等结合起来。
实验装置中:①饱和食盐水的作用是除去氯气中的
②浓硫酸的作用是除去氯气中的
收集装置中:③该装置中收集氯气使用的是
④利用NaOH处理尾气,Cl2与NaOH反应的离子方程式:
⑤检验氯气是否收集满可用湿润的淀粉KI试纸放在集气瓶口,若试纸
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】实验室中所用少量氯气用下列方法制取:4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O试回答下列问题:
Cl2↑+MnCl2+2H2O试回答下列问题:
(1)该反应中___________ 是氧化剂,氧化剂和还原剂的物质的量之比为________ 。写出该反应的离子方程式___________ 。
(2)若用右图装置收集氯气,气体应从___________ 口进入。

(3)氯气有毒、且氯气溶入水显酸性,请写出氯气溶于水的离子方程式___________ ,若吸入大量氯气,可中毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用NaOH溶液来吸收有毒的氯气,化学方程式为____________ 。
 Cl2↑+MnCl2+2H2O试回答下列问题:
Cl2↑+MnCl2+2H2O试回答下列问题:(1)该反应中
(2)若用右图装置收集氯气,气体应从

(3)氯气有毒、且氯气溶入水显酸性,请写出氯气溶于水的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】氯气是一种重要的化工原料,农药的生产及药物的合成都需要用到氯气。某兴趣小组通过以下装置制得纯净的氯气。回答下列问题:
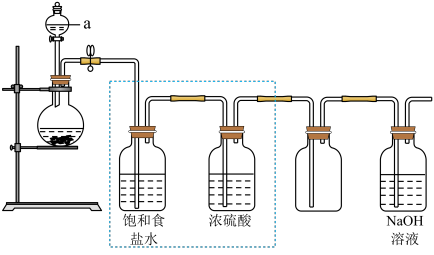
(1)仪器a的名称为__ 。
(2)该实验需要加热,则a中盛装的试剂是__ (填名称),生成氯气的离子方程式为__ 。
(3)若将虚线中的装置去除,则制得的Cl2中混有的杂质为___ (填化学式)。
(4)当集气瓶中___ ,则说明Cl2已收集满;NaOH溶液的作用是___ 。

(1)仪器a的名称为
(2)该实验需要加热,则a中盛装的试剂是
(3)若将虚线中的装置去除,则制得的Cl2中混有的杂质为
(4)当集气瓶中
您最近一年使用:0次
【推荐2】实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。下图是实验室利用此反应制备氯气并进行一系列相关实验的装置(夹持设备已略)。
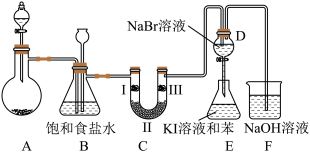
(1)装置B的作用是______ ,实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象:_______ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入______ (选“a”“b”或“c”)
(3)设计装置D、E的目的是为了比较Cl2、Br2、I2的氧化性强弱.已知Br2的水溶液因浓度不同而呈现橙色或红棕色,I2难溶于水而易溶于苯,且I2的苯溶液为紫红色.当向D中缓缓通入足量Cl2时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2,请写出D中对应的离子方程式并用单线桥法表示出电子转移情况:_________ 。打开活塞,将D中的少量溶液加入E中,振荡E,观察到E中溶液分为两层,上层(苯层)为紫红色.该现象______ (填“能”或“不能”)说明Br2的氧化性大于I2。
(4)装置F的作用是除去污染性的物质(Cl2、Br2等),已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3,且 值与温度高低有关.若烧杯中装有500mL 0.2mol/L的NaOH溶液,则最多可吸收标况下的Cl2的体积为
值与温度高低有关.若烧杯中装有500mL 0.2mol/L的NaOH溶液,则最多可吸收标况下的Cl2的体积为______ L(忽略Cl2溶于水)。

(1)装置B的作用是
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | |
| Ⅰ | 干燥的有色布条 | 湿润的有色布条 | 干燥的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F的作用是除去污染性的物质(Cl2、Br2等),已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3,且
 值与温度高低有关.若烧杯中装有500mL 0.2mol/L的NaOH溶液,则最多可吸收标况下的Cl2的体积为
值与温度高低有关.若烧杯中装有500mL 0.2mol/L的NaOH溶液,则最多可吸收标况下的Cl2的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某中学化学实验小组探究Na2O2能否与CO2反应生成O2,用如下的实验装置进行实验:(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)

回答下列问题:
(1)仪器a的名称是____________ ,a中液体试剂应选用_____________ (填“6 mol·L-1盐酸”或“6 mol·L-1硫酸”)。
(2)装置B的作用是______________ ,装置C的作用是_____________ 。
(3)装置D中发生反应的化学方程式是__________________________ 。
(4)装置E中碱石灰的作用是_________________________________ 。
(5)该实验装置中,如何证明Na2O2与CO2反应能否生成O2____________ 。

回答下列问题:
(1)仪器a的名称是
(2)装置B的作用是
(3)装置D中发生反应的化学方程式是
(4)装置E中碱石灰的作用是
(5)该实验装置中,如何证明Na2O2与CO2反应能否生成O2
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】用如图所表示的方法研究金属钠与水反应的性质,其中A是用带孔的铝箔包着的小块的金属钠.

(1)从大块钠上取下的小块钠要用滤纸擦一擦,这样做的目的是_______________ 。
(2)包裹钠块的铝箔要预先扎上足够多的小孔,若孔数不够,可能出现的不良后果是__________ .假如在实验刚开始就将镊子松开拿出水面,A表现出的现象是 _______________________ ,出现这种现象的原因是______________ 。
(3)据预测,钠与水反应生成氢气和氢氧化钠.
证明生成氢氧化钠的实验方法和相应的现象是______________________ ;
(4)已知反应结束后铝箔和钠均消失,请写出相关反应的离子方程式:______________________________

(1)从大块钠上取下的小块钠要用滤纸擦一擦,这样做的目的是
(2)包裹钠块的铝箔要预先扎上足够多的小孔,若孔数不够,可能出现的不良后果是
(3)据预测,钠与水反应生成氢气和氢氧化钠.
证明生成氢氧化钠的实验方法和相应的现象是
(4)已知反应结束后铝箔和钠均消失,请写出相关反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某兴趣小组用下图所示实验装置(部分夹持仪器已略去)制取并探究Cl2的性质,装置(I)中发生反应的化学方程式为: 。
。
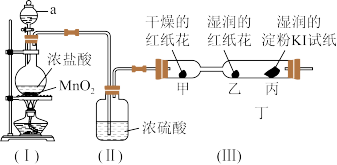
[实验探究]
(1)装置(Ⅰ)中仪器a的名称是_______ 。
(2)装置(Ⅱ)中浓硫酸的作用是_______ 。
(3)实验进行一段时间后,装置(Ⅲ)中的实验现象与分析:
①对甲、乙两处红纸花颜色变化的描述正确的是_______ (填标号)。
A.甲不褪色,乙褪色 B.甲褪色,乙不褪色
②对比甲、乙两处实验现象,可知具有漂白性的物质是_______ (填“Cl2”或“HClO”)。
③丙处淀粉KI试纸变为_______ (填“蓝色”或“红色”),其中Cl2和KI发生反应,补充完整下面的化学方程式: _______。
_______。______
(4)从实验安全和环境保护的角度考虑,该实验存在的一个明显缺陷是_______ 。
(5)用8.7gMnO2固体与足量浓盐酸反应,可生成Cl2气体体积(标准状况下)理论上最多为_______ L。(已知MnO2的摩尔质量为87g/mol)
[知识应用]
Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。
(6)已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、 三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是_______ (填标号)。

A.3~5.5 B.5.5~7.5
 。
。
[实验探究]
(1)装置(Ⅰ)中仪器a的名称是
(2)装置(Ⅱ)中浓硫酸的作用是
(3)实验进行一段时间后,装置(Ⅲ)中的实验现象与分析:
①对甲、乙两处红纸花颜色变化的描述正确的是
A.甲不褪色,乙褪色 B.甲褪色,乙不褪色
②对比甲、乙两处实验现象,可知具有漂白性的物质是
③丙处淀粉KI试纸变为
 _______。
_______。(4)从实验安全和环境保护的角度考虑,该实验存在的一个明显缺陷是
(5)用8.7gMnO2固体与足量浓盐酸反应,可生成Cl2气体体积(标准状况下)理论上最多为
[知识应用]
Cl2常用于饮用水消毒。Cl2溶于水得到氯水,氯水中HClO的浓度越大杀菌能力越强。
(6)已知25℃时,氯水中Cl2(溶于水的氯气分子)、HClO、
 三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
三种微粒所占百分数与pH的关系如图。则用Cl2处理饮用水时,溶液的pH最佳控制范围是
A.3~5.5 B.5.5~7.5
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】氯化铁的熔点为304℃、沸点为316℃,是一种处理工业废水的高效廉价的絮凝剂,易溶于水并有强烈的吸水性。某化学兴趣小组拟利用如图装置来制备无水FeCl3(夹待装置省略)。
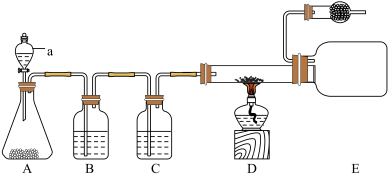
回答下列问题:
(1)仪器a的名称是____ ,装置A中用高锰酸钾固体与浓盐酸反应制取Cl2的化学方程式是____ 。
(2)B中试剂是____ 。球形干燥管中所装试剂为碱石灰,其作用是____ 。
(3)实验时,先通入一段时间的氯气,再点燃酒精灯,原因是____ 。
(4)直接将D装置中的硬质玻璃管插入E装置的广口瓶中,其目的是____ 。
(5)实验结束后,若将D中所得固体加水溶解后,测得溶液中有Fe2+存在。用离子方程式解释可能的原因____ 。

回答下列问题:
(1)仪器a的名称是
(2)B中试剂是
(3)实验时,先通入一段时间的氯气,再点燃酒精灯,原因是
(4)直接将D装置中的硬质玻璃管插入E装置的广口瓶中,其目的是
(5)实验结束后,若将D中所得固体加水溶解后,测得溶液中有Fe2+存在。用离子方程式解释可能的原因
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】NaClO2用于棉、麻、粘胶纤维及织物的漂白。实验室制备NaClO2的装置如下图所示:
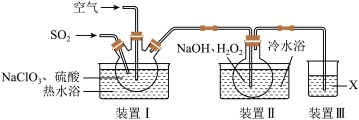
装置Ⅱ中反应生成NaClO2的化学方程式为____________________ 。反应后的溶液中阴离子除了 、
、 、Cl-、ClO-、OH-外还可能含有的一种阴离子是
、Cl-、ClO-、OH-外还可能含有的一种阴离子是_________ ,检验该离子的方法是____________ 。

装置Ⅱ中反应生成NaClO2的化学方程式为
 、
、 、Cl-、ClO-、OH-外还可能含有的一种阴离子是
、Cl-、ClO-、OH-外还可能含有的一种阴离子是
您最近一年使用:0次
【推荐3】普通立德粉(BaSO4·ZnS)广泛用于工业生产中,可利用ZnSO4和BaS共沉淀法制备。以粗氧化锌(含Zn、CuO、FeO等杂质)和BaSO4为原料制备立德粉的流程如下:
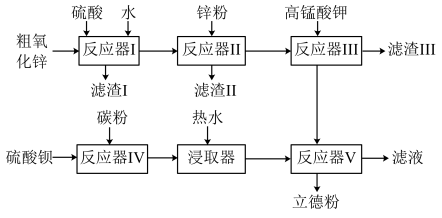
(1)生产ZnSO4的过程中,反应器Ⅰ要保持强制通风,原因是___ 。
(2)加入锌粉的主要目的是___ (用离子方程式表示)。
(3)已知KMnO4在酸性溶液中被还原为Mn2+,在弱酸性、弱碱性溶液中被还原为MnO2,在碱性溶液中被还原为MnO42-。据流程判断,加入KMnO4时溶液的pH应调至___ ;
a.2.2~2.4 b.5.2~5.4 c.12.2~12.4
滤渣Ⅲ的成分为____ 。
(4)制备BaS时,按物质的量之比计算,BaSO4和碳粉的投料比要大于1:2,目的是__ ;生产过程中会有少量氧气进入反应器Ⅳ,反应器Ⅳ中产生的尾气需用碱液吸收,原因是__ 。
(5)普通立德粉(BaSO4·ZnS)中ZnS含量为29.4%,高品质银印级立德粉中ZnS含量为62.5%。在ZnSO4、BaS、Na2SO4、Na2S中选取三种试剂制备银印级立德粉,所选试剂为___ ,反应的化学方程式为__ (已知BaSO4相对分子质量为233,ZnS相对分子质量为97)。

(1)生产ZnSO4的过程中,反应器Ⅰ要保持强制通风,原因是
(2)加入锌粉的主要目的是
(3)已知KMnO4在酸性溶液中被还原为Mn2+,在弱酸性、弱碱性溶液中被还原为MnO2,在碱性溶液中被还原为MnO42-。据流程判断,加入KMnO4时溶液的pH应调至
a.2.2~2.4 b.5.2~5.4 c.12.2~12.4
滤渣Ⅲ的成分为
(4)制备BaS时,按物质的量之比计算,BaSO4和碳粉的投料比要大于1:2,目的是
(5)普通立德粉(BaSO4·ZnS)中ZnS含量为29.4%,高品质银印级立德粉中ZnS含量为62.5%。在ZnSO4、BaS、Na2SO4、Na2S中选取三种试剂制备银印级立德粉,所选试剂为
您最近一年使用:0次




