化学键的键能是指形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知热化学方程式:S(g)+O2(g)===SO2(g) ΔH=-297.23 kJ·mol-1,分析下列说法中正确的是
| A.S(g)+O2(g)===SO2(l) |ΔH|>297.23 kJ·mol-1 |
| B.S(g)+O2(g)===SO2(l) |ΔH|<297.23 kJ·mol-1 |
| C.1 mol SO2的键能总和等于1 mol S和1 mol O2的键能之和 |
| D.1 mol SO2的键能总和小于1 mol S和1 mol O2的键能之和 |
更新时间:2018-12-28 09:43:13
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】我国成功发射“天宫一号”飞行器的长征Ⅱ火箭推进器中盛有强还原剂液态肼(N2H4)和液态四氧化二氮(N2O4)。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。
已知:①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4
上述反应中ΔH4=
已知:①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4
上述反应中ΔH4=
| A.2ΔH3-2ΔH2-ΔH1 | B.2ΔH3+2ΔH2-ΔH1 |
| C.2ΔH3-2ΔH2+ΔH1 | D.-2ΔH3-2ΔH2-ΔH1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】盖斯是热化学的奠基人,他于1840年提出盖斯定律,对这一定律的理解,以下说法不正确的是
| A.不管化学反应是一步完成或分几步完成,其反应热是相同的 |
| B.化学反应的反应热只与反应体系的始态和终态有关,而与反应途径无关 |
| C.可以直接测量任意一反应的反应热 |
| D.可以用已经精确测定的反应热效应来计算难于测量或不能测量的反应的热效应 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】已知某化学反应 ,其反应过程中体系的能量变化如图所示,则下列说法正确的是
,其反应过程中体系的能量变化如图所示,则下列说法正确的是

 ,其反应过程中体系的能量变化如图所示,则下列说法正确的是
,其反应过程中体系的能量变化如图所示,则下列说法正确的是
A.该反应的热效应为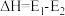 |
| B.图中A…B…C过渡态存在是因为使用了催化剂 |
C. 为正反应的活化能 为正反应的活化能 |
D.该反应中,反应物的键能总和等于 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】甲醇是重要的化工原料,工业上由CO、 和
和 合成甲醇的主要反应如下:
合成甲醇的主要反应如下:
I.

II.

III.

已知:反应Ⅲ中相关化学键的数据如下表
则 键的键能a为
键的键能a为
 和
和 合成甲醇的主要反应如下:
合成甲醇的主要反应如下:I.


II.


III.


已知:反应Ⅲ中相关化学键的数据如下表
| 化学键 |  |  |  |  |  |
键能/ | 436 | 343 | a | 465 | 413 |
 键的键能a为
键的键能a为| A.1076 | B.826 | C.779 | D.538 |
您最近半年使用:0次



