W、X、Y、Z 是原子序数依次增大的四种短周期元素。W 的气态氢化物能使紫色石蕊溶液变蓝,W、X和Y三种元素的最高价氧化物的水化物两两之间可以发生反应,W、X、Y、Z 的最外层电子数之和为 16。回答下列问题:
(1)Z 单质的电子式是________________ 。W 的气态氢化物能使紫色石蕊溶液变蓝的原因:__________________ (用化学方程式表示)。
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是:_____ 。
(3)Z 最高价氧化物对应的水化物化学式为____ 。
(4)Z 和氧元素、硫元素组成的 SOZ2 是一种液态化合物,沸点为 77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出, 该气体可使滴有品红试液的滤纸褪色。请写出 SOZ2 和水反应的化学方程式_____ 。
(1)Z 单质的电子式是
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是:
(3)Z 最高价氧化物对应的水化物化学式为
(4)Z 和氧元素、硫元素组成的 SOZ2 是一种液态化合物,沸点为 77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出, 该气体可使滴有品红试液的滤纸褪色。请写出 SOZ2 和水反应的化学方程式
更新时间:2019-01-09 16:43:54
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】某些简单原子的原子结构可用如图形象地表示:

其中“●”表示质子或电子,“○”表示中子,
(1)下列有关叙述正确的是_____ (填序号)。
(2)科学家已经发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2具有相同的_____ (填序号)。
(3)由②和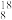 O组成的11克水中,含有中子数的物质的量为
O组成的11克水中,含有中子数的物质的量为______ ;含有电子数目为_____ 。
(4)某元素的核素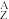 X,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol•L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
X,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol•L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
①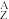 X的质量数A是
X的质量数A是_____ 。
②37gXCl2中所含质子数的物质的量为_____ 。
(5)碲被誉为工业领域的“维生素”,碲在元素周期表中表示如图,写出Te、S、Cl三种元素对应简单氢化物的还原性由强到弱的顺序_____ (用化学式表示)。


其中“●”表示质子或电子,“○”表示中子,
(1)下列有关叙述正确的是
| A.①②③是不同元素的原子 | B.①②③是三种化学性质不同的粒子 |
| C.①②③互为同位素 | D.①②③具有相同的质量数 |
| A.原子数 | B.分子数 | C.体积 | D.电子数 |
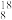 O组成的11克水中,含有中子数的物质的量为
O组成的11克水中,含有中子数的物质的量为(4)某元素的核素
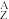 X,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol•L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:
X,1.11g该核素的氯化物XCl2配成的溶液需用20mL1mol•L-1的AgNO3溶液才能把Cl-完全沉淀下来,已知此核素中质子数与中子数相等,则:①
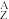 X的质量数A是
X的质量数A是②37gXCl2中所含质子数的物质的量为
(5)碲被誉为工业领域的“维生素”,碲在元素周期表中表示如图,写出Te、S、Cl三种元素对应简单氢化物的还原性由强到弱的顺序

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的应用。
完成下列填空:
(1)镓(Ga)与铝同主族,镓的氯化物与氨水反应的化学方程式:____________________________ 。
(2)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:2Al+4BaO 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3
常温下Al的金属性比Ba的金属性________ (填“强”或“弱”)。利用上述方法可制取Ba的主要原因是__________________________ 。
a.高温时Al的活泼性大于Ba
b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定
d.Ba的沸点比Al的低
完成下列填空:
(1)镓(Ga)与铝同主族,镓的氯化物与氨水反应的化学方程式:
(2)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:2Al+4BaO
 3Ba↑+BaO·Al2O3
3Ba↑+BaO·Al2O3常温下Al的金属性比Ba的金属性
a.高温时Al的活泼性大于Ba
b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定
d.Ba的沸点比Al的低
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C、D是原子序数依次增大的同一短同期元素,A、B是金属元素,C、D是非金属元素。
(1)AB各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为___________________________ 。
(2)A与C 可形成化合物A2C,该化合物的电子式为_______________________ 。
(3)C的低价氧化物通入D单质的水溶液中,发生反应的化学方程式为________________________________________ 。
(4)ABCD四种元素简单离子的离子半径由大到小的顺序是(用离子符号表示):____ 。
(5)四种元素中金属性最强的(填元素符号)______ ;非金属性最强的__________
(1)AB各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为
(2)A与C 可形成化合物A2C,该化合物的电子式为
(3)C的低价氧化物通入D单质的水溶液中,发生反应的化学方程式为
(4)ABCD四种元素简单离子的离子半径由大到小的顺序是(用离子符号表示):
(5)四种元素中金属性最强的(填元素符号)
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】汽车安全气囊中的填充物有NaN3 (叠氮酸钠)、 、
、 等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:
等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:
(1)写出N2的电子式:_______ 。
(2)NaN3是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。NaN3晶体中存在的化学键类型是_______ 。
(3)汽车安全气囊填充物的三种物质中属于共价化合物的是_______ (填写化学式),所涉及的5种元素中,原子半径最大的是_______ (填写元素符号)。
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: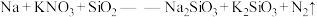 (未配平)。
(未配平)。
(4)写出配平后完整的化学方程式,并用单线桥法标出电子转移的方向和数目_______ 。
(5)结合金属钠的化学性质,说明汽车安全气囊中填充 、
、 的目的
的目的_______ 。
(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的NaN3质量是_______ 。
 、
、 等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:
等物质,NaN3遇撞击时能生成金属钠和N2。完成下列填空:(1)写出N2的电子式:
(2)NaN3是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。NaN3晶体中存在的化学键类型是
(3)汽车安全气囊填充物的三种物质中属于共价化合物的是
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式为:
,化学方程式为: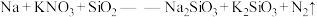 (未配平)。
(未配平)。(4)写出配平后完整的化学方程式,并用单线桥法标出电子转移的方向和数目
(5)结合金属钠的化学性质,说明汽车安全气囊中填充
 、
、 的目的
的目的(6)某品牌汽车设计安全气囊受撞击时需产生44.8L气体(已换算至标准状况下的体积),则该安全气囊中需填充的NaN3质量是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】氮是生命的基础,由于存在着氮的循环,生命世界才能像我们所见到的那样生机勃勃,充满活力.如图是自然界中氮的循环图,请分析此图并回答有关问题.
(1)大气中的氮以_____ (填化学式)形式存在。图中共表示了_______ 种固氮的途径。
(2)由图可知,动植物体内的氮主要存在于蛋白质中,当动植物尸体发生腐败时,往往会产生一种含氮的气体,其电子式为___________ 。土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:K2S+KNO3+H2O N2+K2SO4+KOH
N2+K2SO4+KOH
(3)上述反应中涉及1~18号元素的原子半径从大到小的顺序是_________________ 。属于共价化合物的反应物(或生成物)的结构式是_____________ 。
(4)配平上述反应方程式,并标出电子转移的方向和数目_____________ 。上述反应的氧化剂是_________________ ,被氧化的元素是____________________ 。
(5)上述过程的发生改变了土壤的成分,从而对农业生产产生一定的不利影响,请选择任一角度进行简要说明:_______________________ 。
(6)工业合成氨的简易流程如下图,通过循环Ⅰ可利用的气态物质是_____________

a.催化剂 b.只有N2 c.只有H2 d.N2和H2

(1)大气中的氮以
(2)由图可知,动植物体内的氮主要存在于蛋白质中,当动植物尸体发生腐败时,往往会产生一种含氮的气体,其电子式为
 N2+K2SO4+KOH
N2+K2SO4+KOH(3)上述反应中涉及1~18号元素的原子半径从大到小的顺序是
(4)配平上述反应方程式,并标出电子转移的方向和数目
(5)上述过程的发生改变了土壤的成分,从而对农业生产产生一定的不利影响,请选择任一角度进行简要说明:
(6)工业合成氨的简易流程如下图,通过循环Ⅰ可利用的气态物质是

a.催化剂 b.只有N2 c.只有H2 d.N2和H2
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】有A、B、C、D、E五种短周期元素,其元素特征信息如下表,回答下列问题:
(1)写出下列元素的名称:C________ ,E________ ;元素E在元素周期表中的位置是__________ 。
(2)写出A、B、C形成的化合物M的电子式________ ;B和C的离子中,半径较小的是______ (填离子符号 );五种原子中半径最大的是________ (填元素符号 )。五种元素最高价氧化物的水化物酸性最强的是(以上填化学式)________________________________ 。
(3)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为________ 。
(4)D单质与M的水溶液反应的离子方程式:________ 。
元素编号 | 元素特征信息 |
A | 其单质是密度最小的物质 |
B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
D | 其氢氧化物和氧化物都有两性,与C同周期 |
E | 与C同周期,原子半径在该周期最小 |
(1)写出下列元素的名称:C
(2)写出A、B、C形成的化合物M的电子式
(3)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为
(4)D单质与M的水溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】(I)俄美科学家联合小组宣布合成出114号元素(FI)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中位于第______ 周期,_____ 族,属于金属元素还是非金属元素?____
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式________ 。
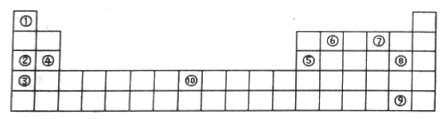
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为__________ 。
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为___________ 。
(3)元素⑩的单质与⑦的氢化物高温下反应的化学方程式为___________ 。
(III)判断以下叙述正确的是__________ 。
部分短周期元素的原子半径及主要化合价
A. L2+、R2-的核外电子数相等
B. 单质与稀盐酸反应的速率L<Q
C. M与T形成的化合物一定具有两性
D. 氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中位于第
(2)如果该元素存在最高价氧化物对应的水化物,请写出其化学式
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)元素⑦的氢化物与⑧的单质反应的离子方程式为
(2)元素②和⑤的最高价氧化物的水化物相互反应的化学方程式为
(3)元素⑩的单质与⑦的氢化物高温下反应的化学方程式为
(III)判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A. L2+、R2-的核外电子数相等
B. 单质与稀盐酸反应的速率L<Q
C. M与T形成的化合物一定具有两性
D. 氢化物的沸点为HnT>HnR
E. M的单质能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】随着原子序数的递增,八种短周期元素(用字母x、y、z…・表示)的原子半径的相对大小、最高正价或最低负价的变化如下图所示。请根据判断出的元素回答下列问题
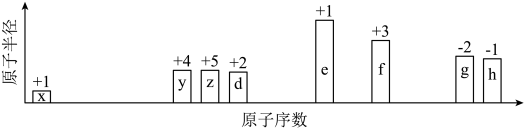
(1)f在元素周期表中的位置是第三周期第____ 族。
(2)比较d、e常见离子的半径大小:_______ (用化学符号表示且用“>”连接,下同)。比较g、h的最高价氧化物对应的水化物的酸性强弱:_______
(3)写出x与z形成的常见四原子共价化合物的电子式_______
(4)物质A是一种常用的比水轻的有机溶剂,其仅由x、y两种元素组成,且y元素与x元素的质量比为12:1,A的相对分子质量为78。A与浓硫酸、浓硝酸在50~60℃下发生反应的化学方程式为__________ ,反应类型为__________ 。
(5)f的最高价氧化物对应的水化物可以与e的最高价氧化物对应的水化物反应,请写出该反应的离子方程式:_______________ 。

(1)f在元素周期表中的位置是第三周期第
(2)比较d、e常见离子的半径大小:
(3)写出x与z形成的常见四原子共价化合物的电子式
(4)物质A是一种常用的比水轻的有机溶剂,其仅由x、y两种元素组成,且y元素与x元素的质量比为12:1,A的相对分子质量为78。A与浓硫酸、浓硝酸在50~60℃下发生反应的化学方程式为
(5)f的最高价氧化物对应的水化物可以与e的最高价氧化物对应的水化物反应,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为______ (填元素符号);
②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______ (填化学式)。
(2)①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:___________ 。
(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)___________ 。
a.MnO2 b.FeCl3 c.Na2SO3 d.CaCO3
(4)由表中元素形成的物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为________________ 。
| IA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)④、⑤、⑥的原子半径由大到小的顺序为
②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(2)①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
(3)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.FeCl3 c.Na2SO3 d.CaCO3
(4)由表中元素形成的物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】随着原子序数的递增,八种短周期元素(用字母x、y、z…・表示)的原子半径的相对大小、最高正价或最低负价的变化如下图所示。请根据判断出的元素回答下列问题

(1)f在元素周期表中的位置是第三周期第____ 族。
(2)比较d、e常见离子的半径大小:_______ (用化学符号表示且用“>”连接,下同)。比较g、h的最高价氧化物对应的水化物的酸性强弱:_______
(3)写出x与z形成的常见四原子共价化合物的电子式_______
(4)物质A是一种常用的比水轻的有机溶剂,其仅由x、y两种元素组成,且y元素与x元素的质量比为12:1,A的相对分子质量为78。A与浓硫酸、浓硝酸在50~60℃下发生反应的化学方程式为__________ ,反应类型为__________ 。
(5)f的最高价氧化物对应的水化物可以与e的最高价氧化物对应的水化物反应,请写出该反应的离子方程式:_______________ 。

(1)f在元素周期表中的位置是第三周期第
(2)比较d、e常见离子的半径大小:
(3)写出x与z形成的常见四原子共价化合物的电子式
(4)物质A是一种常用的比水轻的有机溶剂,其仅由x、y两种元素组成,且y元素与x元素的质量比为12:1,A的相对分子质量为78。A与浓硫酸、浓硝酸在50~60℃下发生反应的化学方程式为
(5)f的最高价氧化物对应的水化物可以与e的最高价氧化物对应的水化物反应,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.A、D同主族,C、E同主族,D、E、F同周期.A、B的原子最外层电子数之和与C原子的最外层电子数相等.A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子(题中的字母只代表元素代号,与实际元素符号无关).
请回答下列问题:
(1)A~F六种元素原子,原子半径最大的是 (填对应的元素符号).
(2)A与B两种元素组成一种阳离子,该离子符号为 .
(3)C、D两种元素组成的化合物的化学式是 .
(4)E、F两种元素中非金属性较强的是 ,能够证明这一结论的化学事实是 .
请回答下列问题:
(1)A~F六种元素原子,原子半径最大的是 (填对应的元素符号).
(2)A与B两种元素组成一种阳离子,该离子符号为 .
(3)C、D两种元素组成的化合物的化学式是 .
(4)E、F两种元素中非金属性较强的是 ,能够证明这一结论的化学事实是 .
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】(1)X原子有两个电子层,它能与最活泼的金属Y形成 的化合物,X是
的化合物,X是_______ 元素(写元素符号)。
(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是_______ 元素(写元素符号),n=_______ 。
(3)下表是元素周期表的一部分,回答有关问题:
①在这些元素中,最不活泼的元素的结构示意图是______________
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为___________ ;碱性最强的与呈两性的发生反应的离子方程式__________
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有___________
④用电子式表示由元素(8)和(10)形成化合物的过程:_________________
 的化合物,X是
的化合物,X是(2)6C元素能够与某非金属元素R形成化合物CRn,已知CRn分子中各原子核外最外层电子总数为32,核外电子数总和为74,则R是
(3)下表是元素周期表的一部分,回答有关问题:
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | (1) | (2) | ||||||
| 3 | (3) | (4) | (5) | (6) | (7) | (8) | (9) | |
| 4 | (10) | (11) | (12) |
①在这些元素中,最不活泼的元素的结构示意图是
②在这些元素的最高价氧化物对应的水化物中,酸性最强的与呈两性的发生反应的化学方程式为
③元素(8)、(11)和氧元素形成一种广泛使用杀菌消毒剂,该物质中存在的化学键有
④用电子式表示由元素(8)和(10)形成化合物的过程:
您最近一年使用:0次



