下列描述中正确的是
| A.已知C(石墨,s)=C(金刚石,s) ∆H=+1.9kJ·mol-1,则由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 |
| B.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的∆H=2×(+283.0) kJ·mol-1 |
| C.有些化学反应的发生不会伴随着能量的变化 |
| D.已知2H2(g)+O2(g)=2H2O(g) ∆H=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ∙mol-1 |
更新时间:2019-01-10 17:16:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】科研人员通过控制光沉积的方法构建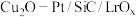 型复合材料光催化剂,然后以Fe2+和Fe3+离子渗透
型复合材料光催化剂,然后以Fe2+和Fe3+离子渗透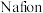 膜在酸性介质下构建了一个还原和氧化反应分离的人工光合体系,其反应机理如图:
膜在酸性介质下构建了一个还原和氧化反应分离的人工光合体系,其反应机理如图:

下列说法正确的是
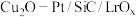 型复合材料光催化剂,然后以Fe2+和Fe3+离子渗透
型复合材料光催化剂,然后以Fe2+和Fe3+离子渗透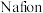 膜在酸性介质下构建了一个还原和氧化反应分离的人工光合体系,其反应机理如图:
膜在酸性介质下构建了一个还原和氧化反应分离的人工光合体系,其反应机理如图:
下列说法正确的是
| A.该反应能量转化形式为光能→化学能 |
B.该人工光合体系的总反应为 |
| C.图中a、b分别代表Fe3+、Fe2+ |
D.Cu2O→Pt上发生的反应为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关叙述正确的是
| A.高温下进行的反应都是吸热反应,常温下能够进行的反应都是放热反应 |
B.实验室用4mol SO2与2mol O2进行下列反应:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为80% 2SO3(g)ΔH=-196.64kJ/mol,当放出314.624kJ热量时,SO2的转化率为80% |
| C.常温下,向纯水中通入一定量二氧化硫,则水的电离平衡被促进 |
| D.向3mL0.1mol/LAgNO3溶液中滴入5滴0.1mol/L NaCl溶液产生白色沉淀,再滴入KI稀溶液沉淀显黄色,则Ksp(AgI)<Ksp(AgCl) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】图象可直观地表现化学变化中的物质变化和能量变化。下列判断错误的是


A.图甲所示反应为放热反应。且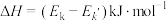 |
| B.已知石墨比金刚石稳定,则金刚石转化为石墨过程中的能量变化如图乙 |
C.图丙所示反应的热化学方程式为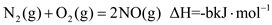 |
D.若 的能量变化如图丁,则 的能量变化如图丁,则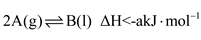 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一些烷烃的燃烧热如下表:
下列说法正确的是
| 化合物 | ΔH/(kJ·mol-1) | 化合物 | ΔH/(kJ·mol-1) |
| 甲烷 | -891.0 | 正丁烷 | -2878.0 |
| 乙烷 | -1560.8 | 异丁烷 | -2869.6 |
| 丙烷 | -2221.5 | 2-甲基丁烷 | -3531.3 |
| A.正戊烷的燃烧热大约是3540 kJ·mol-1 |
| B.热稳定性:正丁烷>异丁烷 |
| C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8 kJ·mol-1 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】正交硫在一定条件下可以转化为单斜硫,能量变化如图所示。在该条件下,下列说法正确的是
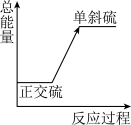

| A.单斜硫比正交硫更稳定 |
| B.1 mol S(单斜硫)比1 mol S(正交硫)的总能量高 |
| C.正交硫转化为单斜硫是放热反应 |
| D.等质量的单斜硫和正交硫完全燃烧释放的能量一样多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于热化学方程式的叙述正确的是
A.已知石墨比金刚石稳定,则C(石墨,s) C(金刚石,s) C(金刚石,s)  |
B.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
C.稀盐酸和稀氢氧化钠溶液混合,其热化学方程式为 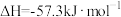 |
D.甲烷的燃烧热为890.3 ,热化学方程式为 ,热化学方程式为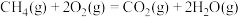  |
您最近一年使用:0次
【推荐3】下列说法或表示法正确的是
| A.等量的白磷蒸气和白磷固体分别完全燃烧,后者放出热量多 |
| B.由C(s,石墨)=C(s,金刚石) ΔH=+1.19 kJ·mol-1可知,金刚石比石墨稳定 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:N2(g)+3H2(g)  2NH3(g) △H = -92.2 kJ/mol。下列说法
2NH3(g) △H = -92.2 kJ/mol。下列说法不正确 的是
 2NH3(g) △H = -92.2 kJ/mol。下列说法
2NH3(g) △H = -92.2 kJ/mol。下列说法| A.1 mol N2(g)和3 mol H2(g)的能量之和高于2 mol NH3 (g)的能量 |
| B.形成2 mol NH3(g)的化学键释放的总能量大于断裂1 mol N2 (g) 和3 mol H2 (g) 的化学键所吸收的总能量 |
| C.加入催化剂是为了加大反应速率,缩短生产周期,降低生产成本 |
| D.将1 mol N2(g)和3 mol H2(g)充入一密闭容器中充分反应,放出92.2 kJ 的热量 |
您最近一年使用:0次
【推荐2】已知反应 ( aq)+2I-(aq)
( aq)+2I-(aq) 2
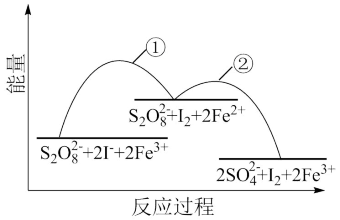
2 (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是
①2Fe3+(aq)+2I-(aq) I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
②2Fe2+( aq)+ (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
 ( aq)+2I-(aq)
( aq)+2I-(aq) 2
2 (aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是
(aq)+I2(aq),若向该溶液中加入含Fe3+的某溶液,反应机理如图所示。下列有关说法错误的是①2Fe3+(aq)+2I-(aq)
 I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)②2Fe2+( aq)+
 (aq)=2Fe3+(aq)+2
(aq)=2Fe3+(aq)+2 (aq)
(aq)
| A.反应①和反应②相比,反应②更快 |
| B.Fe3+是该反应的催化剂 |
| C.增大Fe3+的浓度,能够加快反应速率 |
| D.若不加Fe3+,正反应的活化能比逆反应的活化能大 |
您最近一年使用:0次

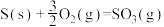

 )的燃烧热的热化学方程式:
)的燃烧热的热化学方程式: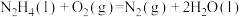

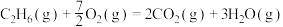
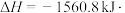


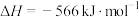
 和
和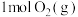 反应生成
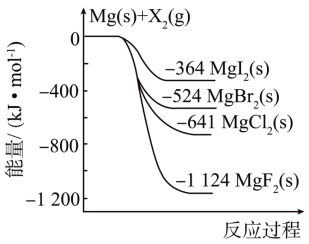
反应生成 过程中的能量变化,下列说法正确的是
过程中的能量变化,下列说法正确的是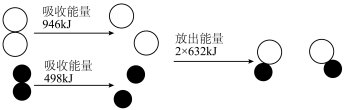
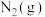 和
和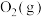 反应生成
反应生成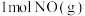 吸收能量为180kJ
吸收能量为180kJ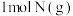 和
和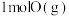 总能量比
总能量比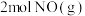 能量高
能量高

