下列推理错误的是( )
| A.酸性强弱比较:HClO4>H2SO4>H3PO4>H2SiO3 |
| B.溶解度大小比较:Mg(OH)2> Ba(OH)2 |
| C.碱性大小比较:Pb(OH)4>Sn(OH)4>Ge(OH)4 |
| D.稳定性:H2O>H2S>H2Se>H2Te |
更新时间:2019-04-16 15:51:48
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列各组顺序的排列正确的是
| A.最高正价:P<S<Cl<Ar | B.热稳定性:H2O>HF>HCl |
| C.酸性强弱:HNO3<H2CO3<H3PO4 | D.还原性 F- <Cl-<Br- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】现有四种元素的基态原子的电子排布式如下:①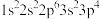 ;②
;②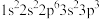 ;③
;③ ;④
;④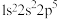 。则下列有关比较中正确的是
。则下列有关比较中正确的是
| A.第一电离能:④>③>①>② | B.原子半径:④>③>②>① |
| C.电负性:④>③>①>② | D.最高正化合价:④>①>③=② |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关碱金属铷(Rb)的叙述中,不正确的是
| A.Rb2CO3易溶、易电离 |
| B.Rb位于周期表第五周期第IA族 |
| C.在钠、钾、铷三种单质中,铷的熔点最高 |
| D.氢氧化铷与盐酸反应的离子方程式是OH-+H+=H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据原子结构及元素周期律的知识,下列推断正确的是( )
| A.核外电子排布相同的微粒化学性质也相同 |
B. Cl与 Cl与 Cl得电子能力相同 Cl得电子能力相同 |
| C.Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐1】已知33As、35Br位于同一周期,下列关系正确的是
| A.原子半径:As>Cl>P | B.热稳定性:HCl>AsH3>HBr |
| C.还原性:As3->S2->Cl- | D.酸性:H3AsO4>H2SO4>H3PO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
名校
【推荐2】工业上电解熔融 和冰晶石
和冰晶石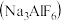 的混合物可制得铝。下列说法正确的是
的混合物可制得铝。下列说法正确的是
 和冰晶石
和冰晶石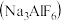 的混合物可制得铝。下列说法正确的是
的混合物可制得铝。下列说法正确的是A.半径大小: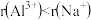 | B.电负性大小: |
C.电离能大小: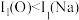 | D.碱性强弱: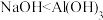 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、W、R的原子序数依次增加,X、Y、W位于不同周期,原子序数:3Y=Z+R,常温下X与Y可组成两种液态二元化合物。某种缓冲溶液的主要成分结构如图。下列说法错误的是
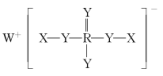
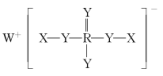
| A.R的最高价氧化物对应的水化物为强酸 |
| B.简单氢化物的稳定性:Y<Z |
| C.X、W均能与Y形成具有漂白性的化合物 |
| D.简单离子半径:Y>Z>W |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X元素的最高价含氧酸能与其气态氢化物化合生成盐。下列说法不正确的是
| X | Y | |
| Z | W |
| A.原子半径:Z>W>X>Y |
| B.元素X、Z、W、Y的最高化合价分别与其主族序数相等 |
| C.H4ZO4和H3WO4是弱酸 |
| D.最高价氧化物对应水化物的酸性:X>W>Z |
您最近一年使用:0次

 、
、 、
、 的酸性依次增强
的酸性依次增强
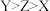

 分子的
分子的 模型为三角锥形
模型为三角锥形

