按要求完成下列方程式
(1)磁性氧化铁与足量的稀硝酸反应的离子方程式:________
(2)铜与硫共热的化学方程式:_________
(3)二氧化氮通入水中的化学方程式:________
(4)氨的催化氧化的化学方程式:___________
(5)往Ba(OH)2溶液中滴加NaHSO4溶液使溶液呈中性的离子方程式:________
(1)磁性氧化铁与足量的稀硝酸反应的离子方程式:
(2)铜与硫共热的化学方程式:
(3)二氧化氮通入水中的化学方程式:
(4)氨的催化氧化的化学方程式:
(5)往Ba(OH)2溶液中滴加NaHSO4溶液使溶液呈中性的离子方程式:
更新时间:2019-04-21 17:41:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】写出下列方程式
(1)写出下列物质的电离方程式:
①AlCl3___________ ,
②Fe2(SO4)3___________ ,
(2)写出下列反应的化学方程式:
①稀盐酸与氢氧化镁反应___________ ,
②硝酸银溶液与氯化钾反应___________ ;
(3)写出下列反应的离子方程式:
①稀盐酸与碳酸钙反应___________ ,
②氢氧化钡溶液与稀硫酸反应___________ ;
(1)写出下列物质的电离方程式:
①AlCl3
②Fe2(SO4)3
(2)写出下列反应的化学方程式:
①稀盐酸与氢氧化镁反应
②硝酸银溶液与氯化钾反应
(3)写出下列反应的离子方程式:
①稀盐酸与碳酸钙反应
②氢氧化钡溶液与稀硫酸反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】综合利用CO2对构建低碳社会、促进工业可持续发展有重要意义。
途径1:可用工业废气中二氧化碳制备再生能源物质——甲醇。反应原理为:CO2(g)+3H2(g)⇌CH3OH(g) + H2O(g) +53.7kJ
某温度下,向2L密闭容器中通入0.04 mol CO2和0.08 mol H2,测得其压强(p)随时间(t)变化(如图1中)曲线I所示。
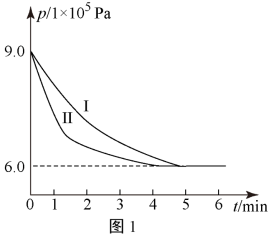
(1)以CO2来表示5 min内的化学反应反应速率υ(CO2)=_______ 。
(2)若只改变某一条件,其他条件相同时,曲线变化为II,则改变的条件是_______ 。
途径2:还可以通过以下途径实现CO2向CH3OH的转化(Q1、Q2均大于0):
反应I:CO2(g)+H2(g)⇌H2O(g)+CO(g)+Q1
反应Ⅱ:2H2(g)+CO(g)⇌CH3OH(g)+Q2
反应I和反应Ⅱ的平衡常数K随温度T的变化如图2所示。
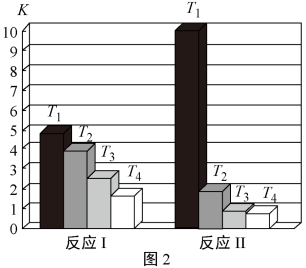
(3)根据图中数据分析可知,T1_______ T2(选填“>”、“<”或“=”);
(4)目前,许多国家采用CO2代替CO(以煤和天然气为原料)生产CH3OH。请阐述理由:_______
(5)0.02molCO2通入含有10mL 3 mol/L NaOH溶液中:
①所得溶液中取2mL,滴加几滴稀Ba(OH)2溶液,c(CO )
)_______ (选填“增大、减小、不变、无法确定”),写出反应的离子方程式_______ ;
②反应后的溶液还能吸收CO2的物质的量是_______ ;
③反应后的溶液中离子浓度由大到小的顺序排列_______ 。
途径1:可用工业废气中二氧化碳制备再生能源物质——甲醇。反应原理为:CO2(g)+3H2(g)⇌CH3OH(g) + H2O(g) +53.7kJ
某温度下,向2L密闭容器中通入0.04 mol CO2和0.08 mol H2,测得其压强(p)随时间(t)变化(如图1中)曲线I所示。

(1)以CO2来表示5 min内的化学反应反应速率υ(CO2)=
(2)若只改变某一条件,其他条件相同时,曲线变化为II,则改变的条件是
途径2:还可以通过以下途径实现CO2向CH3OH的转化(Q1、Q2均大于0):
反应I:CO2(g)+H2(g)⇌H2O(g)+CO(g)+Q1
反应Ⅱ:2H2(g)+CO(g)⇌CH3OH(g)+Q2
反应I和反应Ⅱ的平衡常数K随温度T的变化如图2所示。

(3)根据图中数据分析可知,T1
(4)目前,许多国家采用CO2代替CO(以煤和天然气为原料)生产CH3OH。请阐述理由:
(5)0.02molCO2通入含有10mL 3 mol/L NaOH溶液中:
①所得溶液中取2mL,滴加几滴稀Ba(OH)2溶液,c(CO
 )
)②反应后的溶液还能吸收CO2的物质的量是
③反应后的溶液中离子浓度由大到小的顺序排列
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是有关物质的转化图,有些反应物、生成物 已略去,它们之间的转化关系如下:
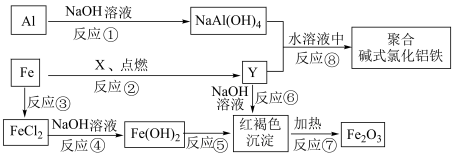
请填写有关空白。
(1) 的化学式是
的化学式是_______ ; 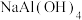 的名称是
的名称是_______ 。
(2)配制 溶液常常加入铁粉,原因是
溶液常常加入铁粉,原因是_______ 。
(3)在敞口容器中进行反应④,实验现象为_______ 。
(4)写出反应⑦的化学方程式:_______ 。
(5)写出下列反应的离子 方程式:
反应①的离子方程式为_______ ;
“聚合碱式氯化铝铁”的化学式为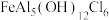 ,则反应③的离子方程式为
,则反应③的离子方程式为_______ 。

请填写有关空白。
(1)
 的化学式是
的化学式是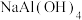 的名称是
的名称是(2)配制
 溶液常常加入铁粉,原因是
溶液常常加入铁粉,原因是(3)在敞口容器中进行反应④,实验现象为
(4)写出反应⑦的化学方程式:
(5)写出下列反应的
反应①的离子方程式为
“聚合碱式氯化铝铁”的化学式为
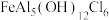 ,则反应③的离子方程式为
,则反应③的离子方程式为
您最近一年使用:0次
【推荐1】饮用水质最是关系人类健康的重要问题。
I.(1)在我国,一些贫困山区的居民至今还饮用井水,但暴雨过后井水浑浊无法饮用。为了能让浑浊的井水尽快变澄清,你会建议他们最好向井水中投入下列物质中的___ (填序号)。
A.NaCl B.Na2CO3C.KAl(SO4)2·12H2O D.CuSO4
(2)ClO2是一种广谱型的消毒剂,将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得。反应中还原剂和氧化剂的物质的量之比为___ 。
(3)“84”消毒液是一种以NaClO为主的消毒剂,广泛应用于医院、食品加工、家庭等的卫生消毒。“84”消毒液中通入CO2能增强消毒效果,写出向“84”消毒液中通入过量CO2的离子方程式:___ 。
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠的溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4++6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中FeSO4是___ (填“氧化剂”或“还原剂”),请写出Na2O2与CO2反应的化学方程式:___ 。
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量之比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:___ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为___ mol。
I.(1)在我国,一些贫困山区的居民至今还饮用井水,但暴雨过后井水浑浊无法饮用。为了能让浑浊的井水尽快变澄清,你会建议他们最好向井水中投入下列物质中的
A.NaCl B.Na2CO3C.KAl(SO4)2·12H2O D.CuSO4
(2)ClO2是一种广谱型的消毒剂,将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得。反应中还原剂和氧化剂的物质的量之比为
(3)“84”消毒液是一种以NaClO为主的消毒剂,广泛应用于医院、食品加工、家庭等的卫生消毒。“84”消毒液中通入CO2能增强消毒效果,写出向“84”消毒液中通入过量CO2的离子方程式:
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠的溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4++6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。该反应中FeSO4是
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量之比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】配平方程式: Zn + HNO3→Zn(NO3)2+N2+H2O
___________________________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:_____________ 。
(2)在海洋循环中,通过如图所示的途径固碳。

①写出钙化作用的离子方程式:_____________ 。
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整:_____________+_____________=(CH2O)x+x18O2+xH2O,_____________
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2,用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图所示),将虚线框中的装置补充完整并标出所用试剂。_____________

②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymLHCl溶液,海水中溶解无机碳的浓度=_____________ mol/L。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:
(2)在海洋循环中,通过如图所示的途径固碳。

①写出钙化作用的离子方程式:
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整:_____________+_____________=(CH2O)x+x18O2+xH2O,
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2,用N2从酸化后的海水中吹出CO2并用碱液吸收(装置示意图如图所示),将虚线框中的装置补充完整并标出所用试剂。

②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymLHCl溶液,海水中溶解无机碳的浓度=
您最近一年使用:0次



