综合利用CO2对构建低碳社会、促进工业可持续发展有重要意义。
途径1:可用工业废气中二氧化碳制备再生能源物质——甲醇。反应原理为:CO2(g)+3H2(g)⇌CH3OH(g) + H2O(g) +53.7kJ
某温度下,向2L密闭容器中通入0.04 mol CO2和0.08 mol H2,测得其压强(p)随时间(t)变化(如图1中)曲线I所示。
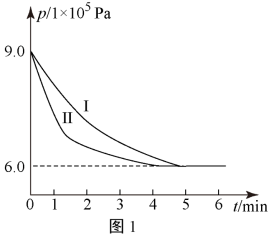
(1)以CO2来表示5 min内的化学反应反应速率υ(CO2)=_______ 。
(2)若只改变某一条件,其他条件相同时,曲线变化为II,则改变的条件是_______ 。
途径2:还可以通过以下途径实现CO2向CH3OH的转化(Q1、Q2均大于0):
反应I:CO2(g)+H2(g)⇌H2O(g)+CO(g)+Q1
反应Ⅱ:2H2(g)+CO(g)⇌CH3OH(g)+Q2
反应I和反应Ⅱ的平衡常数K随温度T的变化如图2所示。
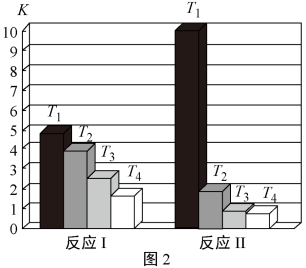
(3)根据图中数据分析可知,T1_______ T2(选填“>”、“<”或“=”);
(4)目前,许多国家采用CO2代替CO(以煤和天然气为原料)生产CH3OH。请阐述理由:_______
(5)0.02molCO2通入含有10mL 3 mol/L NaOH溶液中:
①所得溶液中取2mL,滴加几滴稀Ba(OH)2溶液,c(CO )
)_______ (选填“增大、减小、不变、无法确定”),写出反应的离子方程式_______ ;
②反应后的溶液还能吸收CO2的物质的量是_______ ;
③反应后的溶液中离子浓度由大到小的顺序排列_______ 。
途径1:可用工业废气中二氧化碳制备再生能源物质——甲醇。反应原理为:CO2(g)+3H2(g)⇌CH3OH(g) + H2O(g) +53.7kJ
某温度下,向2L密闭容器中通入0.04 mol CO2和0.08 mol H2,测得其压强(p)随时间(t)变化(如图1中)曲线I所示。

(1)以CO2来表示5 min内的化学反应反应速率υ(CO2)=
(2)若只改变某一条件,其他条件相同时,曲线变化为II,则改变的条件是
途径2:还可以通过以下途径实现CO2向CH3OH的转化(Q1、Q2均大于0):
反应I:CO2(g)+H2(g)⇌H2O(g)+CO(g)+Q1
反应Ⅱ:2H2(g)+CO(g)⇌CH3OH(g)+Q2
反应I和反应Ⅱ的平衡常数K随温度T的变化如图2所示。

(3)根据图中数据分析可知,T1
(4)目前,许多国家采用CO2代替CO(以煤和天然气为原料)生产CH3OH。请阐述理由:
(5)0.02molCO2通入含有10mL 3 mol/L NaOH溶液中:
①所得溶液中取2mL,滴加几滴稀Ba(OH)2溶液,c(CO
 )
)②反应后的溶液还能吸收CO2的物质的量是
③反应后的溶液中离子浓度由大到小的顺序排列
2022·上海闵行·一模 查看更多[3]
更新时间:2021-12-19 11:41:56
|
相似题推荐
【推荐1】氧化还原反应在高中化学中是一类重要的反应类型。 、
、 、
、 、
、 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:
(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
(2)实验室迅速制备少量氯气可利用如下反应: (未配平)。
(未配平)。 与
与 反应生成
反应生成 ,反应后
,反应后 转化为
转化为_______ , 发生反应
发生反应_______ (填“氧化”或“还原”)。
(3) 溶液能与Cu反应制作印刷电路板,其制作原理可用
溶液能与Cu反应制作印刷电路板,其制作原理可用 表示。
表示。
①上式中X的化学式为_______ 。
②若有32g铜参与反应,则参与反应的 的质量为
的质量为_______ g。
③该反应的离子方程式为_______ 。
(4)已知方程式: 。用双线桥法标出电子转移的方向和数目
。用双线桥法标出电子转移的方向和数目_______ 。
(5)某反应的反应物与生成物有 、KCl、
、KCl、 、
、 、HCl、
、HCl、 ,已知氧化性:
,已知氧化性: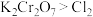 ,写出并配平该化学方程式:
,写出并配平该化学方程式:_______ 。
 、
、 、
、 、
、 是中学化学中常用的氧化剂。回答下列问题:
是中学化学中常用的氧化剂。回答下列问题:(1)下列基本反应类型中一定属于氧化还原反应的是_______(填字母)。
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
 (未配平)。
(未配平)。 与
与 反应生成
反应生成 ,反应后
,反应后 转化为
转化为 发生反应
发生反应(3)
 溶液能与Cu反应制作印刷电路板,其制作原理可用
溶液能与Cu反应制作印刷电路板,其制作原理可用 表示。
表示。①上式中X的化学式为
②若有32g铜参与反应,则参与反应的
 的质量为
的质量为③该反应的离子方程式为
(4)已知方程式:
 。用双线桥法标出电子转移的方向和数目
。用双线桥法标出电子转移的方向和数目(5)某反应的反应物与生成物有
 、KCl、
、KCl、 、
、 、HCl、
、HCl、 ,已知氧化性:
,已知氧化性: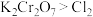 ,写出并配平该化学方程式:
,写出并配平该化学方程式:
您最近一年使用:0次
【推荐2】高锰酸盐具有强氧化性,常用于杀菌消毒。
(1)已知 是一种不稳定的物质,具有强氧化性。可发生反应:
是一种不稳定的物质,具有强氧化性。可发生反应: 。
。
①配平该反应的离子方程式:_______ 。
②该反应的实验现象为_______ 。
③上述反应中,发生还原反应的粒子是_______ (写化学式),每消耗3个 ,反应转移电子的个数为
,反应转移电子的个数为_______ 。
(2)已知某容器中发生了一个化学反应,反应过程中存在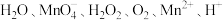 六种粒子。在反应过程中测得
六种粒子。在反应过程中测得 和
和 的粒子数目随时间变化的曲线如图所示。
的粒子数目随时间变化的曲线如图所示。
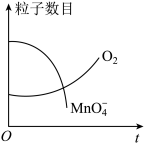
①写出该反应的离子方程式:_______ *。
②该反应中,氧化剂与还原剂的粒子数目之比为_______ 。
③若消耗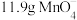 ,则生成氧气的质量为
,则生成氧气的质量为_______ 。
(3)水中的溶解氧 是水生生物生存不可缺少的条件。将水样与
是水生生物生存不可缺少的条件。将水样与 碱性悬浊液混合,反应生成
碱性悬浊液混合,反应生成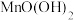 ,实现氧的固定。“氧的固定”中发生反应的化学方程式为
,实现氧的固定。“氧的固定”中发生反应的化学方程式为_______ 。
(1)已知
 是一种不稳定的物质,具有强氧化性。可发生反应:
是一种不稳定的物质,具有强氧化性。可发生反应: 。
。①配平该反应的离子方程式:
②该反应的实验现象为
③上述反应中,发生还原反应的粒子是
 ,反应转移电子的个数为
,反应转移电子的个数为(2)已知某容器中发生了一个化学反应,反应过程中存在
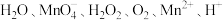 六种粒子。在反应过程中测得
六种粒子。在反应过程中测得 和
和 的粒子数目随时间变化的曲线如图所示。
的粒子数目随时间变化的曲线如图所示。
①写出该反应的离子方程式:
②该反应中,氧化剂与还原剂的粒子数目之比为
③若消耗
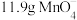 ,则生成氧气的质量为
,则生成氧气的质量为(3)水中的溶解氧
 是水生生物生存不可缺少的条件。将水样与
是水生生物生存不可缺少的条件。将水样与 碱性悬浊液混合,反应生成
碱性悬浊液混合,反应生成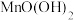 ,实现氧的固定。“氧的固定”中发生反应的化学方程式为
,实现氧的固定。“氧的固定”中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子有_______ (填离子符号)。
(2)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、 、Cl-、
、Cl-、 中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是_______ 。
(3)高铁酸钾 是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为
是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为 (未配平),每生成
(未配平),每生成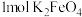 ,转移的电子数为
,转移的电子数为_______ 。
(4)自然界中Cr主要以 价和
价和 价形式存在。
价形式存在。 中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将
中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将 还原。其离子方程式为
还原。其离子方程式为_______ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子有
(2)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、
 、Cl-、
、Cl-、 中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是(3)高铁酸钾
 是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为
是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为 (未配平),每生成
(未配平),每生成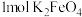 ,转移的电子数为
,转移的电子数为(4)自然界中Cr主要以
 价和
价和 价形式存在。
价形式存在。 中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将
中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将 还原。其离子方程式为
还原。其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g)ΔH>0,已知该反应在2404℃,平衡常数K=6.4×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为___________ ,N2的转化率是___________ 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是___________。
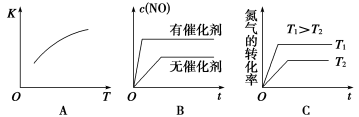
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下图变化趋势正确的是______ (填字母序号)。
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数________ (填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应___________ (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是___________ 。
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是___________。
| A.消耗1molN2同时生成1molO2 | B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 | D.2v正(N2)=v逆(NO) |

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
您最近一年使用:0次
【推荐2】下列反应在210℃达到平衡:
①PCl5(g) PCl3(g)+Cl2(g) ΔH>0,K=1;
PCl3(g)+Cl2(g) ΔH>0,K=1;
②CO(g)+Cl2(g) COCl2(g) ΔH<0,K=5×104;
COCl2(g) ΔH<0,K=5×104;
③COCl2(g) CO(g)+Cl2(g);
CO(g)+Cl2(g);
(1)根据反应①的平衡常数K表达式,下列等式必定成立的是____ 。
A.c(PCl5)=c(PCl3)=c(Cl2)=1 B.c(PCl5)=c(PCl3)∙c(Cl2)=1
C.c(PCl5)=c(PCl3)∙c(Cl2)
反应②和反应③的平衡常数K表达式________ (填“相同”或“不同”)。
(2)降低Cl2的浓度,反应③的K值________ (填“增大”“减小”或“不变”)。
(3)要使反应①和反应②的K值相等,应采取的措施是________ 。
A.反应①②同时升温 B.反应①②同时降温
C.反应①降温,反应②维持在210℃
①PCl5(g)
 PCl3(g)+Cl2(g) ΔH>0,K=1;
PCl3(g)+Cl2(g) ΔH>0,K=1;②CO(g)+Cl2(g)
 COCl2(g) ΔH<0,K=5×104;
COCl2(g) ΔH<0,K=5×104;③COCl2(g)
 CO(g)+Cl2(g);
CO(g)+Cl2(g);(1)根据反应①的平衡常数K表达式,下列等式必定成立的是
A.c(PCl5)=c(PCl3)=c(Cl2)=1 B.c(PCl5)=c(PCl3)∙c(Cl2)=1
C.c(PCl5)=c(PCl3)∙c(Cl2)
反应②和反应③的平衡常数K表达式
(2)降低Cl2的浓度,反应③的K值
(3)要使反应①和反应②的K值相等,应采取的措施是
A.反应①②同时升温 B.反应①②同时降温
C.反应①降温,反应②维持在210℃
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在化学反应A(g)+B(g) 2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。

(1)Q___________ 0 (填“>”“<”或“=”)。
(2)熵变ΔS___________ 0(填“>”“<”或“=”)。
(3)该反应___________ 自发进行(填“能”或“不能”)。
(4)升高温度,平衡常数K___________ (填“增大”“减小”或“不变”),平衡向___________ 方向移动,平衡向该方向移动的理由是___________ 。
 2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
2C(g)+D(g) ΔH=Q kJ·mol-1过程中的能量变化如图所示,回答下列问题。
(1)Q
(2)熵变ΔS
(3)该反应
(4)升高温度,平衡常数K
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】 ,两种酸的电离平衡常数如下表。
,两种酸的电离平衡常数如下表。
 的电离平衡常数表达式
的电离平衡常数表达式
________ 。
 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为________ 。
 溶液和
溶液和 溶液反应的主要离子方程式为
溶液反应的主要离子方程式为________ 。
 ,两种酸的电离平衡常数如下表。
,两种酸的电离平衡常数如下表。  |  | |
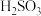 |  |  |
 |  |  |
 的电离平衡常数表达式
的电离平衡常数表达式
 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为 溶液和
溶液和 溶液反应的主要离子方程式为
溶液反应的主要离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】NaClO溶液具有漂白能力,已知25℃时, ,向含有NaOH的NaClO溶液中逐滴滴入
,向含有NaOH的NaClO溶液中逐滴滴入 溶液,滴加过程中溶液的pH随
溶液,滴加过程中溶液的pH随 溶液的体积的变化曲线及实验现象见下表。
溶液的体积的变化曲线及实验现象见下表。
(1)NaClO的电子式是_______ ,次氯酸钠溶液中离子浓度大小顺序是:_______ 。
(2)25℃,pH=7.0的NaClO和HClO的混合溶液中,[HClO]_______ [ ] (填<,>或=)。
] (填<,>或=)。
 ,向含有NaOH的NaClO溶液中逐滴滴入
,向含有NaOH的NaClO溶液中逐滴滴入 溶液,滴加过程中溶液的pH随
溶液,滴加过程中溶液的pH随 溶液的体积的变化曲线及实验现象见下表。
溶液的体积的变化曲线及实验现象见下表。| 变化曲线 | 实验现象 |
 | ⅰ.A→B产生红褐色沉淀 ⅱ.B→C红褐色沉淀的量增多 ⅲ.C→D红褐色沉淀的量增多 ⅳ.D点附近产生有刺激性气味的气体 ⅴ.D→E红褐色沉淀的量略有增多 |
(2)25℃,pH=7.0的NaClO和HClO的混合溶液中,[HClO]
 ] (填<,>或=)。
] (填<,>或=)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.在室温下,蒸馏水稀释0.01mol/LHA溶液时。
(1)下列呈减小趋势的是_______。
Ⅱ.室温下,取pH=2的盐酸和HA溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示:

(2)图中表示HA溶液pH变化曲线的是_______ (填“A”或“B”)。
(3)设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1_______ m2(填“>”<”或“=”)。
III.盐是一类常见的电解质,实验表明盐溶液不一定呈中性,也可能呈酸性和碱性。
(4)CH3COONa、NH4Cl、KNO3的水溶液分别呈_______ 性、_______ 性、_______ 性。
(5)将AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是_______ 。
(6)0.1mol·L-1碳酸钠溶液和0.1mol·L-1碳酸氢钠溶液等体积混合后,溶液中离子浓度由大到小的顺序是_______ 。
(1)下列呈减小趋势的是_______。
| A.水的电离程度 | B. |
| C.溶液中c(H+)和c(OH-)的乘积 | D.溶液中c(A-)•c(HA)的值 |
Ⅱ.室温下,取pH=2的盐酸和HA溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示:

(2)图中表示HA溶液pH变化曲线的是
(3)设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1
III.盐是一类常见的电解质,实验表明盐溶液不一定呈中性,也可能呈酸性和碱性。
(4)CH3COONa、NH4Cl、KNO3的水溶液分别呈
(5)将AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是
(6)0.1mol·L-1碳酸钠溶液和0.1mol·L-1碳酸氢钠溶液等体积混合后,溶液中离子浓度由大到小的顺序是
您最近一年使用:0次



