下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
| A | B | C | D | |
| 勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏加德罗定律 | |
| 实 验 方 案 | 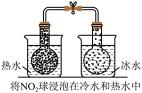 | 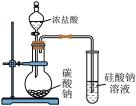 | 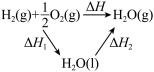 |  |
| 结 果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡, 试管中出现浑浊 | 测得ΔH为ΔH1、 ΔH2的和 | H2与O2的体积比 约为2:1 |
| A.A | B.B | C.C | D.D |
更新时间:2019-04-19 08:50:25
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】三个密闭容器中分别充入N2、H2、CO2三种气体,以下各种情况下排序正确的是
| A.当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(CO2) |
| B.当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(CO2) |
| C.当它们的质量和温度、压强均相同时,三种气体的体积:V(CO2)>V(N2)>V(H2) |
| D.当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(CO2) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】120℃、101.3kPa,甲烷(CH4)和过量的O2的混合物,用电火花引燃(CH4+2O2=CO2+2H2O)后,恢复到原来的温度和压强,测得反应后气体密度为相同条件下H2密度的15倍,则原混合气体中甲烷和氧气的体积比为( )
| A.2∶1 | B.1∶2 | C.1∶7 | D.1∶5 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在一定温度下,2HI(g) H2(g)+I2(g) △H>0的反应达到平衡,下列条件的改变将使混含气体颜色加深的是
H2(g)+I2(g) △H>0的反应达到平衡,下列条件的改变将使混含气体颜色加深的是
 H2(g)+I2(g) △H>0的反应达到平衡,下列条件的改变将使混含气体颜色加深的是
H2(g)+I2(g) △H>0的反应达到平衡,下列条件的改变将使混含气体颜色加深的是| A.降低HI的浓度 | B.升高反应温度 | C.增大容器体积 | D.增大氢气浓度 |
您最近半年使用:0次
单选题
|
较难
(0.4)
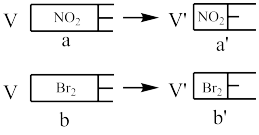
【推荐2】有两个相同带活塞的容器,向容器a中充入NO2(g)待颜色不再变化,再向容器b中充入溴蒸汽,使两容器的颜色和体积相等〔注意:同浓度的NO2和Br2蒸汽颜色相同,2NO2(g) N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
 N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
N2O4(g)(无色),迅速将两容器同时压缩(假设气体不液化),下列说法正确的是
| A.a→a′过程中,颜色突然加深,然后逐渐变浅,最终颜色比原来的浅 |
| B.若对a和b以极慢的速度缓缓压缩,则a和b的颜色均慢慢加深,但在每一个相同的时间点,b的颜色总比a的深 |
| C.假设容器和活塞均为无色,从容器左侧观察a和a′,a′的颜色比a浅 |
| D.气体的物质的量:na′一定大于nb′ |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】在一体积可变的密闭容器里,加入一定量的M、N,发生反应aM(g)+bN(g) cP(g),△H=Q kJ·mol-1,反应达平衡时,P的物质的量浓度(mol·L-1)与容器体积和温度的关系如下表,其中,说法正确的是
cP(g),△H=Q kJ·mol-1,反应达平衡时,P的物质的量浓度(mol·L-1)与容器体积和温度的关系如下表,其中,说法正确的是
 cP(g),△H=Q kJ·mol-1,反应达平衡时,P的物质的量浓度(mol·L-1)与容器体积和温度的关系如下表,其中,说法正确的是
cP(g),△H=Q kJ·mol-1,反应达平衡时,P的物质的量浓度(mol·L-1)与容器体积和温度的关系如下表,其中,说法正确的是
  c(P) c(P) | 1 L | 2 L | 3 L | ||||
| 100℃ | 1.30 | 1.00 | 0.70 | ||||
| 200℃ | 1.20 | 0.90 | 0.62 | ||||
| 300℃ | 1.00 | 0.75 | 0.53 |
| A.Q>0 |
| B.温度不变,扩大容器体积,正反应速率增大,逆反应速率减小 |
| C.容器体积不变,升高温度,平衡体系中M的体积百分含量减小 |
| D.a+b<c |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】Na、Mg、S、Cl是第三周期的四种元素,下列判断错误的是( )
| A.碱性NaOH>Mg(OH)2 |
| B.原子半径r(Mg)<r(S) |
| C.离子半径r(Na+)>r(Mg2+) |
| D.氧化性Cl2>S |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列各组性质比较中正确的是
①颜色:氯化银、溴化银、碘化银,颜色逐渐加深
②离子还原性: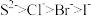
③酸性:
④金属性: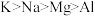
⑤气态氢化物稳定性:
①颜色:氯化银、溴化银、碘化银,颜色逐渐加深
②离子还原性:
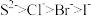
③酸性:

④金属性:
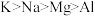
⑤气态氢化物稳定性:

| A.①②③ | B.①④⑤ | C.②③④ | D.①③④⑤ |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】化学是一门以实验为基础的学科。通过分析下列实验现象,得出的结论中正确的是
| 选项 | 实验操作 | 结论 |
| A | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液,观察到溶液变红 | Fe(NO3)2样品已氧化变质 |
| B | 向2mL ZnSO4 和CuSO4的混合溶液中逐滴加入0.01mol/LNa2S溶液,先出现白色沉淀 | 相同温度下,Ksp(ZnS)<Ksp(CuS) |
| C | 取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧化钠溶液中和酸,再加少量碘水,溶液未变蓝 | 淀粉已经完全水解 |
| D | 向NaAlO2的试管中滴加碳酸氢钠溶液,产生白色沉淀 | AlO2-结合氢离子的能力比碳酸根强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列各项操作中符合“先出现沉淀后沉淀完全溶解”现象的有( )组
①向饱和碳酸钠溶液中通入CO2 至过量 ②向Fe(OH)3胶体中逐滴滴加稀H2SO4至过量
③向BaCl2溶液中通入CO2 至过量 ④向澄清石灰水中逐渐通入CO2至过量
⑤向Al2(SO4)3溶液中逐滴滴加Ba(OH)2至过量
⑥向NaAlO2溶液中逐滴滴加盐酸至过量 ⑦向NaAlO2溶液中逐渐通入CO2至过量
①向饱和碳酸钠溶液中通入CO2 至过量 ②向Fe(OH)3胶体中逐滴滴加稀H2SO4至过量
③向BaCl2溶液中通入CO2 至过量 ④向澄清石灰水中逐渐通入CO2至过量
⑤向Al2(SO4)3溶液中逐滴滴加Ba(OH)2至过量
⑥向NaAlO2溶液中逐滴滴加盐酸至过量 ⑦向NaAlO2溶液中逐渐通入CO2至过量
| A.2 | B.3 | C.4 | D.5 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】下列实验操作、现象和解释或结论完全正确的是
| 选项 | 实验操作 | 解释或结论 |
| A | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液。 | 通过测定白色沉淀的质量,可推算二氧化硫的物质的量 |
| B | 实验室用浓硫酸和乙醇制取乙烯,将产生的气体通入溴水中。 | 若溴水褪色,则证明混合气体中有乙烯 |
| C | 向盛有2 mL 0.1mol/L 溶液的试管中滴加2~4滴0.1mol/L NaOH溶液,产生白色沉淀,向上层清液中滴加4滴0.1mol/L 溶液的试管中滴加2~4滴0.1mol/L NaOH溶液,产生白色沉淀,向上层清液中滴加4滴0.1mol/L 溶液,生成红褐色沉淀。 溶液,生成红褐色沉淀。 | 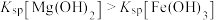 |
| D | 把 和 和 的混合气体通入两只连通的烧瓶,一只烧瓶浸泡在热水中,另一只浸泡在冰水中。浸泡在热水中的烧瓶内红棕色加深。 的混合气体通入两只连通的烧瓶,一只烧瓶浸泡在热水中,另一只浸泡在冰水中。浸泡在热水中的烧瓶内红棕色加深。 | 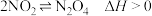 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



