1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经150年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式 填空回答以下问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___ ;
(2)元素①的单质电子式为____ 。
(3)比较③、⑤元素的金属性强弱___ >___ ;并写出它们最高价氧化物对应的水化物间反应的化学方程式____ 。
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是____ 。
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是_____ ;
(6)工业制取⑥的单质的反应的化学方程式为_______ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)元素①的单质电子式为
(3)比较③、⑤元素的金属性强弱
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是
(6)工业制取⑥的单质的反应的化学方程式为
更新时间:2019-05-08 09:20:59
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】实验室用 还原
还原 (沸点:
(沸点: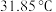 ,易与水反应)制备高纯硅的装置如图所示(夹持装置和尾气处理装置已略去)。
,易与水反应)制备高纯硅的装置如图所示(夹持装置和尾气处理装置已略去)。
(1)装置I中发生反应的离子方程式为___________ 。
(2)装置II盛装的是___________ ,作用是___________ ;装置III水浴加热的目的是___________ 。
(3)实验开始时应先___________ ,再___________ ,这样操作的目的是___________ 。
(4)装置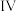 导出的气体在空气中易形成白雾,写出装置
导出的气体在空气中易形成白雾,写出装置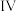 中发生反应的化学方程式:
中发生反应的化学方程式:_______ 。
(5)可利用高纯硅制备甲硅烷 ,其转化过程为高纯硅
,其转化过程为高纯硅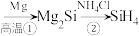 (同时有
(同时有 生成)。反应②中生成
生成)。反应②中生成 与
与 的体积之比为
的体积之比为___________ 。
 还原
还原 (沸点:
(沸点: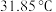 ,易与水反应)制备高纯硅的装置如图所示(夹持装置和尾气处理装置已略去)。
,易与水反应)制备高纯硅的装置如图所示(夹持装置和尾气处理装置已略去)。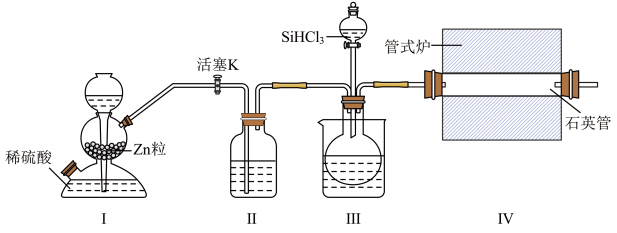
(1)装置I中发生反应的离子方程式为
(2)装置II盛装的是
(3)实验开始时应先
(4)装置
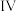 导出的气体在空气中易形成白雾,写出装置
导出的气体在空气中易形成白雾,写出装置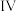 中发生反应的化学方程式:
中发生反应的化学方程式:(5)可利用高纯硅制备甲硅烷
 ,其转化过程为高纯硅
,其转化过程为高纯硅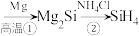 (同时有
(同时有 生成)。反应②中生成
生成)。反应②中生成 与
与 的体积之比为
的体积之比为
您最近一年使用:0次
【推荐2】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制品的主要原料。
(1)已知多晶硅第三代工业制取流程如图所示。
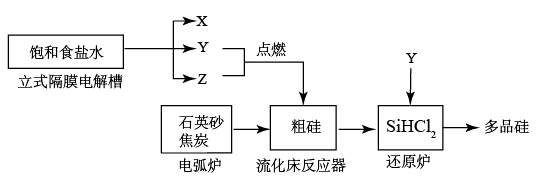
①物质Z的名称是_______ 。
②用石英砂和焦在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为_______
③在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和_______ 。
(2)利用晶体硅的粉末与干燥的氮气在1300~1400℃下反应,可制取结构陶瓷材料氮化硅(Si3N4)。现用如图所示装置(部分仪器已省略)制取少量氮化硅。
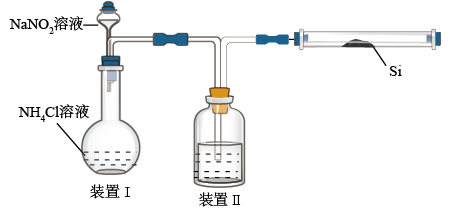
①装置II中所盛试剂为_______ 。
②装置I和装置皿均需要加热,实验中应先_______ (填“皿”或“I”)的热源。
(3)由晶体硅制成的n型半导体、p型半导体可用于太阳能电池。一种太阳能储能电池的工作原理如图所示,已知锂离子电池的总反应为:Li1-xNiO2+xLiC6 LiNiO2+xC6。完成下列问题。
LiNiO2+xC6。完成下列问题。
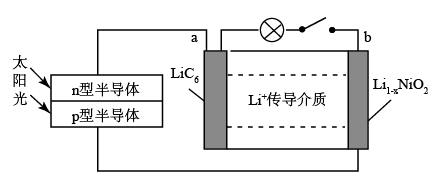
①该锂离子电池充电时,n型半导体作为电源_______ .(填“正”或“负”)极。
②该锂离子电池放电时,b极上的电极反应式为_______ 。
(1)已知多晶硅第三代工业制取流程如图所示。

| 发生的主要反应 | |
| 电弧炉 | SiO2+2C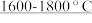 Si+CO↑ Si+CO↑ |
| 流化床反应器 | Si+3HCl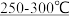 SiHCl3+H2 SiHCl3+H2 |
②用石英砂和焦在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为
③在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |

①装置II中所盛试剂为
②装置I和装置皿均需要加热,实验中应先
(3)由晶体硅制成的n型半导体、p型半导体可用于太阳能电池。一种太阳能储能电池的工作原理如图所示,已知锂离子电池的总反应为:Li1-xNiO2+xLiC6
 LiNiO2+xC6。完成下列问题。
LiNiO2+xC6。完成下列问题。
①该锂离子电池充电时,n型半导体作为电源
②该锂离子电池放电时,b极上的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】以含硅废石(主要成分为SiO2、含少量Fe3O4、Al2O3等杂质)为原料,工业上有以下两种制备高纯硅的工艺。已知:SiCl4沸点57.7 °C ,遇水强烈水解;SiHCl3沸点31.5°C,且能与H2O强烈反应,并在空气中易自燃。

(1)为了提高酸浸速率,可以采取的措施是__________ (写出一种措施)。
(2)酸浸所得的浸液中含有的金属离子是__________ (填化学式)。
(3)检验酸浸所得固体是否洗涤干净的方法是__________ 。
(4)还原过程已得到单质硅,但还要进行后续操作的目的是__________ ,还原过程若加入的焦炭过量,反应所得固体粗硅中可能含有杂质__________ 。
(5)分别写出工艺I和工艺II均在高温条件下制备纯硅的化学方程式:__________ 、__________ ,工艺II与工艺I 相比,制备纯硅的优点是__________ 。

(1)为了提高酸浸速率,可以采取的措施是
(2)酸浸所得的浸液中含有的金属离子是
(3)检验酸浸所得固体是否洗涤干净的方法是
(4)还原过程已得到单质硅,但还要进行后续操作的目的是
(5)分别写出工艺I和工艺II均在高温条件下制备纯硅的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、D、E四种元素均为短周期元素,原子序数逐渐增大。A元素原子的核外电子数、电子层数和最外层电子数均相等。B、D、E三种元素在周期表中的相对位置如图①所示,只有E元素的单质能与水反应生成两种酸,甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素:W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质,X分子含有10个电子。它们之间的转化关系如图②所示。
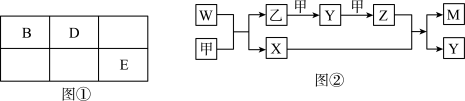
请回答下列问题:
(1)E元素价电子排布式为_____________ ,Z化学式为_____________ ;X分子的空间构型为_____________ 。
(2)E元素可分别与钙(Ca)、钛(Ti)元素形成化合物,其中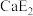 的熔点为782℃,沸点1600℃,
的熔点为782℃,沸点1600℃,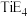 的熔点为−24.1℃,沸点为136.4℃,两者熔沸点差别很大的原因是
的熔点为−24.1℃,沸点为136.4℃,两者熔沸点差别很大的原因是_______________________________________ 。
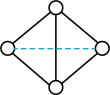
(3)已知一种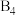 分子结构如图所示:断裂1mol B−B键吸收167kJ的热量,生成1mol B≡B放出942kJ热量。则由
分子结构如图所示:断裂1mol B−B键吸收167kJ的热量,生成1mol B≡B放出942kJ热量。则由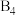 气态分子变成
气态分子变成 气态分子的热化学方程式为:
气态分子的热化学方程式为:_________________________ (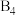 和
和 分子用化学式表示)。
分子用化学式表示)。
(4)将一定量的 、
、 的混合气体放入1L恒容密闭容器中,在200℃下达到平衡。测得平衡气体的总物质的量为0.4mol,其中
的混合气体放入1L恒容密闭容器中,在200℃下达到平衡。测得平衡气体的总物质的量为0.4mol,其中 为0.1mol,
为0.1mol, 为0.1mol。则该条件下
为0.1mol。则该条件下 的平衡转化率为
的平衡转化率为_____________ ,该温度下的平衡常数为_____________ 。

请回答下列问题:
(1)E元素价电子排布式为
(2)E元素可分别与钙(Ca)、钛(Ti)元素形成化合物,其中
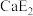 的熔点为782℃,沸点1600℃,
的熔点为782℃,沸点1600℃,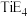 的熔点为−24.1℃,沸点为136.4℃,两者熔沸点差别很大的原因是
的熔点为−24.1℃,沸点为136.4℃,两者熔沸点差别很大的原因是(3)已知一种
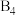 分子结构如图所示:断裂1mol B−B键吸收167kJ的热量,生成1mol B≡B放出942kJ热量。则由
分子结构如图所示:断裂1mol B−B键吸收167kJ的热量,生成1mol B≡B放出942kJ热量。则由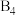 气态分子变成
气态分子变成 气态分子的热化学方程式为:
气态分子的热化学方程式为: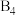 和
和 分子用化学式表示)。
分子用化学式表示)。
(4)将一定量的
 、
、 的混合气体放入1L恒容密闭容器中,在200℃下达到平衡。测得平衡气体的总物质的量为0.4mol,其中
的混合气体放入1L恒容密闭容器中,在200℃下达到平衡。测得平衡气体的总物质的量为0.4mol,其中 为0.1mol,
为0.1mol, 为0.1mol。则该条件下
为0.1mol。则该条件下 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】表给出了五种元素的相关信息,其中B、C、D、E均为短周期主族元素。
根据上述信息填空:
(1)D在元素周期表中的位置是____ 。
(2) B2D与DC2反应能生成D的单质,该反应中作还原剂的是_____ (填化学式)。
(3)写出E2B4的结构式:___ 。E2B4可用作火箭燃料,与B2C2反应可放出大量的热,同时生成两种无污染的物质,写出上述反应的化学方程式:_______ 。
(4)由A形成的简单低价态的阳离子在酸性条件下可被B2C2氧化,请写出该反应的离子方程式:_______ 。
| 元素 | 相关信息 |
| A | 纯净的A的单质是银白色的,可又被划分为黑色金属,其原因是表面常附有黑色的、有磁性的氧化物 |
| B | 在常温、常压下,其单质为气体,是一种最清洁的燃料 |
| C | 其常见单质为空气的重要组分之一,也是地壳中含量最高的元素 |
| D | 室温下其单质为固体,其氧化物大量排放会形成酸雨,造成空气污染 |
| E | 其常见单质通常可用作保护气,是空气的主要成分。该元素的某种氧化物为红棕色气体 |
(1)D在元素周期表中的位置是
(2) B2D与DC2反应能生成D的单质,该反应中作还原剂的是
(3)写出E2B4的结构式:
(4)由A形成的简单低价态的阳离子在酸性条件下可被B2C2氧化,请写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为_____________________________ 。
(2)比较B与C简单氢化物的热稳定性:_________ >____ 。(填化学式)
(3)D,C两元素组成的化合物D2C2与水反应的化学方程式为__________________________
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是______ 。
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
(1)E在元素周期表中的位置为
(2)比较B与C简单氢化物的热稳定性:
(3)D,C两元素组成的化合物D2C2与水反应的化学方程式为
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是___________ (填元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是___________ (写分子式,只答一条即可)。元素⑨和⑩形成的化合物的化学式为___________ ;元素①的原子价电子排布式是___________ 。
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是___________ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是___________ (填名称),可以验证你的结论的是下列中的___________ (填序号)。
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
| 性质元素 | 原子半径(1019m) | 最高价态 | 最低价态 |
| ① | 1.02 | +6 | 2 |
| ② | 2.27 | +1 | — |
| ③ | 0.74 | — | 2 |
| ④ | 1.43 | +3 | — |
| ⑤ | 0.77 | +4 | 4 |
| ⑥ | 1.10 | +5 | 3 |
| ⑦ | 0.99 | +7 | 1 |
| ⑧ | 1.86 | +1 | — |
| ⑨ | 0.75 | +5 | 3 |
| ⑩ | 1.17 | +4 | 4 |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】X、Y、Z、R为短周期主族元素,X为原子半径最大的短周期元素,Y的气态氢化物与其最高价氧化物对应的水化物可反应生成离子化合物,Z元素的单质为淡黄色固体,R与Z同周期,R的最低负价和最高正价分别为−1,+7,另有元素W,其原子序数为34。
(1)元素W在周期表中位置为___________ ,原子结构示意图为___________ 。
(2)X、Y、Z、R元素形成的四种简单离子半径由大到小顺序为___________ (用离子符号表示)。
(3)Y的气态氢化物可与R的单质反应产生白烟,该反应的化学方程式为___________ ,Y的某种氢化物电子数目为18,该氢化物的电子式为___________ 。
(4)设计一个简单可行的实验方案验证Z与R的非金属性强弱___________ 。
(1)元素W在周期表中位置为
(2)X、Y、Z、R元素形成的四种简单离子半径由大到小顺序为
(3)Y的气态氢化物可与R的单质反应产生白烟,该反应的化学方程式为
(4)设计一个简单可行的实验方案验证Z与R的非金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中的位置为_______ ,B的离子结构示意图_______ 。
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)_______ 。C单质与水反应生成的具有漂白性物质的电子式_______
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b.SeO2 既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3
d.非金属性比C元素的强
(4)已知A的某种氢化物相对分子质量为58,写出它的所有可能结构(结构简式):_______ 。
| 元素 | 相关信息 |
| A | 自然界中形成化学物种类最多的元素 |
| B | 单质的焰色反应为黄色 |
| C | 单质是黄绿色气体,可用于自来水消毒 |
| D | −2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中的位置为
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是(填化学式)
(3)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.SeO2 既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为H2SeO3
d.非金属性比C元素的强
(4)已知A的某种氢化物相对分子质量为58,写出它的所有可能结构(结构简式):
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】随着原子序数的递增,八种短周期元素(用字母x~h表示)的原子半径相对大小、最高正价或最低负价的变化如图所示。请回答下列问题:
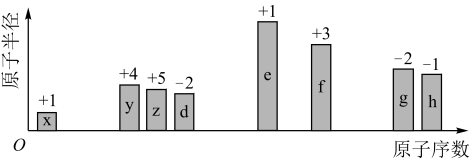
(1)x形成的阴离子的结构示意图为___________ 。
(2)如果1个z原子中含8个中子,则其原子符号为___________ 。
(3)f的最高价氧化物对应水化物和h的最高价氧化物对应的水化物相互反应的离子反应方程式___________ 。
(4)比较d、e常见离子的半径大小:___________ (填离子符号,用“>”连接)。
(5)用电子式表示h的氢化物形成过程___________ 。

(1)x形成的阴离子的结构示意图为
(2)如果1个z原子中含8个中子,则其原子符号为
(3)f的最高价氧化物对应水化物和h的最高价氧化物对应的水化物相互反应的离子反应方程式
(4)比较d、e常见离子的半径大小:
(5)用电子式表示h的氢化物形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题。
(1)②的原子结构示意图是___________ 。
(2)化学性质最不活泼的元素是___________ (填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是______ (填离子符号)。
(4)表中④⑧⑨元素的氢化物的稳定性由强到弱的顺序为_______ (填化学式)。
(5)表中元素⑤与元素⑥金属性更强的是_______ (填化学式),这两种元素的最高价氧化物对应的水化物之间反应的离子方程式为______ ;
(6)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质的化学式为____ ,碱性最强的物质的化学式为_____ 。
| 族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)表中④⑧⑨元素的氢化物的稳定性由强到弱的顺序为
(5)表中元素⑤与元素⑥金属性更强的是
(6)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E、F为短周期主族元素,且原子序数依次增大,A为原子半径最小的元素,A、C常温下能形成两种液态化合物A2C和A2C2,A、D同主族,C、F同主族,B元素质子数为A、D质子数之和的一半,E元素M层与K层电子数相同。
请用化学用语回答下列问题:
(1)E元素在周期表中的位置为_____ ;化合物D2F中含有的化学键为______ ;化合物D2C2的电子式为______ 。
(2)热稳定性:A2C_____ A2F(填“>”或“<”):D、E的最高价氧化物对应水化物的碱性强弱:______ >_____ 。(填化学式)
(3)E在BC2中燃烧的化学方程式为_____ 。
(4)D单质与水反应的离子反应方程式______ 。
(5)C、D、F三种元素形成的简单离子,其半径由大到小的顺序是_____ 。(用离子符号表示)
请用化学用语回答下列问题:
(1)E元素在周期表中的位置为
(2)热稳定性:A2C
(3)E在BC2中燃烧的化学方程式为
(4)D单质与水反应的离子反应方程式
(5)C、D、F三种元素形成的简单离子,其半径由大到小的顺序是
您最近一年使用:0次



